Clear Sky Science · tr
Kristalize nitrijen zincir radikal anyonları
Neden kararsız nitrijen zincirleri önemli
Hava olarak soluduğumuz karışımın büyük kısmını nitrojen gazı oluşturur, ancak üst atmosfer veya patlayıcı maddelerin içi gibi bazı aşırı ortamlarda nitrojen, muazzam kimyasal enerji depolayan enerjik zincirlere bağlanabilir. Bu zincirler gündelik koşullarda neredeyse anında parçalanma eğiliminde olduğundan, bugüne dek yalnızca uzay benzeri plazmalarda veya ezici basınçlar altında geçici biçimde incelenmişlerdi. Bu makale uzun süre ulaşılamaz kabul edilen bir şeyi bildiriyor: kırılgan dört atomlu bir nitrijen zincirini güvenli biçimde içinde tutan, oda sıcaklığında katı kristaller; bu, bu tür yüksek enerjili nitrijen formlarının nasıl davrandığına ve bir gün sentez ile malzemelerde kontrollü reaktif nitrijen kaynakları olarak nasıl kullanılabileceğine dair yeni bir pencere açıyor. 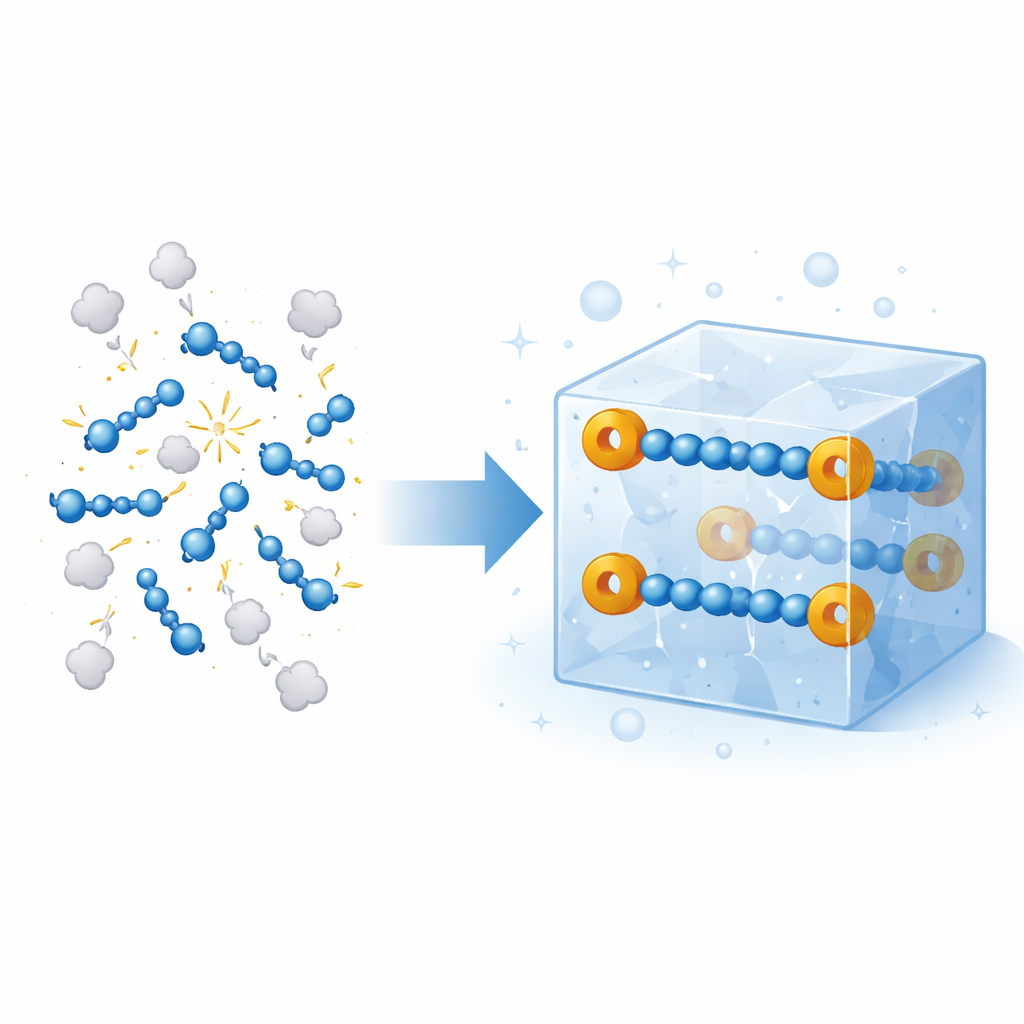
Gökyüzü kimyasından laboratuvara
Üçten fazla nitrijen atomu içeren uzun nitrijen zincirleri, Dünya’nın iyonosferinde ve Satürn’ün uydusu Titan’ın puslu atmosferinde biliniyor; burada yoğun radyasyon ve yüklü parçacıklar N2 moleküllerini kısa süreliğine egzotik iyonlar ve radikaller halinde birleştiriyor. Benzer nitrijen zincirleri, muazzam basınçlarla sıkıştırılmış yoğun katılarda da saptandı ve çok kararlı N2 gazına “geri sıçrama” eğiliminde olduklarından ileri itici ve patlayıcılar için cazip adaylar oluşturuyor; bu süreç enerji açığa çıkarıyor. Sorun şu ki, bu aynı eğilim normal koşullarda onları son derece kısa ömürlü ve tehlikeli kılıyor. Kimyagerler bunları metal atomlarına bağlayarak ya da hacimli organik grupların içine gömerek yatıştırmaya çalıştılar, ancak ekstra bir elektron taşıyan—yani bir radikal anyon olan—gerçek "serbest" nitrijen zincirleri bir şişe içinde izole edilemeyecek kadar reaktif kaldı.
Kararlı dört‑nitrijen zinciri inşa etmek
Yazarlar, metal atomlarına güvenmeden dört‑nitrijenli bir radikal anyonun, {N4}•−, sağlam bir versiyonunu oluşturmayı hedeflediler. Zaten üç‑nitrojen fragmanı içeren yaygın laboratuvar bileşikleri olan basit aril azidlerden başladılar. Bu azidleri potasyum kaynağı ve metal iyonunu saran taç benzeri bir ligand varlığında indirgederek, iki azid biriminin baş‑uça bağlanmasını teşvik ettiler ve her uçta bromlu bir benzen halkasıyla kaplı doğrusal bir N–N–N–N zinciri oluşturdular. Ortaya çıkan anyon, [(4‑BrC6H4)2N4]•− olarak not edildi ve havadan uzak tutulduğunda katı hâlde haftalarca kararlı kalan çarpıcı siyah iğne kristaller halinde kristalleşti. X‑ışını kırınımı, tipik tek ve çift bağlar arasındaki bağ uzunluklarına sahip neredeyse düz dört nitrijen atomlu bir zincir gösteriyor; bu da ekstra elektronun tek bir atoma hapsedilmek yerine paylaşıldığını (delokalize olduğunu) gösteriyor.
Eşleşmemiş elektronun nerede yaşadığını görmek
Bu zincirin alışılmadık derecede kalıcı olmasının nedenini anlamak için ekip, çoklu spektroskopik yöntemleri kuantum‑kimyasal hesaplamalarla birleştirdi. Eşleşmemiş elektronları algılayan bir teknik olan elektron paramanyetik rezonans, radikal karakterin tüm moleküle yayıldığını ancak aromatik halkaların yanındaki iki uç nitrijende en güçlü olduğunu ortaya koydu. Hesaplanmış spin‑yoğunluğu haritaları, eşleşmemiş elektronun çoğunun N4 biriminde yer aldığını; benzen halkalarının ise klasik benzylik radikallerde olduğu gibi elektronun yayılmasına ve stabilize edilmesine yardımcı olan "emniyet valfleri" gibi davrandığını doğruluyor. Morötesi–görünür spektroskopi ve teorik analizler ayrıca, tamamen nitrijen atomlarından oluşan basit bir karbon zincirini andıran bir elektron‑paylaşım orbital ağı olduğunu gösteriyor. 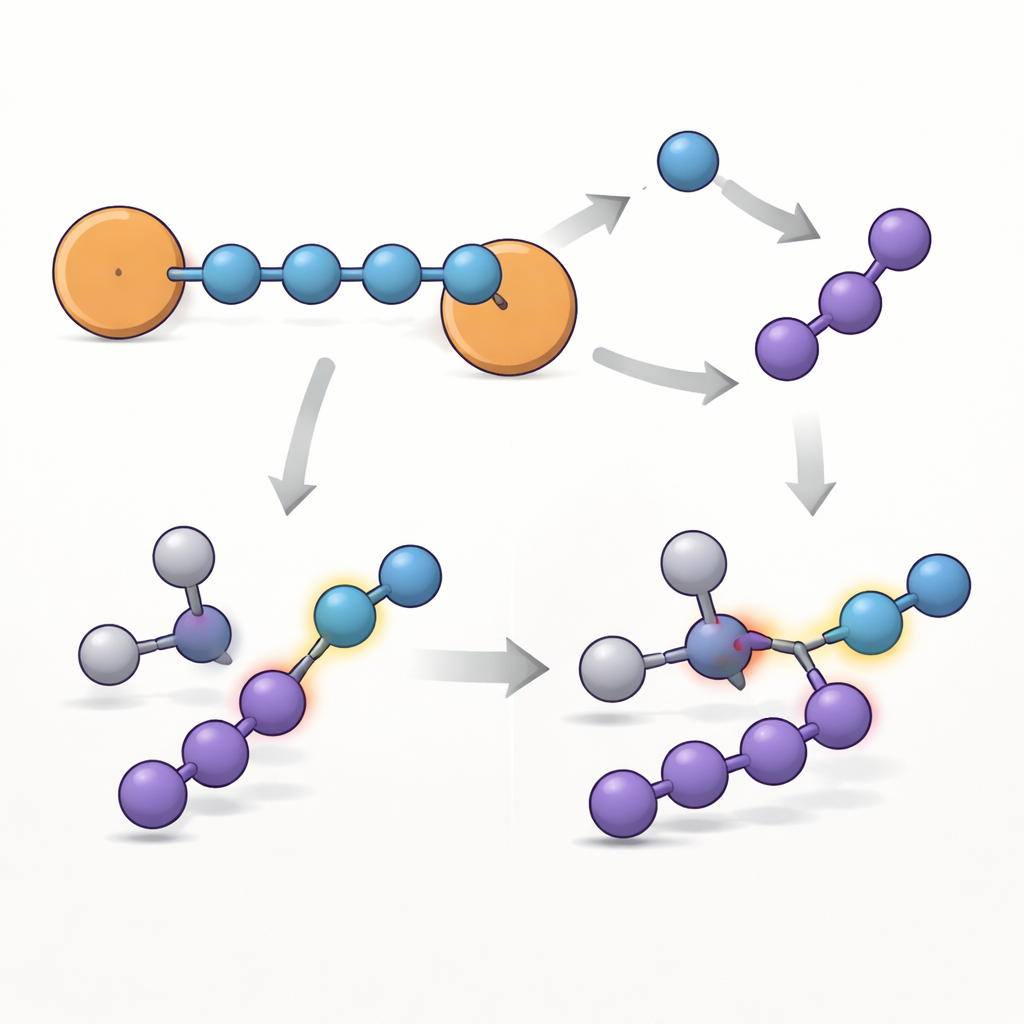
Bir zincir ailesi ve yeni bir nitrijen kaynağı
Yaklaşım genel olduğunu kanıtladı: aromatik halkalardaki yerine göre (floro, kloro, metil veya yerinde phenil) değişiklik yaparak yazarlar ilgili {N4}•− moleküllerinden küçük bir aile üretti. Hepsi aynı temel zincir yapısını koruyor, ancak ömürleri ve eşleşmemiş elektronun kesin dağılımı halka yerine göre değişiyor; bu da kimyagerlerin basit organik modifikasyonlarla kararlılığı ince ayar yapabileceğini gösteriyor. Ekip ardından başı çeken bromlu bileşiğin nasıl reaksiyona girdiğini inceledi. Belirli koşullar altında dört‑nitrijen zinciri tek bir nitrijen birimine (N1) ve üç‑nitrijenli bir fragmana (N3) ayrılıyor. Ürün analizi ve hesaplamalardan elde edilen kanıtlar, bir yolak boyunca nitren radikal anyonu—karbon–hidrojen bağlarına girebilen son derece reaktif bir nitrijen türü—oluştuğunu gösteriyor. Bir aromatik aldehitle reaksiyona sokulduğunda sistem bir karbonil C–H bağını amid bağına dönüştürüyor; bu, bu kristal {N4}•−'ün daha karmaşık moleküller inşa etmek için saklanabilir, tezgâhüstü bir reaktif nitrijen kaynağı olarak hizmet edebileceğini gösteriyor.
Gelecek kimya için anlamı
Kırılgan dört‑nitrijenli radikal zinciri oda sıcaklığında kristal durumda ve kararlı tutan organik bir çerçeveye hapsetmekle, bu çalışma ulaşılması güç bir atmosferik merakı elle tutulur bir laboratuvar reaktifi haline getiriyor. Çalışma, dikkatle seçilmiş aromatik grupların yük ve spini yeterince delokalize ederek tipik N2 kaybının yol açtığı patlayıcı bozulmayı baskılayabildiğini, fakat tetiklendiğinde zincirin kontrollü şekilde parçalanmasına ve güçlü tek‑nitrijen birimlerinin açığa çıkmasına hâlâ izin verebildiğini gösteriyor. Uzman olmayanlar için ana mesaj şudur: kimyagerler nitrijenin en vahşi formlarından birini evcilleştirmeyi öğreniyor; bu, yeni yüksek enerjili maddelere ve nitrojen fragmanlarını önceki yöntemlere kıyasla çok daha fazla kontrolle ilaçlar ve diğer değerli ürünlere aktaran kullanışlı, katı reaktiflere kapı açıyor.
Atıf: Lister-Roberts, R., Galano, D., van IJzendoorn, B. et al. Crystalline nitrogen chain radical anions. Nat. Chem. 18, 686–694 (2026). https://doi.org/10.1038/s41557-025-02040-2
Anahtar kelimeler: nitrijen zincirleri, radikal anyonlar, yüksek enerjili maddeler, nitrin kimyası, organo‑nitrojen sentezi