Clear Sky Science · sv
Kristallina kedjor av kväveradikalanjoner
Varför instabila kvävokedjor spelar roll
Kvävgas utgör största delen av den luft vi andas, men i vissa extrema miljöer—som övre atmosfären eller i sprängämnens inre—kan kväve länkas ihop till energirika kedjor som lagrar enorm kemisk energi. Dessa kedjor faller vanligen isär nästan omedelbart under vardagliga förhållanden, så de har bara studerats flyktigt i rymdliknande plasman eller under extrema tryck. Den här artikeln rapporterar något som länge ansetts utom räckhåll: fasta, rumstempererade kristaller som säkert innehåller en skör fyra‑atomig kvävokedja, vilket öppnar ett nytt fönster för hur sådana högenergiska former av kväve beter sig och hur de en dag kan användas som kontrollerbara källor till reaktivt kväve i syntes och material.
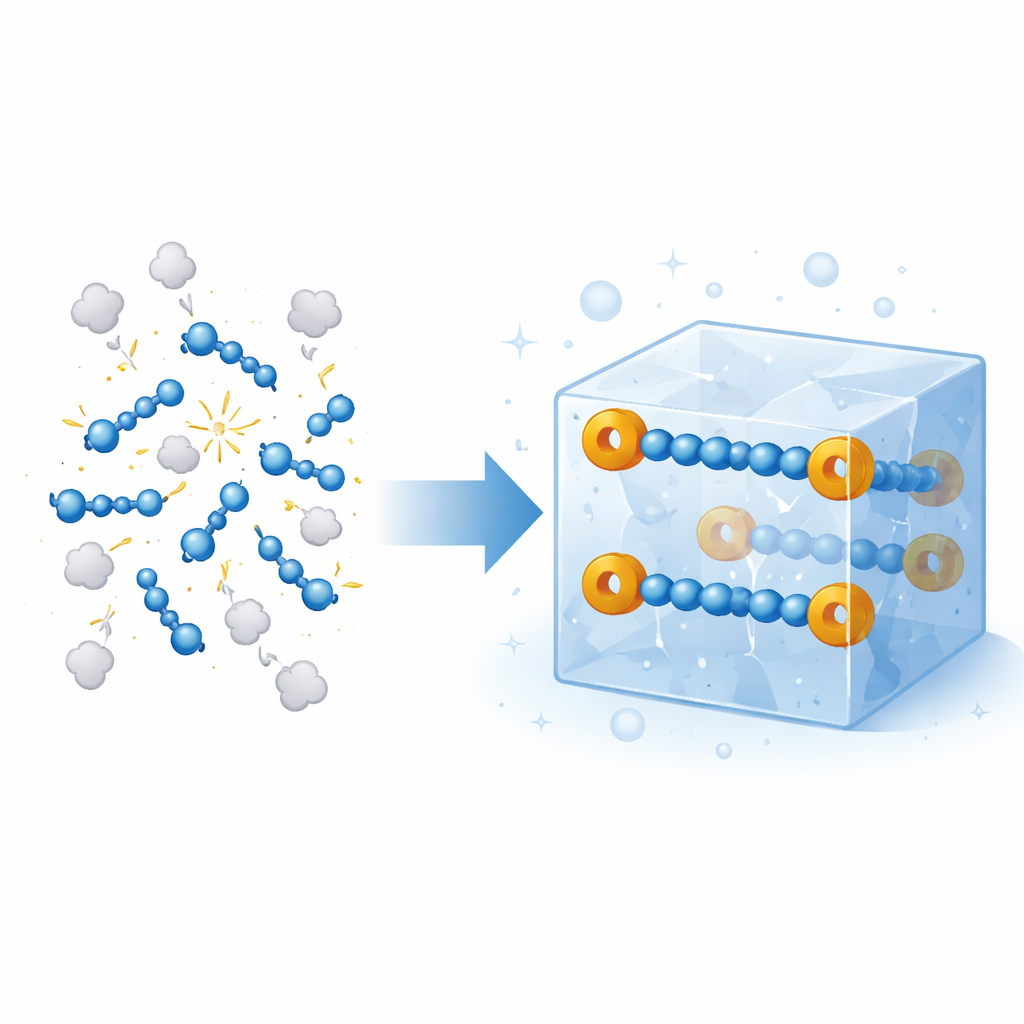
Från himmelkemin till bänkvätskan
Långa kvävokedjor med fler än tre kväveatomer är kända från jordens jonosfär och från den disiga atmosfären kring Saturnus måne Titan, där intensiv strålning och laddade partiklar kortvarigt binder ihop N2-molekyler till exotiska joner och radikaler. Liknande kvävokedjor har observerats inuti täta fasta ämnen som pressats under enorma tryck, och de är intressanta kandidater för avancerade drivmedel och sprängämnen eftersom de tenderar att ”hoppa tillbaka” till mycket stabil gasformigt N2 och frigöra energi. Problemet är att denna samma tendens gör dem extremt kortlivade och farliga under normala förhållanden. Kemister har försökt tämja dem genom att binda dem till metallatomer eller genom att begrava dem i skrymmande organiska grupper, men verkligt ”fria” kvävokedjor som bär en extra elektron—en radikalanjon—har förblivit för reaktiva för att isolera i flaskor.
Att bygga en stabil fyra‑kvävekedja
Författarna satte som mål att skapa en robust version av en fyra‑kväve radikalanjon, betecknad {N4}•−, utan att förlita sig på metallatomer för hållning. De började från enkla arylazider, vanliga laboratorieföreningar som redan innehåller ett tre‑kvävefragment. Genom att reducera dessa azider i närvaro av en kaliumpreparat och en kronliknande ligand som omsluter metalljonen gynnar de att två azidenheter kopplas samman huvud‑till‑huvud och bildar en linjär N–N–N–N‑kedja kapslad i vardera änden av en bromerad bensenring. Den resulterande anjonen, noterad som [(4‑BrC6H4)2N4]•−, kristalliserar som slående svarta nålar som är stabila i veckor i fast form om de hålls borta från luft. Röntgendiffraktion visar en nästan rak kedja av fyra kväveatomer med bindningslängder mellan typiska enkel‑ och dubbelbindningar, vilket indikerar att den extra elektronen är delokaliserad snarare än fångad på en enskild atom.
Att se var den oparade elektronen bor
För att förstå varför denna kedja är så ovanligt beständig kombinerade teamet flera spektroskopiska metoder med kvantkemi‑beräkningar. Elektronparamagnetisk resonans, en teknik som upptäcker oparade elektroner, visade att radikal‑karaktären är utspridd över hela molekylen men starkast vid de två terminala kvävena, som sitter intill de aromatiska ringarna. Beräknade spintäthetskartor bekräftar att största delen av den oparade elektronen befinner sig på N4-enheten, medan bensenringarna fungerar som ”säkerhetsventiler” som hjälper till att sprida ut och stabilisera elektronen, liknande hur de stabiliserar klassiska benzylic‑radikaler. Ultraviolet‑visibel spektroskopi och teoretiska analyser visar vidare ett nätverk av elektrondelande orbitaler som liknar det hos en enkel kolkedja, men byggd helt av kväveatomer.
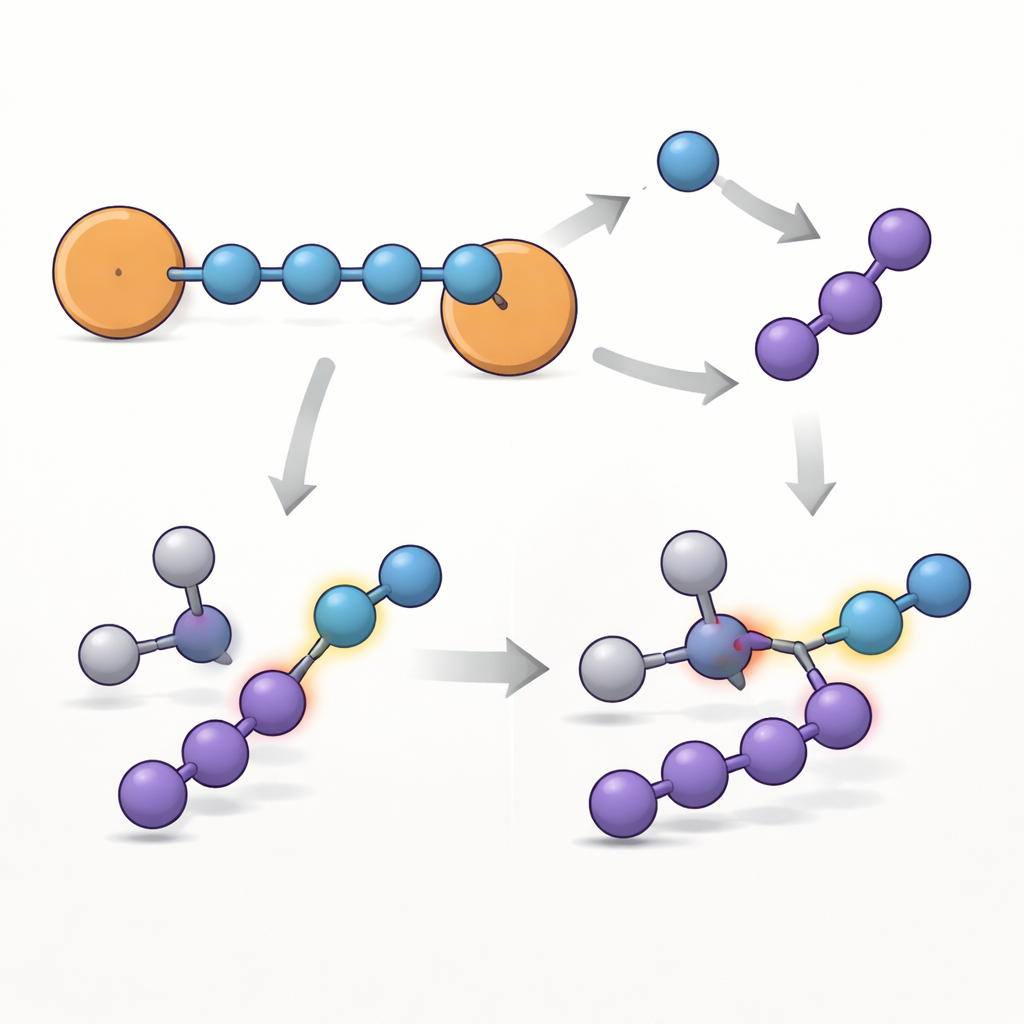
En familj av kedjor och en ny kvävekälla
Tillvägagångssättet visade sig vara generellt: genom att byta substituent på de aromatiska ringarna (fluor, klor, metyl eller osubstituerad fenyl) framställde författarna en liten familj av relaterade {N4}•−‑molekyler. Alla behåller samma grundläggande kedjestruktur, men deras livslängder och den exakta fördelningen av den oparade elektronen varierar med ringsubstituenten, vilket visar att kemister kan finjustera stabiliteten genom enkla organiska modifieringar. Teamet undersökte sedan hur huvudkomponenten med brom reagerar. Under vissa förhållanden bryts fyra‑kvävekedjan upp i en en‑kväveenhet (N1) och ett tre‑kvävefragment (N3). Bevis från produktanalys och beräkningar indikerar att en reaktionsväg ger en nitren‑radikalanjon—en mycket reaktiv kväveart som kan infogas i kol‑vätebindningar. När den reagerar med en aromatisk aldehyd omvandlar systemet en karbonyl C–H‑bindning till en amidbindning, vilket visar att denna kristallina {N4}•− kan fungera som en lagringsbar, bänkvänlig källa till reaktivt kväve för att bygga mer komplexa molekyler.
Vad detta betyder för framtidens kemi
Genom att fånga en ömtålig fyra‑kväve radikkedja i ett organiskt ramverk som förblir kristallint och stabilt vid rumstemperatur gör detta arbete en svårfångad atmosfärisk kuriositet till ett påtagligt laboratoriereagens. Studien visar att noggrant utvalda aromatiska grupper kan delokalisera laddning och spinn tillräckligt för att dämpa den vanliga explosiva förlusten av N2, samtidigt som kedjan fortfarande kan falla sönder på ett kontrollerat sätt när den triggas, och frigöra kraftfulla enkla kväveenheter. För icke‑specialister är huvudbudskapet att kemister lär sig att tämja en av kvävets vildaste former, vilket öppnar dörren för nya högenergiämnen och för bekväma, fasta reagenser som överför kvävfragment till läkemedel och andra värdefulla produkter med långt större kontroll än tidigare möjligt.
Citering: Lister-Roberts, R., Galano, D., van IJzendoorn, B. et al. Crystalline nitrogen chain radical anions. Nat. Chem. 18, 686–694 (2026). https://doi.org/10.1038/s41557-025-02040-2
Nyckelord: kvävokedjor, radikalanjoner, högenergiämnen, nitrenkemi, organo‑kvävesyntes