Clear Sky Science · it
Anioni radicali a catena di azoto cristallini
Perché contano le catene di azoto instabili
Il gas azoto costituisce la maggior parte dell’aria che respiriamo, ma in alcuni ambienti estremi — come l’alta atmosfera o il cuore degli esplosivi — l’azoto può legarsi formando catene energetiche che immagazzinano un’enorme energia chimica. Queste catene di solito si disgregano quasi istantaneamente in condizioni ordinarie, perciò sono state studiate principalmente in plasmi simili allo spazio o sotto pressioni schiaccianti. Questo articolo riporta qualcosa a lungo ritenuto irraggiungibile: cristalli solidi e stabili a temperatura ambiente che contengono in modo sicuro una fragile catena di azoto di quattro atomi, aprendo una nuova finestra sul comportamento di queste forme ad alta energia dell’azoto e su come potrebbero un giorno essere impiegate come sorgenti controllabili di azoto reattivo in sintesi e materiali. 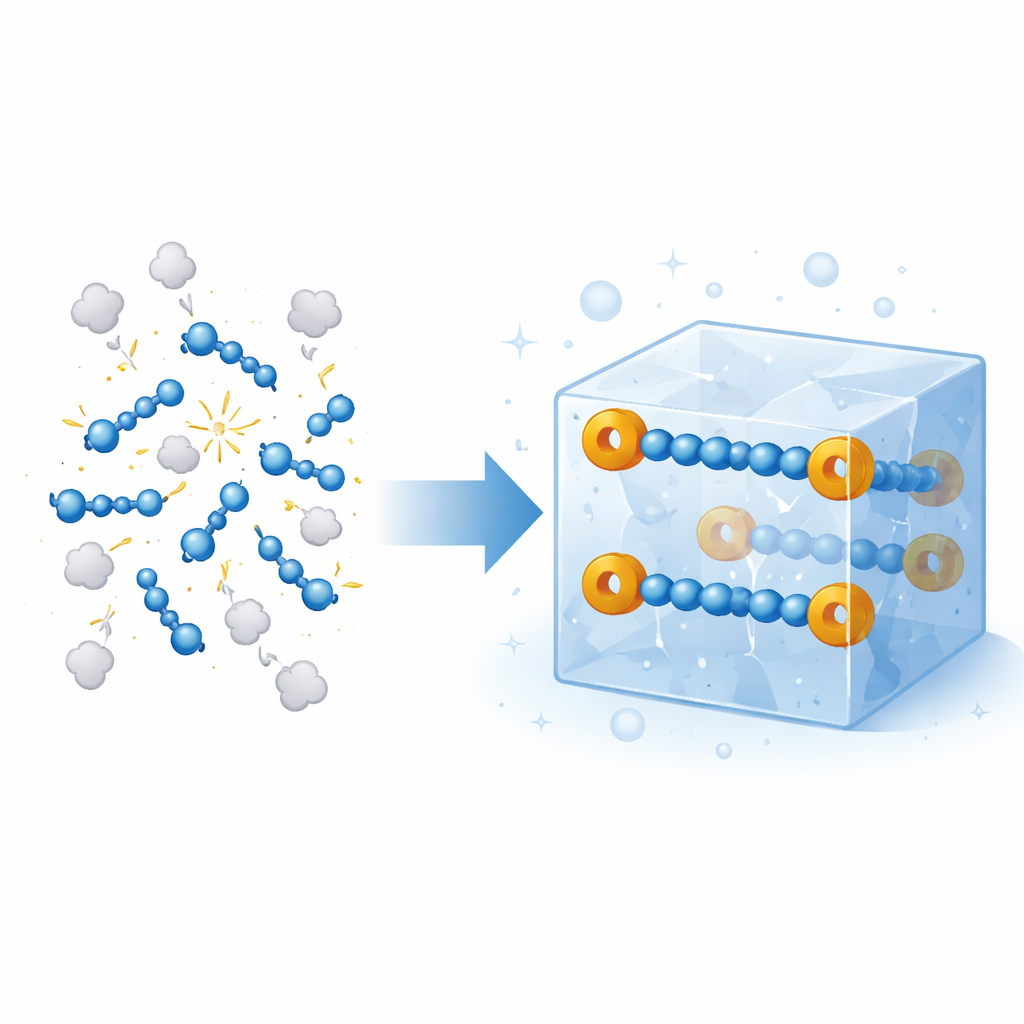
Dalla chimica del cielo al banco di laboratorio
Catene lunghe di azoto contenenti più di tre atomi sono note nell’ionosfera terrestre e nell’atmosfera velata di Titano, la luna di Saturno, dove radiazioni intense e particelle cariche ricuciono brevemente molecole di N2 in ioni e radicali esotici. Catene simili sono state individuate anche all’interno di solidi densi compressi a pressioni enormi, e sono candidate interessanti per propellenti e esplosivi avanzati perché tendono a “ritornare” allo stabile gas N2, rilasciando energia. Il problema è che questa stessa tendenza le rende estremamente di breve durata e pericolose in condizioni normali. I chimici hanno provato a domarle legandole ad atomi metallici o seppellendole in gruppi organici ingombranti, ma vere catene di azoto “libere” che portano un elettrone in più — un anione radicale — sono rimaste troppo reattive per essere isolate in bottiglia.
Costruire una catena di quattro azoti stabile
Gli autori si sono proposti di creare una versione robusta di un anione radicale a quattro azoti, scritto {N4}•−, senza affidarsi ad atomi metallici per stabilizzarlo. Sono partiti da azidi arilici semplici, composti da laboratorio comuni che già contengono un frammento di tre azoti. Riducendo questi azidi in presenza di una fonte di potassio e di un legante a corona che avvolge l’ione metallico, hanno favorito l’accoppiamento testa‑testa di due unità azidiche, formando una catena lineare N–N–N–N sormontata a ciascuna estremità da un anello di benzene bromurato. L’anione risultante, indicato come [(4‑BrC6H4)2N4]•−, cristallizza in aghi neri impressionanti che rimangono stabili per settimane nello stato solido se conservati lontano dall’aria. La diffrazione a raggi X mostra una catena quasi dritta di quattro atomi di azoto con lunghezze di legame tra quelle tipiche di legami semplici e doppi, indicando che l’elettrone in più è condiviso (delocalizzato) piuttosto che localizzato su un singolo atomo.
Localizzare dove vive l’elettrone spaiato
Per capire perché questa catena è così insolitamente persistente, il gruppo ha combinato più metodi spettroscopici con calcoli quantochimici. La risonanza paramagnetica elettronica, una tecnica che rileva elettroni spaiati, ha rivelato che il carattere radicale è distribuito sull’intera molecola ma è più intenso sui due azoti terminali, che si trovano accanto agli anelli aromatici. Mappe di densità di spin calcolate confermano che la maggior parte dell’elettrone spaiato risiede sull’unità N4, con gli anelli benzenici che agiscono come “valvole di sicurezza” che aiutano a dispersere e stabilizzare l’elettrone, in modo analogo a quanto avviene per i radicali benzylici classici. La spettroscopia ultravioletto‑visibile e le analisi teoriche mostrano inoltre una rete di orbitali condivisi dagli elettroni che assomiglia a quella di una semplice catena carboniosa, ma costruita interamente da atomi di azoto. 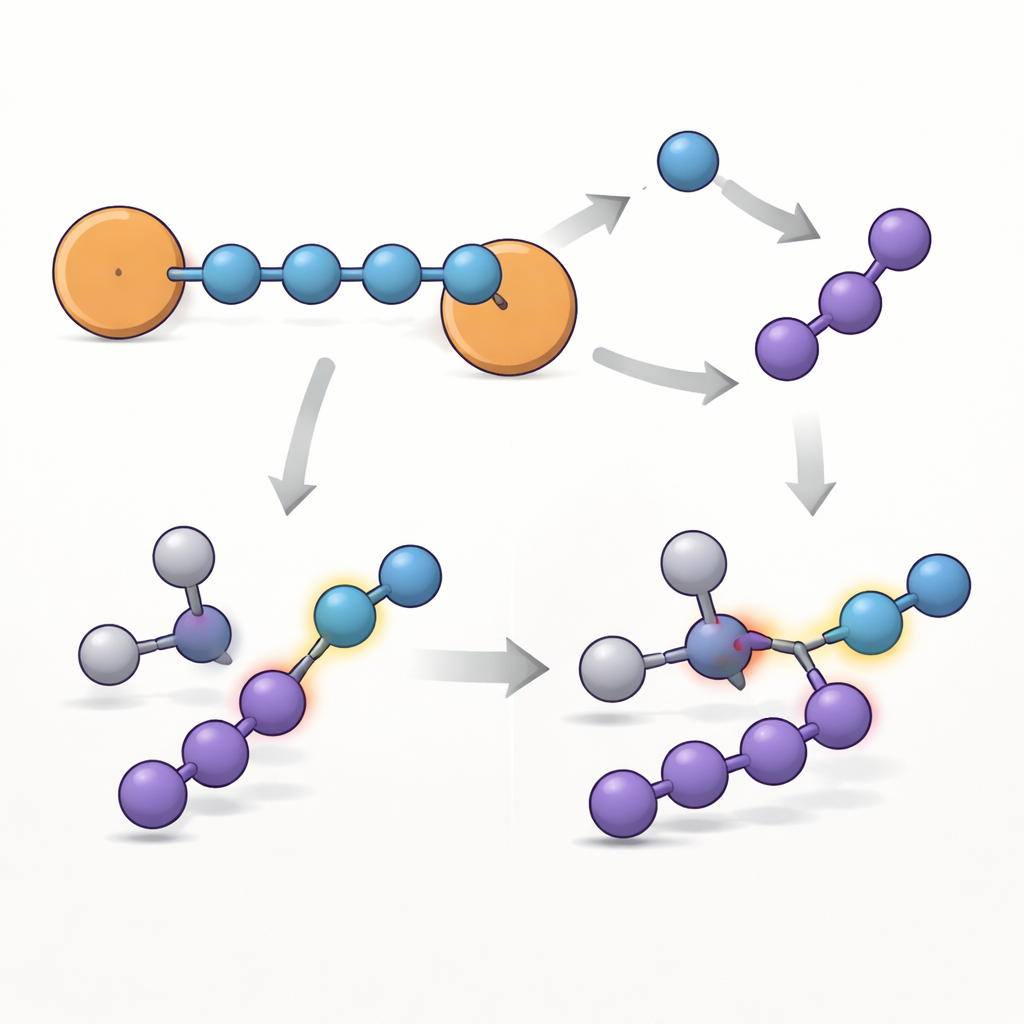
Una famiglia di catene e una nuova sorgente di azoto
L’approccio si è rivelato generale: variando il sostituente sugli anelli aromatici (fluoro, cloro, metile o fenile non sostituito), gli autori hanno generato una piccola famiglia di molecole correlate {N4}•−. Tutte mantengono la stessa struttura di base della catena, ma la loro durata e la distribuzione precisa dell’elettrone spaiato variano con il sostituente dell’anello, mostrando che i chimici possono perfezionare la stabilità mediante semplici modifiche organiche. Il gruppo ha quindi esplorato come reagisce il composto bromurato di punta. In certe condizioni la catena a quattro azoti si rompe in un’unità a singolo azoto (N1) e un frammento a tre azoti (N3). Evidenze dall’analisi dei prodotti e dai calcoli indicano che una via produce un anione radicale nitrenico — una specie di azoto altamente reattiva capace di inserirsi in legami carbonio–idrogeno. Quando reagisce con un’aldeide aromatica, il sistema converte un legame C–H carbonilico in un legame ammidico, dimostrando che questo {N4}•− cristallino può servire come sorgente stoccabile e da banco di azoto reattivo per costruire molecole più complesse.
Cosa significa per la chimica futura
Intrappolando una delicata catena radicale di quattro azoti in un quadro organico che rimane cristallino e stabile a temperatura ambiente, questo lavoro trasforma una curiosità atmosferica elusiva in un reagente di laboratorio tangibile. Lo studio mostra che gruppi aromatici scelti con cura possono delocalizzare carica e spin a sufficienza per sopprimere la consueta perdita esplosiva di N2, pur permettendo alla catena di disfarsi in modo controllato quando attivata, rilasciando potenti unità mononitrogeno. Per i non specialisti, il messaggio chiave è che i chimici stanno imparando a addomesticare una delle forme più selvagge dell’azoto, aprendo la strada a nuovi materiali ad alta energia e a reagenti solidi e pratici che trasferiscono frammenti di azoto in prodotti farmaceutici e altri prodotti di valore con molto maggiore controllo rispetto a quanto fosse possibile in precedenza.
Citazione: Lister-Roberts, R., Galano, D., van IJzendoorn, B. et al. Crystalline nitrogen chain radical anions. Nat. Chem. 18, 686–694 (2026). https://doi.org/10.1038/s41557-025-02040-2
Parole chiave: catene di azoto, anioni radicali, materiali ad alta energia, chimica delle nitreni, sintesi organo‑azotata