Clear Sky Science · pt
Anion-radicais cristalinos de cadeias de nitrogênio
Por que cadeias de nitrogênio instáveis importam
O gás nitrogênio compõe a maior parte do ar que respiramos, mas em certos ambientes extremos — como a alta atmosfera ou o interior de explosivos — o nitrogênio pode ligar-se em cadeias energéticas que armazenam enorme energia química. Essas cadeias costumam se decompor quase instantaneamente em condições cotidianas, por isso têm sido estudadas apenas de forma passageira em plasmas semelhantes aos do espaço ou sob pressões esmagadoras. Este artigo relata algo considerado por muito tempo inalcançável: cristais sólidos estáveis à temperatura ambiente que contêm com segurança uma frágil cadeia de quatro átomos de nitrogênio, abrindo uma nova janela sobre como essas formas de nitrogênio de alta energia se comportam e como elas poderão um dia ser usadas como fontes controláveis de nitrogênio reativo em síntese e em materiais. 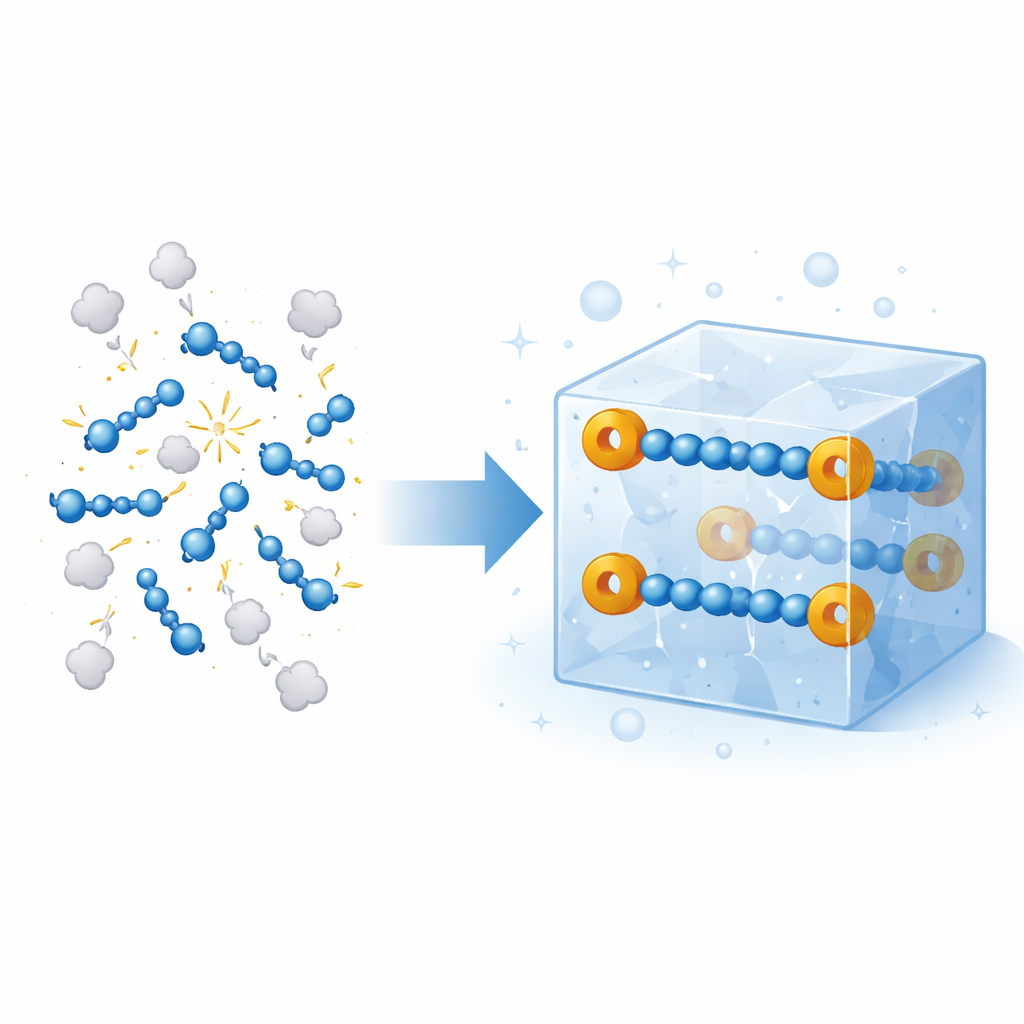
Da química do céu ao banco de laboratório
Cadeias longas de nitrogênio contendo mais de três átomos são conhecidas na ionosfera da Terra e na atmosfera enevoada da lua Titã, de Saturno, onde radiação intensa e partículas carregadas tecem brevemente moléculas de N2 em íons e radicais exóticos. Cadeias semelhantes foram observadas dentro de sólidos densos comprimidos a pressões enormes, e são candidatas atraentes para propelentes e explosivos avançados porque tendem a “recolher‑se” a N2 muito estável, liberando energia. O problema é que essa mesma tendência as torna extremamente de curta duração e perigosas em condições normais. Químicos tentaram domesticá‑las ligando‑as a átomos metálicos ou enterrando‑as dentro de grupos orgânicos volumosos, mas verdadeiras cadeias de nitrogênio “livres” carregando um elétron extra — um ânion‑radical — permaneceram demasiado reativas para serem isoladas em frasco.
Construindo uma cadeia estável de quatro nitrogênios
Os autores propuseram criar uma versão robusta de um ânion‑radical de quatro nitrogênios, escrito {N4}•−, sem recorrer a átomos metálicos para mantê‑lo no lugar. Eles partiram de azidas arílicas simples, compostos comuns de laboratório que já contêm um fragmento de três nitrogênios. Ao reduzir essas azidas na presença de uma fonte de potássio e de um ligante em forma de coroa que envolve o íon metálico, incentivam duas unidades de azida a acoplar cabeça a cabeça, formando uma cadeia linear N–N–N–N tampada em cada extremidade por um anel benzênico bromado. O ânion resultante, anotado como [(4‑BrC6H4)2N4]•−, cristaliza em agulhas pretas marcantes que são estáveis por semanas no estado sólido se mantidas afastadas do ar. Difração de raios X mostra uma cadeia quase retilínea de quatro átomos de nitrogênio com comprimentos de ligação entre típicos de ligações simples e duplas, indicando que o elétron extra está compartilhado (delocalizado) em vez de preso a um único átomo.
Vendo onde vive o elétron desemparelhado
Para entender por que essa cadeia é tão persistentemente incomum, a equipe combinou vários métodos espectroscópicos com cálculos quântico‑químicos. Ressonância paramagnética eletrônica, uma técnica que detecta elétrons desemparelhados, revelou que o caráter radical está espalhado por toda a molécula, mas é mais forte nos dois nitrogênios terminais, que ficam ao lado dos anéis aromáticos. Mapas calculados de densidade de spin confirmam que a maior parte do elétron desemparelhado reside na unidade N4, com os anéis benzênicos atuando como “válvulas de segurança” que ajudam a espalhar e estabilizar o elétron, de forma semelhante à estabilização de radicais benílicos clássicos. Espectroscopia ultravioleta–visível e análises teóricas mostram ainda uma rede de orbitais de compartilhamento eletrônico que se assemelha à de uma cadeia simples de carbono, porém construída inteiramente de átomos de nitrogênio. 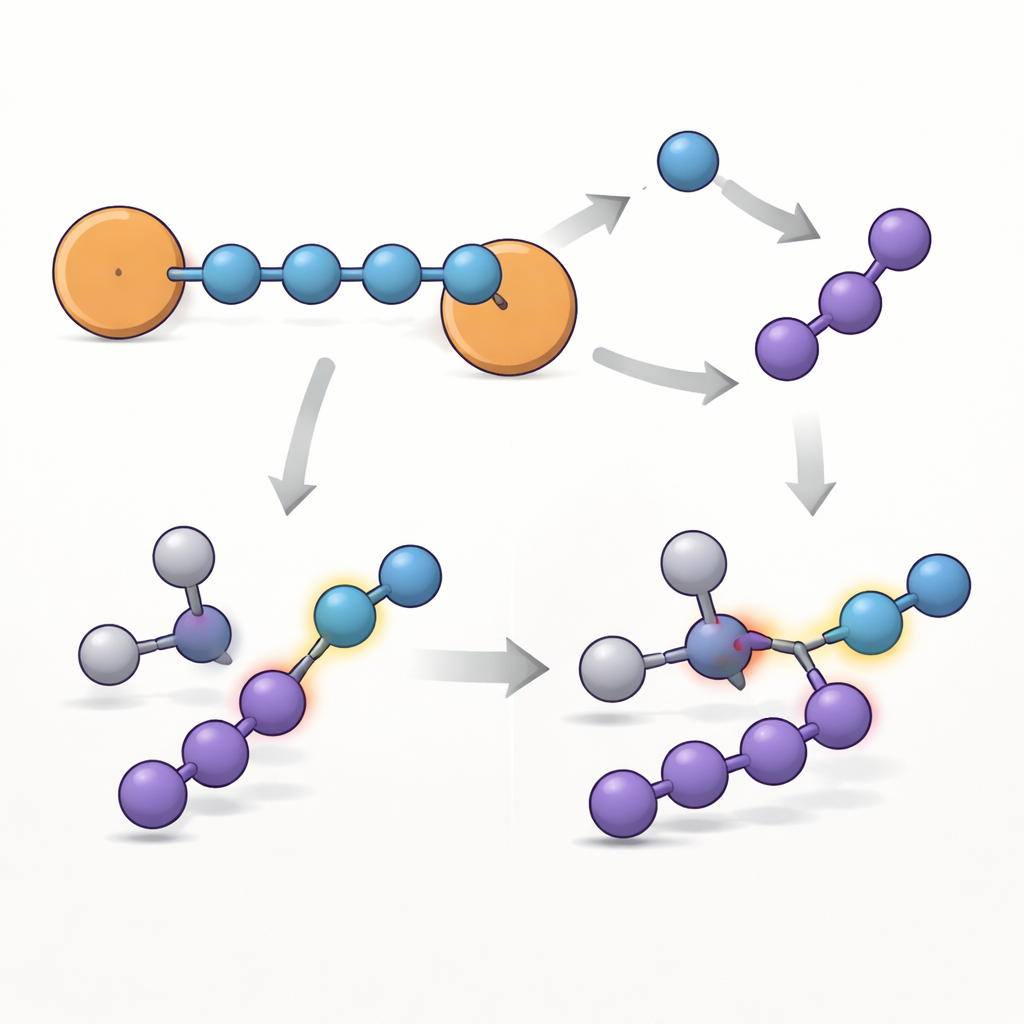
Uma família de cadeias e uma nova fonte de nitrogênio
A abordagem provou ser geral: ao variar o substituinte nos anéis aromáticos (fluoro, cloro, metil ou fenil não substituído), os autores geraram uma pequena família de moléculas relacionadas {N4}•−. Todas mantêm a mesma estrutura básica de cadeia, mas suas vidas‑úteis e a distribuição exata do elétron desemparelhado variam com o substituinte do anel, mostrando que químicos podem ajustar finamente a estabilidade por modificações orgânicas simples. A equipe então explorou como o composto bromado emblemático reage. Em certas condições, a cadeia de quatro nitrogênios se quebra em uma unidade de nitrogênio simples (N1) e um fragmento de três nitrogênios (N3). Evidências da análise dos produtos e de cálculos indicam que uma via produz um ânion‑radical de nitreno — uma espécie de nitrogênio altamente reativa capaz de inserir‑se em ligações carbono–hidrogênio. Quando reagido com um aldeído aromático, o sistema converte uma ligação C–H carbonílica em uma ligação amida, demonstrando que esse {N4}•− cristalino pode servir como fonte armazenável, de bancada, de nitrogênio reativo para construir moléculas mais complexas.
O que isso significa para a química futura
Ao aprisionar uma delicada cadeia radical de quatro nitrogênios em uma estrutura orgânica que permanece cristalina e estável à temperatura ambiente, este trabalho transforma uma curiosidade atmosférica elusiva em um reagente de laboratório tangível. O estudo mostra que grupos aromáticos escolhidos com cuidado podem delocalizar carga e spin o bastante para suprimir a perda explosiva habitual de N2, mas ainda permitir que a cadeia se desfaça de forma controlada quando acionada, liberando potentes unidades de nitrogênio simples. Para não especialistas, a mensagem principal é que químicos estão aprendendo a domesticar uma das formas mais instáveis do nitrogênio, abrindo a porta para novos materiais de alta energia e para reagentes sólidos convenientes que transferem fragmentos de nitrogênio para produtos farmacêuticos e outros produtos valiosos com muito mais controle do que era anteriormente possível.
Citação: Lister-Roberts, R., Galano, D., van IJzendoorn, B. et al. Crystalline nitrogen chain radical anions. Nat. Chem. 18, 686–694 (2026). https://doi.org/10.1038/s41557-025-02040-2
Palavras-chave: cadeias de nitrogênio, ânions-radicais, materiais de alta energia, química de nitrenos, síntese de organo‑nitrogenados