Clear Sky Science · nl
Kristallijne radicaalanionen van stikstofketens
Waarom instabiele stikstofketens ertoe doen
Stikstofgas vormt het grootste deel van de lucht die we inademen, maar in bepaalde extreme omgevingen—zoals de bovenste atmosfeer of de kern van springstoffen—kan stikstof binden tot energierijke ketens die enorme chemische energie opslaan. Deze ketens vallen onder alledaagse omstandigheden meestal vrijwel onmiddellijk uit elkaar, daarom zijn ze tot nu toe vooral vluchtig bestudeerd in ruimte‑achtige plasma’s of onder enorme drukken. Dit artikel rapporteert iets wat lang als onbereikbaar werd beschouwd: vaste, kamertemperatuurkristallen die op veilige wijze een kwetsbare vier‑atoom stikstofketen bevatten, en daarmee een nieuw venster openen op het gedrag van zulke hoogenergetische vormen van stikstof en hoe ze mogelijk ooit als beheersbare bronnen van reactieve stikstof in synthese en materialen kunnen worden ingezet. 
Van hemelchemie naar het lab
Lange stikstofketens met meer dan drie stikstofatomen zijn bekend uit de ionosfeer van de aarde en uit de nevelige atmosfeer van Saturnus’ maan Titan, waar intense straling en geladen deeltjes tijdelijk N2-moleculen aaneenrijgen tot exotische ionen en radicalen. Vergelijkbare stikstofketens zijn waargenomen in dicht samengeperste vastestoffen bij enorme drukken, en ze zijn aantrekkelijke kandidaten voor geavanceerde drijfladingen en springstoffen omdat ze de neiging hebben terug te keren naar zeer stabiel N2-gas en daarbij energie vrij te geven. Het probleem is dat diezelfde eigenschap ze onder normale omstandigheden extreem kortlevend en gevaarlijk maakt. Chemici hebben geprobeerd ze te temmen door ze aan metaalatomen te binden of door ze in omvangrijke organische groepen te verbergen, maar echt “vrije” stikstofketens met een extra elektron—een radicaalanion—bleven te reactief om in een fles te isoleren.
Een stabiele vier‑stikstofketen opbouwen
De auteurs wilden een robuuste versie van een vier‑stikstof radicaalanion creëren, genoteerd als {N4}•−, zonder te vertrouwen op metaalatomen om het op zijn plaats te houden. Ze begonnen met eenvoudige arylaziden, veelgebruikte laboratoriumverbindingen die al een fragment met drie stikstoffen bevatten. Door deze aziden te reduceren in aanwezigheid van een kaliumbron en een kroonsgewijze ligand die het metaalion omsluit, bevorderden ze dat twee azide‑eenheden kop‑aan‑kop koppelen en zo een lineaire N–N–N–N‑keten vormen die aan beide uiteinden is afgedekt met een gebromeerde benzeenring. Het resulterende anion, aangeduid als [(4‑BrC6H4)2N4]•−, kristalliseert als opvallende zwarte naalden die wekenlang stabiel blijven in de vaste fase mits ze van lucht worden weggelopen. Röntgendiffractie toont een nagenoeg rechte keten van vier stikstofatomen met bindingslengten tussen typische enkel‑ en dubbele bindingen, wat aangeeft dat het extra elektron gedeeld (gedelokaliseerd) is in plaats van opgesloten op één atoom.
Zien waar het ongepaarde elektron zit
Om te begrijpen waarom deze keten zo uitzonderlijk persistent is, combineerde het team meerdere spectroscopische methoden met kwantumchemische berekeningen. Elektronenparamagnetische resonantie, een techniek die ongepaarde elektronen detecteert, toonde dat het radicaal‑karakter over het hele molecuul is verdeeld maar het sterkst is bij de twee terminale stikstoffen, die naast de aromatische ringen zitten. Berekende spin‑dichtheidskaarten bevestigen dat het merendeel van het ongepaarde elektron op de N4‑eenheid rust, waarbij de benzeenringen fungeren als “veiligheidskleppen” die helpen het elektron te verspreiden en te stabiliseren, vergelijkbaar met hoe ze klassieke benzylic‑radicalen stabiliseren. Ultraviolet‑zichtbaar‑spectroscopie en theoretische analyses laten bovendien een netwerk van elektrondeeldende orbitalen zien dat doet denken aan dat van een eenvoudige koolstofketen, maar volledig uit stikstofatomen bestaat. 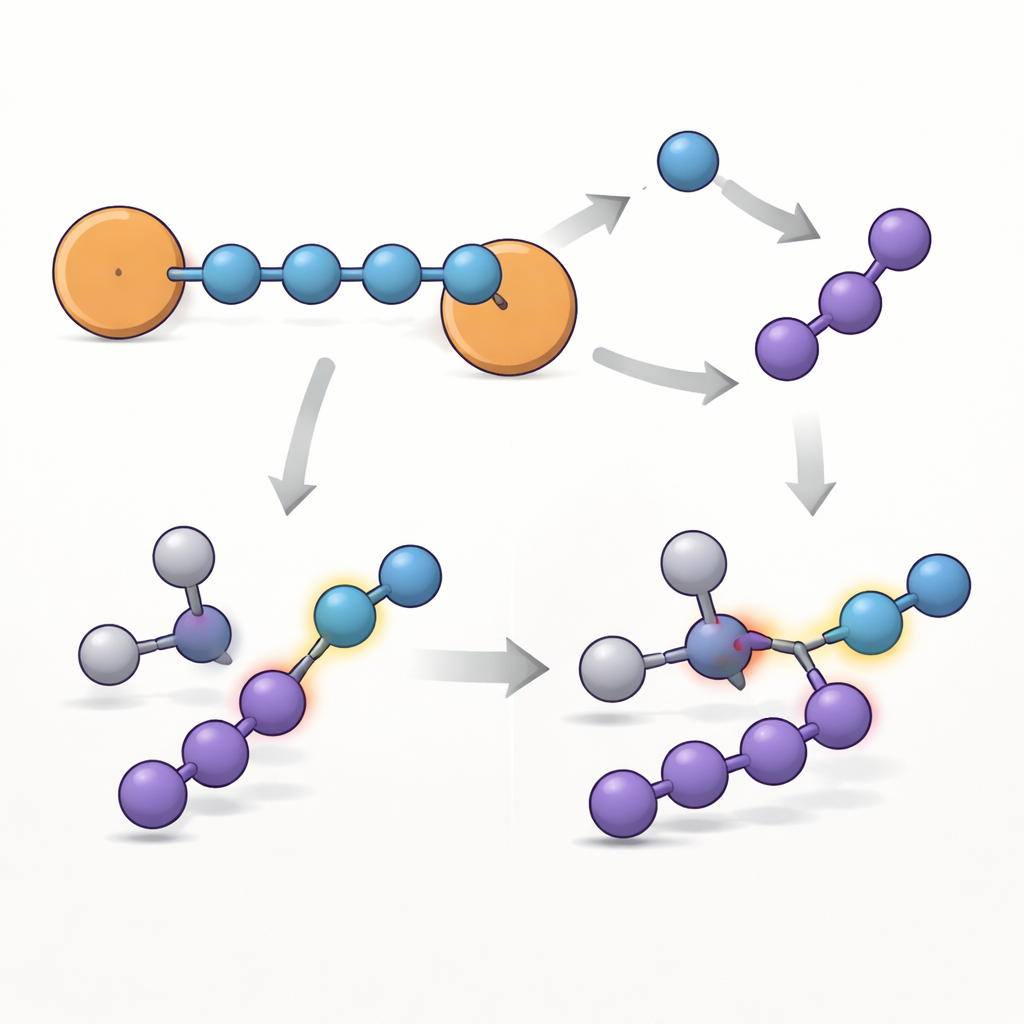
Een familie van ketens en een nieuwe stikstofbron
De aanpak bleek algemeen toepasbaar: door het substituent op de aromatische ringen te variëren (fluor, chloor, methyl of onge substituted fenyl) genereerden de auteurs een kleine familie verwante {N4}•−‑moleculen. Allemaal behouden ze dezelfde basis ketenstructuur, maar hun levensduur en de exacte verdeling van het ongepaarde elektron variëren met het ring‑substituent, wat aantoont dat chemici de stabiliteit eenvoudig kunnen afstemmen door organische modificaties. Het team onderzocht vervolgens hoe het vlaggenschip‑bromide reageert. Onder bepaalde omstandigheden splitst de vier‑stikstofketen zich in een een‑stikstofeenheid (N1) en een drie‑stikstoffragment (N3). Bewijs uit productanalyse en berekeningen wijst erop dat één reactieweg een nitreenderadicaalanion oplevert—een zeer reactieve stikstofsoort die in staat is in koolstof‑waterstofbindingen in te voegen. Bij reactie met een aromatisch aldehyde zet het systeem een carbonyl C–H‑binding om in een amidelink, wat demonstreert dat dit kristallijne {N4}•− kan dienen als een opslaarbare, op het aanrecht bruikbare bron van reactieve stikstof voor de opbouw van complexere moleculen.
Wat dit betekent voor toekomstige chemie
Door een kwetsbare vier‑stikstof radicaalketen te vangen in een organisch raamwerk dat kristallijn blijft en bij kamertemperatuur stabiel is, verandert dit werk een ongrijpbare atmosferische curiositeit in een tastbaar laboratoriumreagens. De studie toont dat zorgvuldig gekozen aromatische groepen lading en spin voldoende kunnen delokaliseren om het gebruikelijke explosieve verlies van N2 te onderdrukken, maar toch toe te laten dat de keten gecontroleerd uiteenvalt wanneer ze wordt geactiveerd, waarbij krachtige enkel‑stikstofeenheden vrijkomen. Voor niet‑specialisten is de kernboodschap dat chemici leren een van de wildste vormen van stikstof te temmen, wat de deur opent naar nieuwe hoogenergetische materialen en naar handige, vaste reagentia die stikstoffragmenten in farmaceutische middelen en andere waardevolle producten kunnen inbrengen met veel grotere controle dan voorheen mogelijk was.
Bronvermelding: Lister-Roberts, R., Galano, D., van IJzendoorn, B. et al. Crystalline nitrogen chain radical anions. Nat. Chem. 18, 686–694 (2026). https://doi.org/10.1038/s41557-025-02040-2
Trefwoorden: stikstofketens, radicaalanionen, hoogenergetische materialen, nitreenchimie, organo‑stikstofsynthese