Clear Sky Science · es
Aniones radicales cristalinos de cadenas de nitrógeno
Por qué importan las cadenas de nitrógeno inestables
El nitrógeno gaseoso constituye la mayor parte del aire que respiramos, pero en ciertos ambientes extremos —como la alta atmósfera o el interior de los explosivos— el nitrógeno puede enlazarse formando cadenas energéticas que almacenan una gran cantidad de energía química. Estas cadenas suelen desintegrarse casi instantáneamente en condiciones ordinarias, por lo que hasta ahora solo se han observado momentáneamente en plasmas similares al espacio o bajo presiones enormes. Este artículo informa de algo que durante mucho tiempo se consideró inalcanzable: cristales sólidos, estables a temperatura ambiente, que contienen de forma segura una frágil cadena de cuatro átomos de nitrógeno, abriendo una nueva ventana sobre cómo se comportan estas formas de nitrógeno de alta energía y cómo podrían, algún día, usarse como fuentes controlables de nitrógeno reactivo en síntesis y materiales. 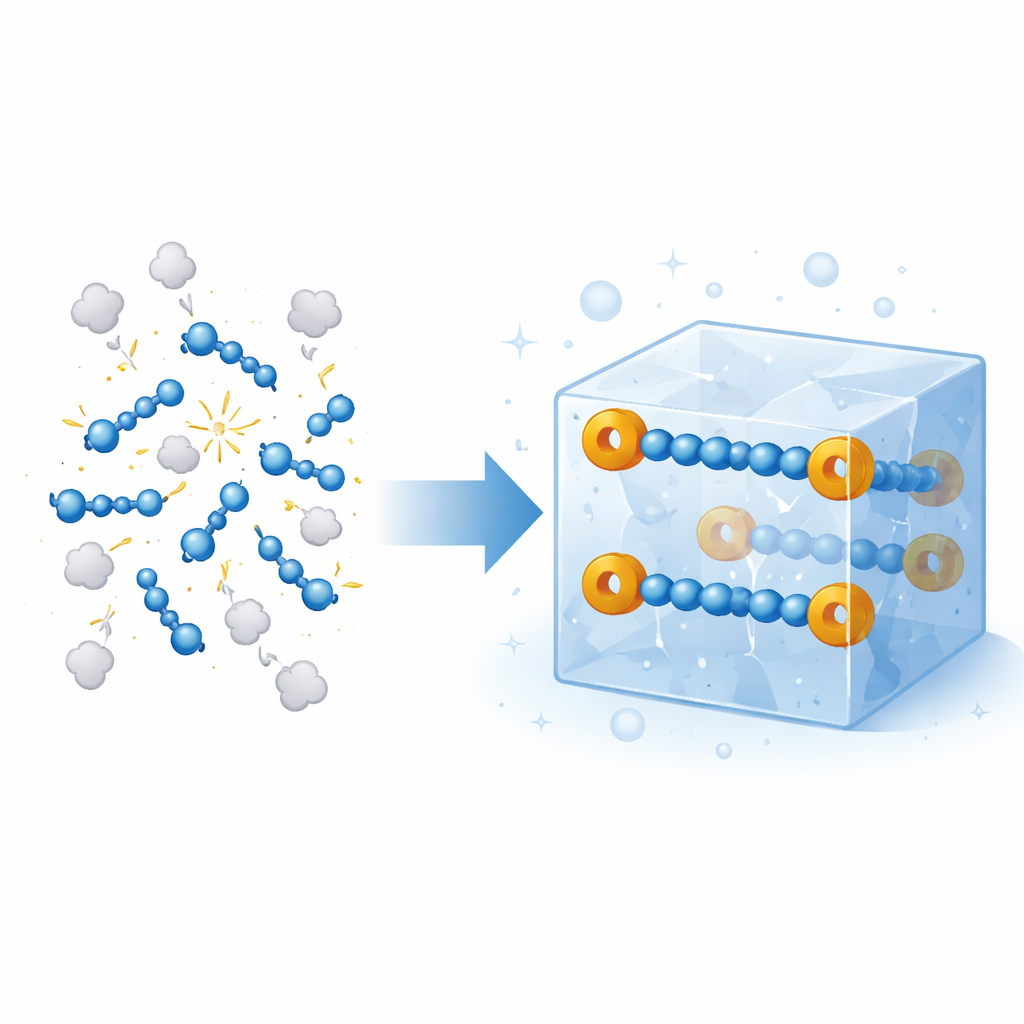
De la química atmosférica al banco de laboratorio
Se conocen largas cadenas de nitrógeno con más de tres átomos en la ionosfera terrestre y en la atmósfera brumosa de Titán, la luna de Saturno, donde la intensa radiación y las partículas cargadas unen brevemente moléculas de N2 en iones y radicales exóticos. Cadenas de nitrógeno similares se han detectado dentro de sólidos densos comprimidos a presiones enormes, y son candidatas atractivas para propelentes y explosivos avanzados porque tienden a «retraerse» hacia el gas muy estable N2, liberando energía. El problema es que esa misma tendencia las hace extremadamente de corta vida y peligrosas en condiciones normales. Los químicos han intentado controlarlas uniéndolas a átomos metálicos o enterrándolas dentro de grupos orgánicos voluminosos, pero las cadenas de nitrógeno verdaderamente “libres” que llevan un electrón extra —un anión radical— han seguido siendo demasiado reactivas para aislarse en un frasco.
Construir una cadena de cuatro nitrógenos estable
Los autores se propusieron crear una versión robusta de un anión radical de cuatro nitrógenos, escrito {N4}•−, sin depender de átomos metálicos para sostenerlo. Partieron de aril azidas sencillas, compuestos de laboratorio comunes que ya contienen un fragmento de tres nitrógenos. Al reducir estas azidas en presencia de una fuente de potasio y de un ligando tipo corona que envuelve el ion metálico, favorecen que dos unidades de azida se acoplen cabeza con cabeza, formando una cadena lineal N–N–N–N rematada en cada extremo por un anillo bencénico bromado. El anión resultante, anotado como [(4‑BrC6H4)2N4]•−, cristaliza en llamativas agujas negras que son estables semanas en estado sólido si se mantienen alejadas del aire. La difracción de rayos X muestra una cadena casi recta de cuatro átomos de nitrógeno con longitudes de enlace entre las típicas de enlaces simples y dobles, lo que indica que el electrón extra está compartido (deslocalizado) en lugar de estar atrapado en un solo átomo.
Ver dónde vive el electrón desapareado
Para entender por qué esta cadena es tan inusualmente persistente, el equipo combinó varios métodos espectroscópicos con cálculos cuántico‑químicos. La resonancia paramagnética electrónica, una técnica que detecta electrones desapareados, reveló que el carácter radical está repartido por toda la molécula pero es más fuerte en los dos nitrógenos terminales, que se sitúan junto a los anillos aromáticos. Los mapas de densidad de espín calculados confirman que la mayor parte del electrón desapareado reside en la unidad N4, con los anillos bencénicos actuando como «válvulas de seguridad» que ayudan a difuminar y estabilizar el electrón, similar a cómo estabilizan los radicales benzílicos clásicos. La espectroscopía ultravioleta‑visible y los análisis teóricos muestran además una red de orbitales compartidos que se asemeja a la de una cadena simple de carbono, pero construida enteramente con átomos de nitrógeno. 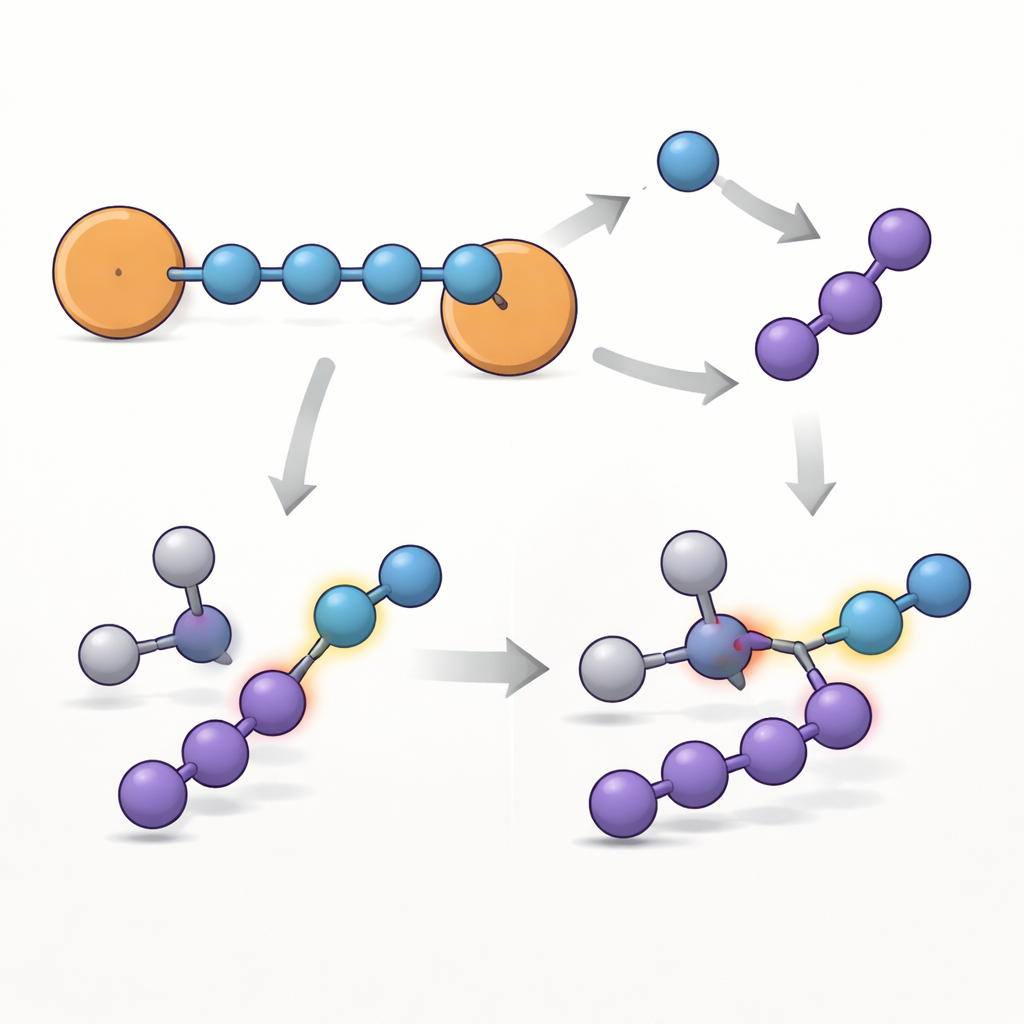
Una familia de cadenas y una nueva fuente de nitrógeno
El enfoque resultó ser general: al cambiar el substituyente en los anillos aromáticos (fluoro, cloro, metilo o fenilo no sustituido), los autores generaron una pequeña familia de moléculas relacionadas {N4}•−. Todas conservan la misma estructura de cadena básica, pero sus vidas medias y la distribución exacta del electrón desapareado varían con el substituyente del anillo, mostrando que los químicos pueden afinar la estabilidad mediante modificaciones orgánicas sencillas. El equipo exploró entonces cómo reacciona el compuesto bromado emblemático. En ciertas condiciones, la cadena de cuatro nitrógenos se rompe en una unidad de un nitrógeno (N1) y un fragmento de tres nitrógenos (N3). La evidencia del análisis de productos y los cálculos indica que una vía produce un anión radical nitreno —una especie de nitrógeno altamente reactiva capaz de insertarse en enlaces carbono‑hidrógeno. Al reaccionar con un aldehído aromático, el sistema convierte un enlace C–H carbonílico en un enlace amida, demostrando que este {N4}•− cristalino puede servir como fuente almacenable y de sobremesa de nitrógeno reactivo para construir moléculas más complejas.
Qué significa esto para la química futura
Al atrapar una delicada cadena radical de cuatro nitrógenos en un entramado orgánico que permanece cristalino y estable a temperatura ambiente, este trabajo convierte una curiosidad atmosférica esquiva en un reactivo tangible de laboratorio. El estudio muestra que grupos aromáticos cuidadosamente elegidos pueden deslocalizar carga y espín lo suficiente como para suprimir la pérdida explosiva habitual de N2, pero aún permitir que la cadena se desintegre de forma controlada cuando se activa, liberando potentes unidades de nitrógeno monoméricas. Para los no especialistas, el mensaje clave es que los químicos están aprendiendo a domesticar una de las formas más salvajes del nitrógeno, abriendo la puerta a nuevos materiales de alta energía y a reactivos sólidos convenientes que transfieren fragmentos de nitrógeno a productos farmacéuticos y otros compuestos valiosos con mucho más control del que se lograba antes.
Cita: Lister-Roberts, R., Galano, D., van IJzendoorn, B. et al. Crystalline nitrogen chain radical anions. Nat. Chem. 18, 686–694 (2026). https://doi.org/10.1038/s41557-025-02040-2
Palabras clave: cadenas de nitrógeno, aniones radicales, materiales de alta energía, química de nitrenos, síntesis orgánico‑nitrogenada