Clear Sky Science · ru
Кристаллические радикальные анионы нитrogenовых цепочек
Почему нестабильные нитrogenовые цепочки важны
Азот в газообразной форме составляет большую часть воздуха, которым мы дышим, но в некоторых экстремальных средах — например в верхних слоях атмосферы или в сердцах взрывчатых веществ — атомы азота могут соединяться в энергетические цепочки, сохраняющие огромную химическую энергию. Такие цепочки обычно распадаются практически мгновенно при обычных условиях, поэтому их изучали преимущественно в плазмах, похожих на космические, или при огромных давлениях. В этой статье сообщается о том, что долго считалось недостижимым: твердые кристаллы при комнатной температуре, безопасно содержащие хрупкую четырехатомную нитrogenовую цепочку, что открывает новое окно в изучение поведения таких высокоэнергетических форм азота и их потенциального использования как управляемых источников реактивного азота в синтезе и материалах. 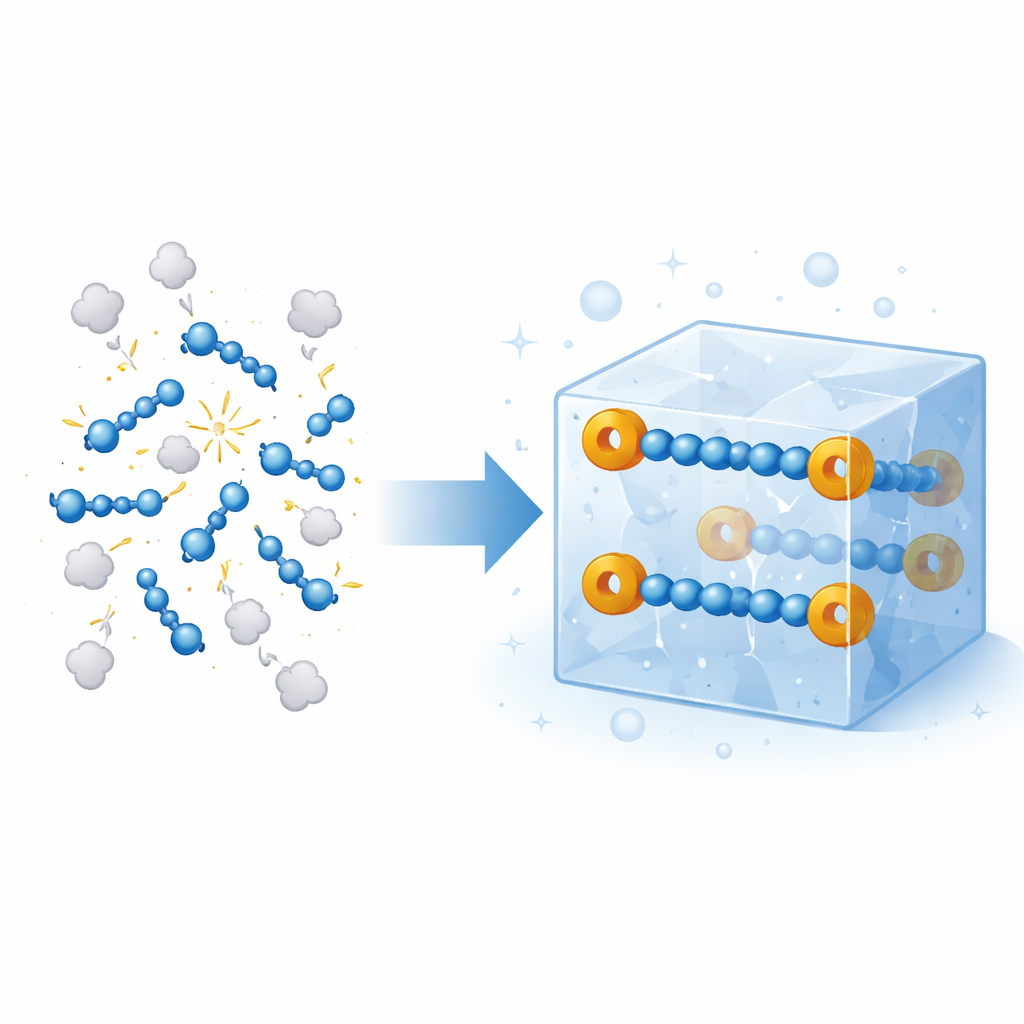
От небесной химии к лабораторному столу
Длинные нитrogenовые цепочки, содержащие более трех атомов азота, известны из ионосферы Земли и из дымчатой атмосферы Титана, спутника Сатурна, где интенсивное излучение и заряженные частицы кратковременно связывают молекулы N2 в экзотические ионы и радикалы. Подобные цепочки обнаруживали и внутри плотных твердых тел, сжатыых при огромных давлениях, и они рассматриваются как перспективные кандидаты для передовых топлива и взрывчатых веществ, поскольку склонны «возвращаться» к очень стабильному газу N2, выделяя энергию. Загвоздка в том, что та же тенденция делает их крайне короткоживущими и опасными при нормальных условиях. Химики пытались приручить их, связывая с атомами металлов или окружая громоздкими органическими группами, но по-настоящему «свободные» нитrogenовые цепочки с лишним электроном — радикальные анионы — оставались слишком реактивными, чтобы их можно было изолировать в пробирке.
Создание стабильной четырехнитrogenовой цепочки
Авторы поставили цель получить устойчивую версию четырехнитrogenового радикального аниона, обозначаемого {N4}•−, без опоры на атомы металлов для фиксации. Они начали с простых арил-азидов, широко доступных лабораторных соединений, которые уже содержат фрагмент из трех азотов. Восстанавливая эти азиды в присутствии источника калия и лиганда в форме «короны», оборачивающего ион металла, они способствовали сшивке двух азидных звеньев «голова-к-голове», образуя линейную N–N–N–N цепочку, запертую по концам бромированными бензольными кольцами. Получившийся анион, записываемый как [(4‑BrC6H4)2N4]•−, кристаллизуется в виде эффектных черных игл, которые в твердом состоянии стабильны неделями при отсутствии воздуха. Данные рентгеновской дифракции показывают почти прямую цепочку из четырех атомов азота с длинами связей между типичными одиночными и двойными, что указывает на делокализацию лишнего электрона, а не его локализацию на одном атоме.
Где живет неспаренный электрон
Чтобы понять, почему эта цепочка необычно устойчива, команда сочетала несколько спектроскопических методов с квантово‑химическими расчетами. Электронный парамагнитный резонанс, метод обнаружения неспаренных электронов, показал, что радикальный характер распределен по всей молекуле, но наиболее выражен на двух терминальных атомах азота, стоящих у ароматических колец. Расчеты карт спиновой плотности подтверждают, что большая часть неспаренного электрона сосредоточена в N4 блоке, а бензольные кольца действуют подобно «предохранительным клапанам», помогая растянуть и стабилизировать электрон, аналогично тому, как они стабилизируют классические бензильные радикалы. Ультрафиолет–видимая спектроскопия и теоретический анализ дополнительно показывают сеть орбиталей совместного распределения электронов, напоминающую структуру простой углеродной цепочки, но построенную целиком из атомов азота. 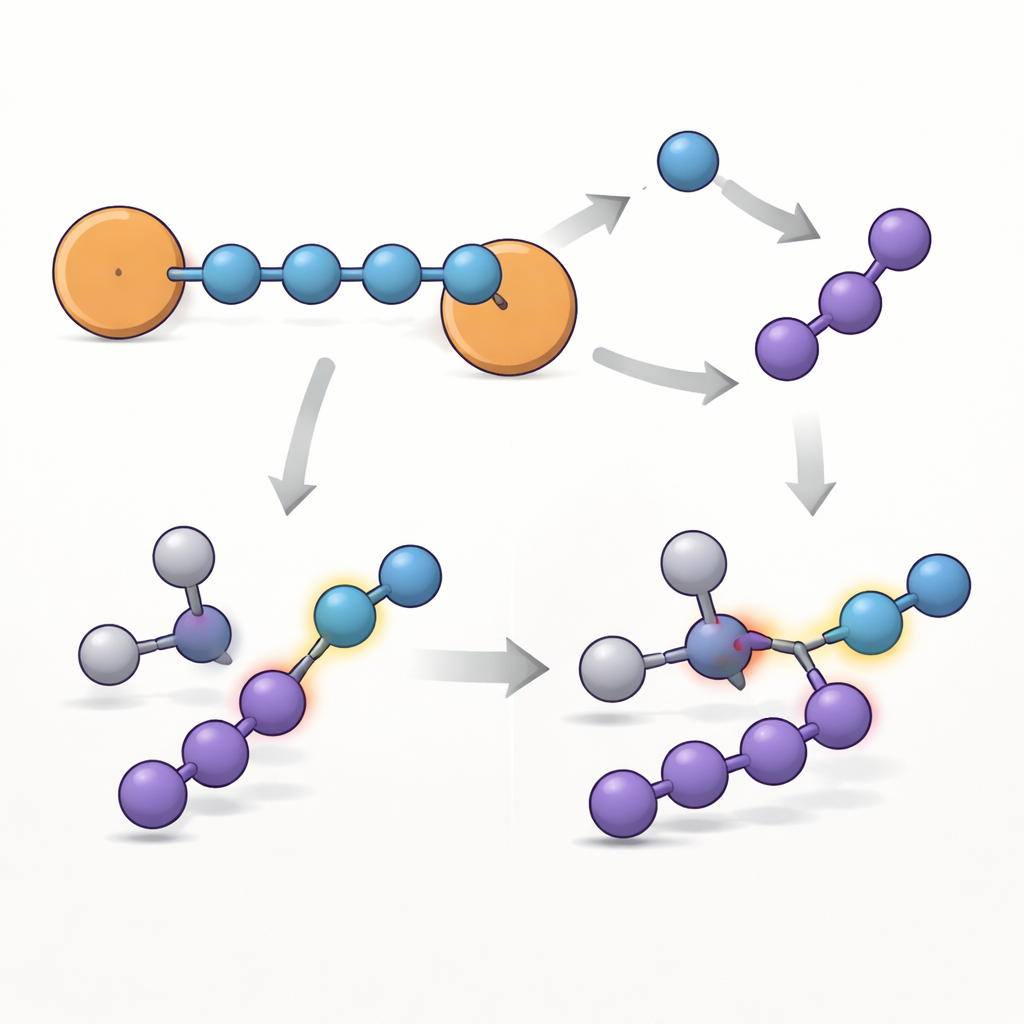
Семейство цепочек и новый источник азота
Подход оказался общим: изменяя заместитель на ароматическом кольце (фтор, хлор, метил или незамещенный фенил), авторы получили небольшую серию родственных молекул {N4}•−. Все они сохраняют ту же основную структуру цепочки, но их время жизни и точное распределение неспаренного электрона изменяются в зависимости от заместителя на кольце, показывая, что химики могут тонко настраивать устойчивость простыми органическими модификациями. Команда затем исследовала реакции флагманского бромированного соединения. При определенных условиях четырехнитrogenовая цепочка распадается на однозвенный фрагмент (N1) и трехнитrogenовый фрагмент (N3). Данные анализа продуктов и расчеты указывают, что один путь приводит к образованию радикального аниона нитрена — крайне реактивного азотсодержащего вида, способного внедряться в связи C–H. При реакции с ароматическим альдегидом система преобразует C–H связь карбонильной группы в амидную связь, демонстрируя, что этот кристаллический {N4}•− может служить хранимым, настольным источником реактивного азота для построения более сложных молекул.
Что это значит для будущей химии
Захватив деликатную четырехнитrogenовую радикальную цепочку в органической матрице, которая остается кристаллической и стабильной при комнатной температуре, эта работа превращает эфемерное атмосферное явление в осязаемый лабораторный реагент. Исследование показывает, что продуманно подобранные ароматические группы способны делокализовать заряд и спин в достаточной степени, чтобы подавить обычную взрывную потерю N2, но при этом позволять цепочке разрушаться контролируемо при запуске, высвобождая мощные однозвенные азотные фрагменты. Главная мысль для неспециалистов в том, что химики учатся укрощать одну из самых «диких» форм азота, открывая путь к новым высокоэнергетическим материалам и удобным твердым реагентам, которые переносят азотные фрагменты в фармацевтические и другие ценные продукты с гораздо большим контролем, чем это было ранее возможно.
Цитирование: Lister-Roberts, R., Galano, D., van IJzendoorn, B. et al. Crystalline nitrogen chain radical anions. Nat. Chem. 18, 686–694 (2026). https://doi.org/10.1038/s41557-025-02040-2
Ключевые слова: нитrogenовые цепочки, радикальные анионы, высокоэнергетические материалы, химия нитренов, синтез органоазота