Clear Sky Science · tr
Alzheimer’in Aβ’si, erken nanoküme çözünmesi yoluyla Tau faz ayrışmasını ve agregasyonunu katalizler
Alzheimer’ı anlamada bunun önemi
Alzheimer hastalığı, beyinde iki tür zararlı protein birikimiyle tanınır: sinir hücrelerinin dışında yapışkan amiloid‑beta (Aβ) plakları ve hücrelerin içinde Tau adı verilen bir proteinin dolanmış iplikçikleri. Klinik olarak her ikisinin de birlikte ortaya çıktığı ve hafıza kaybını kötüleştirdiği bilinmekle birlikte, birinin diğerini nasıl tetiklediği uzun süredir gizemini koruyor. Bu çalışma, ortak bir Aβ formunun Tau’u sıvı, geri dönüşümlü hâlden sert, toksik kümelere iten moleküler bir katalizör gibi davrandığını göstererek onların işbirliğinin gizli, erken bir aşamasını açığa çıkarıyor. Bu geçişin anlaşılması, tam gelişmiş plaklar ve düğümler oluşmadan çok önce hasarı durdurmanın yeni yollarını açabilir.
İki sorun çıkaran protein, bağlantılı bir öykü
Aβ ve Tau genellikle ayrı kötü karakterler olarak incelendi. Aβ, plaklar halinde toplanan kısa parçacıklar oluştururken, iç hücre iskeletine yardımcı olan Tau, nöronları tıkayan liflere dönüşebilir. Ancak sadece plaka yükü, bir kişinin bilişsel gerilemesinin şiddetiyle yakından ilişki göstermezken, Tau düğümleri gösterir. Bu örüntü, Aβ’nin sahneyi hazırlayıp Tau’nun hasarın büyük kısmını verdiği fikrini güçlendirmiştir. Yine de her iki proteinin hâlâ çözeltide dolaştığı veya küçük damlacıklar halinde yoğunlaştığı en erken adımlarda neler olduğu belirsizdi. Yazarlar, beyin sıvısında en bol bulunan Aβ türü olan Aβ40’a odaklanır ve bunun Tau’un yoğunlaşma, katılaşma ve nihayet sinir hücrelerine zehir olma eğilimini nasıl değiştirdiğini sorgular.
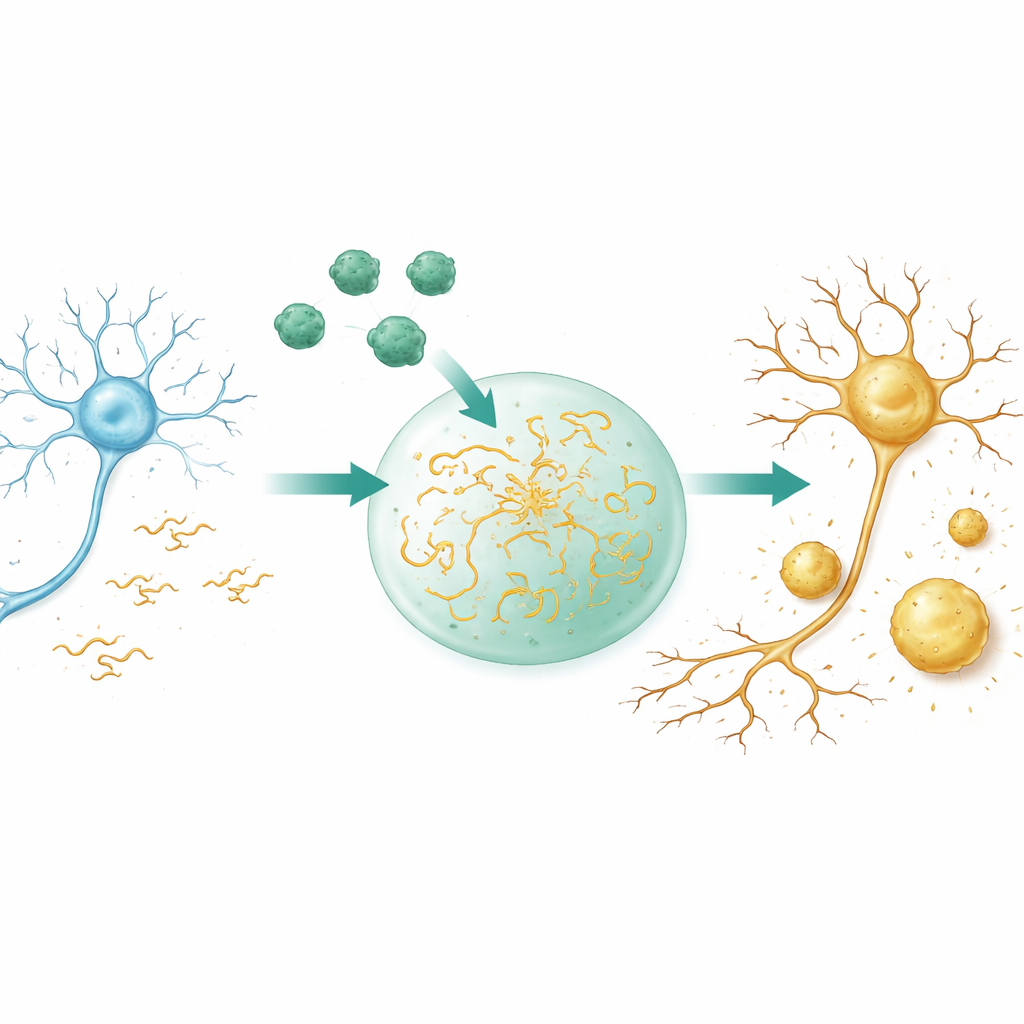
Geçici damlacıklardan sert kütlelere
Hücrelerde birçok protein, zar olmadan yağın suda ayrılması gibi damla benzeri kondensatlar halinde ayrışabilir. Bu damlacıklar molekülleri yoğunlaştırır, reaksiyonları hızlandırır ve daha sonra kalıcı çökeltilere sertleşebilir. Araştırmacılar, mikroskoplar ve ışığa dayalı ölçümler kullanarak, kendi koşullarında Aβ40’ın tek başına bu tür sıvı damlacıklar oluşturmadığını; bunun yerine doğrudan katı benzeri parçacıklara agregelendiğini gösterir. Oysa Tau kolaylıkla moleküllerinin hızla hareket edip karıştığı sıvı damlacıklar oluşturur. İki protein, kalabalık, hücreye benzer bir ortamda birleştirildiğinde, Aβ40 Tau damlacıklarının içine çekilir ve Tau’un yoğunlaşma eğilimini çarpıcı biçimde artırır. Damlacıklar daha düşük Tau düzeylerinde oluşur, daha hızlı ortaya çıkar, daha büyük büyür ve en önemlisi sıvı doğalarını daha çabuk kaybederek jelimsi ve sonra sert bir hâle gelirler.
Aβ’nin Tau’u nanoskalada nasıl yeniden şekillendirdiği
Herhangi bir görünür damlacık oluşmadan önce, Tau yalnızca tek moleküller halinde durmaz; tespit edilmesi zor, küçük dinamik kümeler de oluşturur. Hassas kütle ölçümleri ve nükleer manyetik rezonans kullanılarak ekip, Aβ40’ın başlangıçta bu Tau nanokümelerini daha küçük, daha çözünür türlere ayırdığını bulur. İlk bakışta bu koruyucu gibi görünebilir, ancak bilgisayar simülasyonları ve ek deneyler farklı bir tablo ortaya koyar. Aβ40 ile Tau karşılaştığında, Tau moleküllerinin daha sıkı paketlendiği ve daha az hareket ettiği, Aβ40’ın ise içinde görece hareketli kaldığı karışık kondensatların oluştuğu görülür. Ayrıntılı modelleme, her iki proteindeki yüklü ve suyu itin bölgelerin birbirini çektiğini ve aynı zamanda Tau–Tau temaslarını güçlendirdiğini gösterir. Net etki, Tau’un yoğunlaşma bariyerini ve bu kondensatların sertleşmesini düşürmektir.

Değişmiş damlacıklardan artan hücre hasarına
Yazarlar daha sonra bu değişen hâllerin canlı hücreler için ne anlama geldiğini sorgular. Liflere özgü yığılma biçimleri aldığında ışıldayan bir boya ile amiloid benzeri yapıları izlerler. Sadece Tau damlacıkları bu tür bir sinyal göstermezken, Aβ40 bulunduğunda yoğunlaşma içinde parlak, lif‑benzeri maddeler hızla ortaya çıkar ve fibril büyümeden önce normalde görülen yavaş “gecikme” neredeyse ortadan kalkar. Besi kaplarında büyütülen sinir‑benzeri hücrelerde, faz ayrışmasından geçmiş Tau ve Aβ40 karışımları, yalnızca Tau’a kıyasla belirgin biçimde daha zehirlidir. Kalabalıklaştırma yokken, Aβ40 bazen Tau agregatlarını daha çözünür ve biraz daha az zararlı hale getirebilir; bu, çevre koşullarına—beynin farklı bölgelerinde veya hastalığın farklı evrelerinde olacağı gibi—göre koruyucu ile yıkıcı etkileşimler arasındaki dengenin güçlü biçimde değiştiğini gösterir.
Gelecek tedaviler için ne anlama geliyor
Birlikte ele alındığında, bu çalışma Alzheimer kimyasının adımlı bir görüşünü destekler: Aβ40 önce erken Tau kümelerini dağıtır, sonra Tau’u ve kendisini yoğun damlacıklara toplar ve nihayet bu damlacıkların sert fibrillere ve toksik yapılara dönüşümünü hızlandırır. Bu bakımdan Aβ40 basit bir tetikleyiciden çok, Tau’u hastalıkla ilişkili yapılara giden belirli bir yola yönlendiren bir katalizör gibi davranır. Uzman olmayanlar için ana mesaj, Alzheimer’daki hasarın görünür plaklar ve düğümler ortaya çıkmadan çok önce, nanoskaladaki damlacıklar ve kümelerin gizli dünyasında belirlenebileceğidir. Aβ–Tau etkileşimlerini kesintiye uğratan, Tau kondensatlarını sıvı, geri döndürülebilir bir durumda tutan veya bunların katı agregalara sertleşmesini engelleyen tedaviler, nörodejenerasyonu yavaşlatmak veya durdurmak için yeni yollar sunabilir.
Atıf: Sun, X., Tang, Y., Wang, X. et al. Alzheimer’s Aβ catalyzes Tau phase separation and aggregation via early nanocluster solubilization. Nat Commun 17, 3755 (2026). https://doi.org/10.1038/s41467-026-70083-1
Anahtar kelimeler: Alzheimer hastalığı, amiloid‑beta, Tau proteini, faz ayrışması, protein agregasyonu