Clear Sky Science · he
א -β של אלצהיימר מקטלז הפרדה פאזית והצטברות של חלבון טאו באמצעות המסולק המוקדם של ננו‑אשכולות
מדוע זה חשוב להבנת אלצהיימר
מחלת אלצהיימר ידועה בשתי צורות הצטברות מזיקות של חלבונים במוח: פלאק‑עמילואיד‑בטא (Aβ) דביק מחוץ לתאי עצב וסבכים של חלבון שנקרא טאו בתוך התאים. רופאים יודעים ששתי הצורות מופיעות יחד ומחמירות את אובדן הזיכרון, אבל כיצד האחת מובילה לשנייה היה תעלומה ממושכת. המחקר הזה חושף שלב מוקדם ונסתר של השותפות ביניהן, ומראה שסוג שכיח של Aβ יכול לפעול כזרז מולקולרי שמנדנד את הטאו ממצב נוזלי והפיך אל גושים קשיחים וسمיים. הבנת המעבר הזה עשויה לפתוח דרכים חדשות למנוע את הנזק הרבה לפני שהפלאקים והסבכים המלאים נוצרים.
שני חלבונים מטרידים, סיפור מחובר אחד
Aβ וטאו נחקרו בדרך‑כלל כגורמים נפרדים. Aβ נוצר מקטעים קצרים שמתאספים לפלאקים, בעוד טאו, מסייע למבנה הפנימי של התא, יכול להתלפף לסיבים שמסתמים את הנוירונים. עם זאת, כמות הפלאקים לבדה אינה מתאמת היטב עם רמת הירידה הקוגניטיבית של אדם, בעוד שסבכי טאו כן. תבנית זו חיזקה את הרעיון ש‑Aβ עשוי להכין את הבמה וטאו מספק את רוב הנזק. עם זאת, מה שקורה בשלבים הראשונים — כאשר שני החלבונים עדיין נעים בתמיסה או מעובדים לטיפות זעירות — לא היה ברור. החוקרים מתמקדים ב‑Aβ40, הסוג השכיח ביותר של Aβ בנוזל המוח, ושואלים כיצד הוא משנה את הנטייה של טאו להתעבות, להתמצק ולרעיל בסופו של דבר תאי עצב.
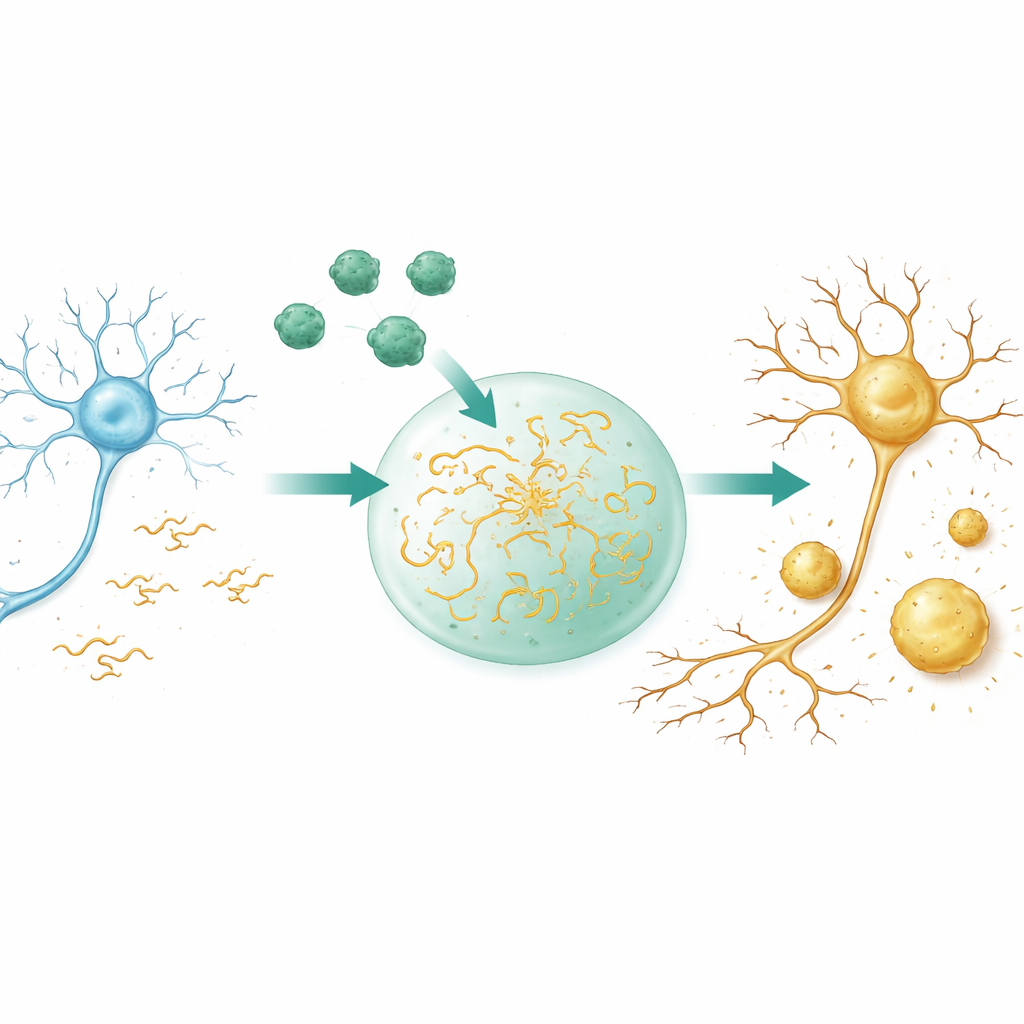
מתאים חולפים לטלאים מחוספסים
חלבונים רבים בתאים יכולים להיפרד לעיבויים דמויי‑טיפות, קצת כמו שמן במים, ללא צורך בממברנות. טיפות אלה מרוכזות במולקולות, מאיצות תגובות, ובהמשך יכולות להתמצק להפקדות קבועות יותר. בעזרת מיקרוסקופים ומדידות מבוססות אור, החוקרים מראים ש‑Aβ40 בעצמו אינו יוצר תחת תנאיהם טיפות נוזליות כאלה; במקום זאת הוא מתגבש ישירות לחלקיקים דמויי‑מוצק. טאו, בניגוד לכך, יוצר בקלות טיפות נוזליות שבהן המולקולות נעות במהירות ומתערבבות. כאשר שני החלבונים משולבים בסביבה צפופה המדמה תא, Aβ40 נמשך לתוך טיפות טאו ומגביר באופן דרמטי את קלות העיבוי של טאו. הטיפות נוצרות ברמות טאו נמוכות יותר, מופיעות מהר יותר, גדלות יותר, והכי חשוב — מאבדות את אופיין הנוזלי מהר יותר, הופכות לג’ל‑דמיות ואז לקשיחות.
כיצד Aβ מעצב את טאו בקנה‑מידה ננו
לפני שמופיעות טיפות גלויות, טאו אינו צף רק כמולקולות יחידות; הוא גם יוצר אשכולות ננו דינמיים וקטנים שקשה לגילוי. באמצעות מדידות מסה רגישות ודה‑הד למגנטית גרעינית, הקבוצה מגלה ש‑Aβ40 בתחילה מפרק את ננו‑אשכולות הטאו למינים קטנים יותר ונמסים יותר. במבט ראשון זה נשמע מגן, אבל סימולציות ממוחשבות וניסויים נוספים חושפים תמונה שונה. ברגע ש‑Aβ40 וטאו נתקלים זה בזה, הם בונים עיבויים מעורבים שבהם מולקולות טאו נארזות בצפיפות רבה יותר ונעות פחות, בעוד ש‑Aβ40 נשארת יחסית ניידת בפנים. דגמים מפורטים מראים כי אזורים טעונים ודחויי‑מים בשני החלבונים מושכים זה את זה ובמקביל מחזקים את מגעי טאו‑טאו. האפקט הנקי הוא הורדת המחסום לעיבוי של טאו ולחיזוק ההתמצקות של אותם עיבויים.

מהעיבויים המשתנים לנזק תאיים מוגבר
החוקרים שאלו אז מה משמעות המצבים המשתנים האלה לתאים חיים. הם עוקבים אחרי מבנים דמויי‑עמילואיד בעזרת צבע שמתלבלב כשחלבונים מאמצים את הצורות הערומות האופייניות לסיבים. טיפות טאו לבד מראות אות מועטת כזו, אך כאשר Aβ40 נוכח, חומר בהיר ודמוי‑סיב מופיע במהירות בתוך העיבויים, ותקופת ה"השהיה" האיטית של גידול סיבים כמעט נעלמת. בתאים דמויי‑עצבים שגודלו בפטריות, תערובות של טאו ו‑Aβ40 שעברו הפרדה פאזית רעילות באופן משמעותי יותר מטאו לבדו. ללא צפיפות הסביבה, Aβ40 עשוי לפעמים להפוך את הצברי הטאו ליותר מסיסים ופחות מזיקים במעט, מה שמרמז שהאיזון בין אינטראקציות מגנות להרוסות תלוי בחוזקה בתנאים מסביב — בדיוק כפי שיהיה באזורים או בשלבים שונים של המוח.
מה המשמעות לטיפולים עתידיים
במבט כולל, העבודה תומכת בתצורה שלבי של הכימיה באלצהיימר: Aβ40 תחילה מפזר אשכולות טאו מוקדמים, אחר כך מסייע לאסוף טאו ואת עצמו לטיפות צפופות, ולבסוף מואץ את המהפך של אותן טיפות לסיבים קשיחים ולצברים רעילים. במובן זה Aβ40 מתנהג פחות כטריגר פשוט ויותר כקטליזטור שמכוון את טאו לאורך מסלול מסוים לעבר מבנים מקושרי מחלה. למסיימים שאינם מומחים, המסר המרכזי הוא שהנזק באלצהיימר עשוי להיקבע הרבה לפני שהפלאקים והסבכים נראים לעין, בעולם נסתר של טיפות ואשכולות בננומקווה. טיפולים שמפריעים למגעי Aβ–טאו, משמרים את עיבויי הטאו במצב נוזלי והפיך, או מונעים את התמצקותם לצברים מוצקים עשויים להציע דרכים חדשות להאט או לעצור את הניוון העצבתי.
ציטוט: Sun, X., Tang, Y., Wang, X. et al. Alzheimer’s Aβ catalyzes Tau phase separation and aggregation via early nanocluster solubilization. Nat Commun 17, 3755 (2026). https://doi.org/10.1038/s41467-026-70083-1
מילות מפתח: מחלת אלצהיימר, עמילואיד‑בטא, חלבון טאו, הפרדה פאזית, הצטברות חלבונים