Clear Sky Science · ja
アルツハイマーのAβは初期ナノクラスターの可溶化を介してTauの相分離と凝集を触媒する
アルツハイマー理解においてなぜ重要か
アルツハイマー病は、神経細胞の外側にできる粘着性のアミロイドβ(Aβ)プラークと、細胞内で絡み合うTauというタンパク質の二種類の有害な蓄積で知られています。臨床では両者が同時に現れ記憶障害を悪化させることが分かっていますが、どちらがどのように相手を駆動するのかは長く謎のままでした。本研究はその共同作用の初期段階を明らかにし、一般的なAβの形態が分子触媒のように働いて、Tauを流動的で可逆的な状態から硬く有毒な塊へと押しやることを示します。この転換を理解することで、プラークやもつれが顕在化するずっと前に損傷を止める新たな治療戦略が開ける可能性があります。
二つの問題性タンパク質、つながった物語
AβとTauは従来、別々の敵として研究されてきました。Aβは短い断片が集まってプラークを形成し、一方で細胞内の足場を助けるTauは繊維状にねじれてニューロンを詰まらせ得ます。ただし、プラークの量だけでは認知機能の低下の程度をよく説明せず、Tauのもつれの方がより相関が強いことが知られています。このパターンが、Aβが舞台を整え、Tauが主要な損傷をもたらすという考えを後押ししてきました。しかし、両者がまだ溶液中や微小な液滴として渦巻いている最初の段階で何が起きるかは不明でした。著者らは脳脊髄液中で最も豊富なAβの形態であるAβ40に注目し、それがTauの凝集、固化、そして最終的に神経細胞へ有害になる傾向をどのように変えるかを問いかけます。
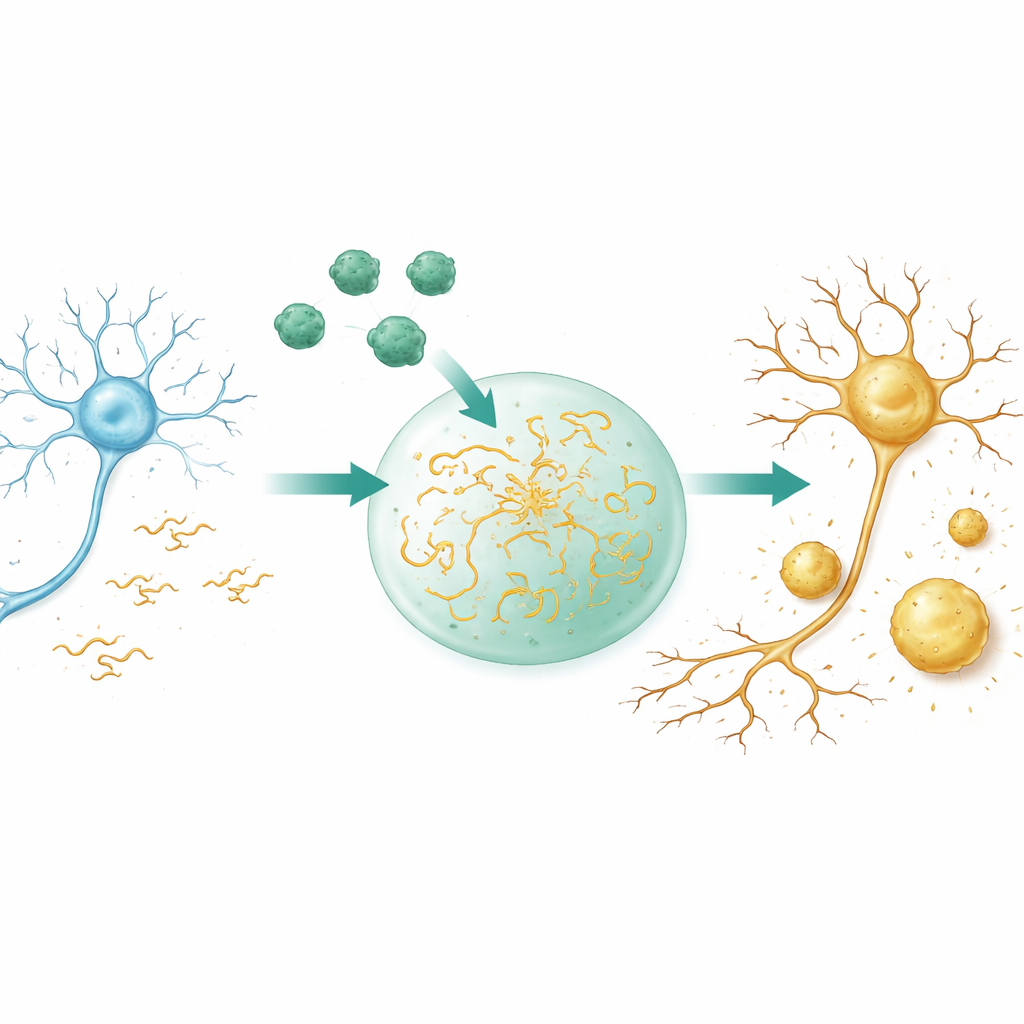
つかの間の液滴から硬化した塊へ
多くの細胞内タンパク質は膜を伴わずに油と水のように液滴様の凝縮体を形成できます。これらの液滴は分子を濃縮し反応を促進し、後により恒常的な堆積物へ硬化することがあります。顕微鏡や光学的計測を用いて、研究者らはAβ40単独では彼らの条件下でこうした液滴を形成せず、むしろ直接的に固体様の粒子へ凝集することを示します。対照的にTauは容易に液滴を作り、中の分子は活発に移動し混合します。二つのタンパク質を細胞のように混雑した環境で混合すると、Aβ40はTauの液滴に取り込まれ、Tauの凝集しやすさを劇的に高めます。液滴はより低いTau濃度で形成され、より速く現れ、より大きくなり、重要なことに液体の性質を速やかに失い、ゲル状から最終的に剛直になります。
AβがナノスケールでTauをどのように再構築するか
目に見える液滴が生じる前でさえ、Tauは単一分子だけで漂っているわけではなく、検出が難しい小さく動的なクラスターを形成しています。高感度の質量測定と核磁気共鳴を用いて、チームはAβ40が当初これらのTauナノクラスターをより小さく可溶性の高い種へと分解することを見出します。一見するとそれは保護的に思えますが、計算機シミュレーションと追加実験は異なる絵を示します。Aβ40とTauが出会うと、混合凝縮体が構築され、そこでTau分子はより密に詰まり移動性が低下する一方、Aβ40は比較的流動的なままでいることが明らかになります。詳細なモデリングは、両者の帯電領域や疎水性領域が互いに引き合い、同時にTau–Tau間の接触を強化することを示します。結果として、Tauが凝縮しそれらの凝縮体が硬化するための障壁が低くなります。

変化した液滴がもたらす細胞損傷の増大
著者らは次に、これらの状態変化が生きた細胞にとって何を意味するかを問います。タンパク質がフィブリル特有の積層構造をとると光る色素でアミロイド様の構造を追跡します。Tau単独の液滴はそのようなシグナルがほとんどありませんが、Aβ40が存在すると、凝縮体内に明るいフィブリル様の物質が急速に現れ、通常フィブリルが成長する前に見られる遅延がほぼ消失します。培養皿で育てた神経様細胞では、相分離を経たTauとAβ40の混合物はTau単独よりも著しく毒性が高くなります。混雑がない条件では、Aβ40はときにTau凝集体をより可溶化し有害性をやや低くすることもあり得るため、保護的相互作用と破壊的相互作用の天秤は周囲の条件に強く依存し、脳の領域や病期によって異なる可能性が高いことが示唆されます。
今後の治療に対する含意
総じて、本研究はアルツハイマーの化学的プロセスを段階的にとらえる見方を支持します:まずAβ40が初期のTauクラスターを散開させ、次にTauと自身を濃密な液滴へと集め、最後にそれらの液滴を剛直なフィブリルや有毒な集合体へと変換するのを促進します。この意味でAβ40は単純な発火装置というよりは、Tauを疾患関連構造へと特定の経路で導く触媒のように振る舞います。専門外の方への主要なメッセージは、アルツハイマーの損傷は可視的なプラークやもつれが現れるずっと前、ナノスケールの液滴やクラスターという隠れた世界で決まる可能性があるということです。Aβ–Tauの接触を遮断する、Tau凝縮体を流動で可逆的な状態に保つ、あるいはそれらが固体の凝集体へ硬化するのを防ぐ治療は、神経変性を遅らせるか止める新たな方法を提供するかもしれません。
引用: Sun, X., Tang, Y., Wang, X. et al. Alzheimer’s Aβ catalyzes Tau phase separation and aggregation via early nanocluster solubilization. Nat Commun 17, 3755 (2026). https://doi.org/10.1038/s41467-026-70083-1
キーワード: アルツハイマー病, アミロイドβ, Tauタンパク質, 相分離, タンパク質凝集