Clear Sky Science · it
La Aβ dell’Alzheimer catalizza la separazione di fase e l’aggregazione della Tau tramite la solubilizzazione precoce dei nanocluster
Perché questo è importante per comprendere l’Alzheimer
La malattia di Alzheimer è nota per due tipi di accumuli proteici dannosi nel cervello: placche appiccicose di amiloide‑beta (Aβ) all’esterno delle cellule nervose e grovigli di una proteina chiamata Tau all’interno di esse. I medici sanno che entrambi compaiono insieme e aggravano la perdita di memoria, ma come uno stimoli l’altro è stato a lungo un mistero. Questo studio mette in luce uno stadio iniziale nascosto della loro interazione, mostrando che una forma comune di Aβ può agire come un catalizzatore molecolare che spinge la Tau da uno stato fluido e reversibile in ammassi rigidi e tossici. Capire questo passaggio potrebbe aprire nuove strade per fermare il danno molto prima che si formino placche e grovigli evidenti.
Due proteine problematiche, una storia connessa
Aβ e Tau sono state di solito studiate come cattivi separati. Aβ forma frammenti corti che si raccolgono in placche, mentre la Tau, un aiuto per lo scheletro interno della cellula, può avvolgersi in fibre che intasano i neuroni. Tuttavia, il carico di placche da solo non corrisponde strettamente al grado di decadimento cognitivo di una persona, mentre i grovigli di Tau sì. Questo schema ha alimentato l’idea che Aβ possa preparare il terreno e che Tau infligga gran parte del danno. Tuttavia, ciò che accade nei primi passi—quando entrambe le proteine sono ancora in soluzione o condensate in minuscole goccioline—è rimasto poco chiaro. Gli autori si concentrano su Aβ40, il tipo di Aβ più abbondante nel fluido cerebrale, e indagano come questo modifichi la tendenza della Tau a condensarsi, solidificarsi e infine avvelenare le cellule nervose.
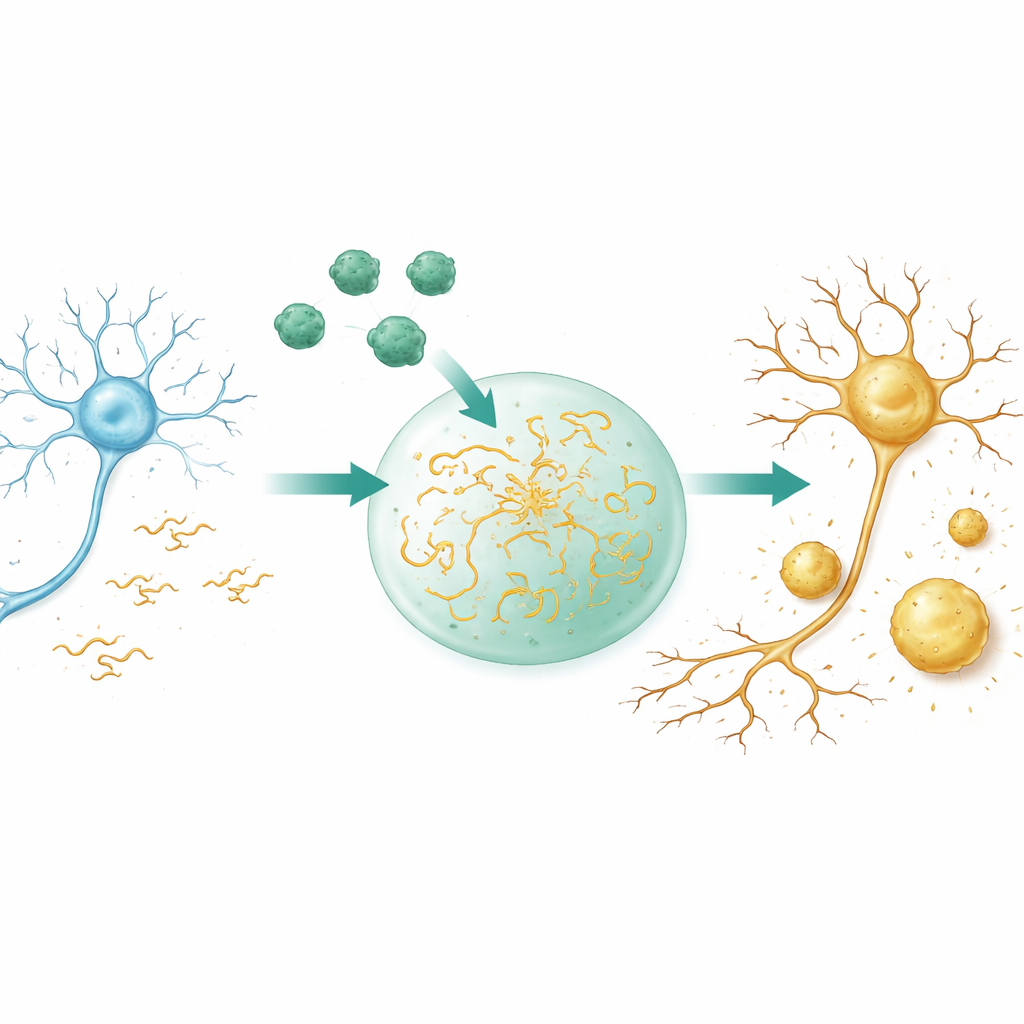
Da goccioline fugaci a grumi induriti
Molte proteine nelle cellule possono separarsi in condensati simili a goccioline, un po’ come olio in acqua, senza l’aiuto di membrane. Queste goccioline concentrano molecole, accelerano reazioni e possono poi indurirsi in depositi più permanenti. Usando microscopi e misure basate sulla luce, i ricercatori mostrano che Aβ40 da solo non forma tali goccioline nelle loro condizioni; al contrario, si aggrega direttamente in particelle di tipo solido. La Tau, invece, forma facilmente goccioline liquide le cui molecole si muovono rapidamente e si mescolano. Quando le due proteine sono combinate in un ambiente affollato e simile a quello cellulare, Aβ40 viene incorporata nelle goccioline di Tau e aumenta in modo drastico la facilità con cui Tau si condensa. Le goccioline si formano a livelli più bassi di Tau, compaiono più rapidamente, crescono di più e, cosa cruciale, perdono la loro natura liquida più in fretta, diventando gel‑like e poi rigide.
Come Aβ rimodella la Tau su scala nanometrica
Prima che emergano goccioline visibili, la Tau non galleggia solo come singole molecole; forma anche minuscoli cluster dinamici difficili da rilevare. Usando misure di massa sensibili e risonanza magnetica nucleare, il gruppo scopre che Aβ40 inizialmente spezza questi nanocluster di Tau in specie più piccole e più solubili. A prima vista ciò sembra protettivo, ma simulazioni al computer e ulteriori esperimenti rivelano un quadro diverso. Quando Aβ40 e Tau si incontrano, costruiscono condensati misti in cui le molecole di Tau si impaccano più strettamente e si muovono meno, mentre Aβ40 resta relativamente mobile all’interno. Modellizzazioni dettagliate mostrano che regioni cariche e idrofobiche di entrambe le proteine si attraggono reciprocamente e nello stesso tempo rafforzano i contatti Tau–Tau. L’effetto netto è abbassare la barriera per la condensazione della Tau e per l’indurimento di quei condensati.

Da goccioline alterate a maggiore danno cellulare
Gli autori chiedono poi cosa significano questi stati mutati per le cellule viventi. Tracciano strutture simili ad amiloidi con un colorante che si illumina quando le proteine adottano le forme impilate tipiche dei fibrilli. Le goccioline di Tau da sole mostrano poco segnale di questo tipo, ma quando Aβ40 è presente compare rapidamente materiale brillante, simile a fibrilli, all’interno dei condensati, e il solito lento “ritardo” prima della crescita dei fibrilli è quasi cancellato. In cellule di tipo nervoso coltivate in piastre, miscele di Tau e Aβ40 che hanno subito separazione di fase sono nettamente più tossiche della sola Tau. In assenza di effetto di affollamento, Aβ40 può talvolta rendere gli aggregati di Tau più solubili e leggermente meno dannosi, suggerendo che l’equilibrio tra interazioni protettive e distruttive dipende fortemente dalle condizioni circostanti—proprio come avverrebbe in diverse regioni o fasi del cervello.
Cosa significa per i trattamenti futuri
Nel complesso, il lavoro sostiene una visione a stadi della chimica dell’Alzheimer: Aβ40 prima disperde i primi cluster di Tau, poi aiuta a raccogliere Tau e se stessa in goccioline dense, e infine accelera la trasformazione di quelle goccioline in fibrilli rigidi e assemblaggi tossici. In questo senso, Aβ40 si comporta meno come un semplice innesco e più come un catalizzatore che indirizza la Tau lungo un percorso verso strutture legate alla malattia. Per il pubblico generale, il messaggio chiave è che il danno nell’Alzheimer può essere deciso molto prima che compaiano placche e grovigli visibili, in un mondo nascosto di goccioline e cluster su scala nanometrica. Terapie che interrompono i contatti Aβ–Tau, mantengono i condensati di Tau in uno stato fluido e reversibile o prevengono il loro indurimento in aggregati solidi potrebbero offrire nuove vie per rallentare o fermare la neurodegenerazione.
Citazione: Sun, X., Tang, Y., Wang, X. et al. Alzheimer’s Aβ catalyzes Tau phase separation and aggregation via early nanocluster solubilization. Nat Commun 17, 3755 (2026). https://doi.org/10.1038/s41467-026-70083-1
Parole chiave: Malattia di Alzheimer, amiloide‑beta, proteina Tau, separazione di fase, aggregazione proteica