Clear Sky Science · de
Alzheimer’s Aβ katalysiert Tau-Phasentrennung und Aggregation über frühe Auflösung von Nanoklustern
Warum das für das Verständnis von Alzheimer wichtig ist
Die Alzheimer‑Krankheit ist bekannt für zwei Arten schädlicher Proteinablagerungen im Gehirn: klebrige Amyloid‑Beta (Aβ)-Plaques außerhalb von Nervenzellen und verhedderte Fasern eines Proteins namens Tau in deren Inneren. Ärztinnen und Ärzte wissen, dass beide zusammen auftreten und den Gedächtnisverlust verschlechtern, doch wie das eine das andere antreibt, war lange unklar. Diese Studie enthüllt eine versteckte, frühe Phase ihrer Wechselwirkung und zeigt, dass eine verbreitete Aβ‑Form wie ein molekularer Katalysator wirken kann, der Tau von einem flüssigen, reversiblen Zustand in starre, toxische Klumpen überführt. Das Verständnis dieses Übergangs könnte neue Wege eröffnen, Schäden zu verhindern, noch bevor sich ausgeprägte Plaques und Verfilzungen bilden.
Zwei problematische Proteine, eine zusammenhängende Geschichte
Aβ und Tau wurden bislang meist getrennt als Schurken betrachtet. Aβ bildet kurze Fragmente, die sich zu Plaques sammeln, während Tau, ein Helfer des intrazellulären Gerüsts, zu Fasern verdrillt, die Neurone verstopfen können. Die Plaque‑Last allein korreliert jedoch nicht eng mit dem Ausmaß kognitiver Verschlechterung, während Tau‑Verfilzungen das tun. Dieses Muster nährt die Idee, dass Aβ die Bühne bereiten und Tau den größten Teil des Schadens anrichten könnte. Was aber in den frühesten Schritten geschieht — wenn beide Proteine noch in Lösung schwimmen oder in winzigen Tröpfchen kondensiert vorliegen — war unklar. Die Autorinnen und Autoren konzentrieren sich auf Aβ40, den in der Gehirnflüssigkeit häufigsten Aβ‑Typ, und untersuchen, wie er Taus Neigung zur Kondensation, Verfestigung und letztlich zur Vergiftung von Nervenzellen verändert.
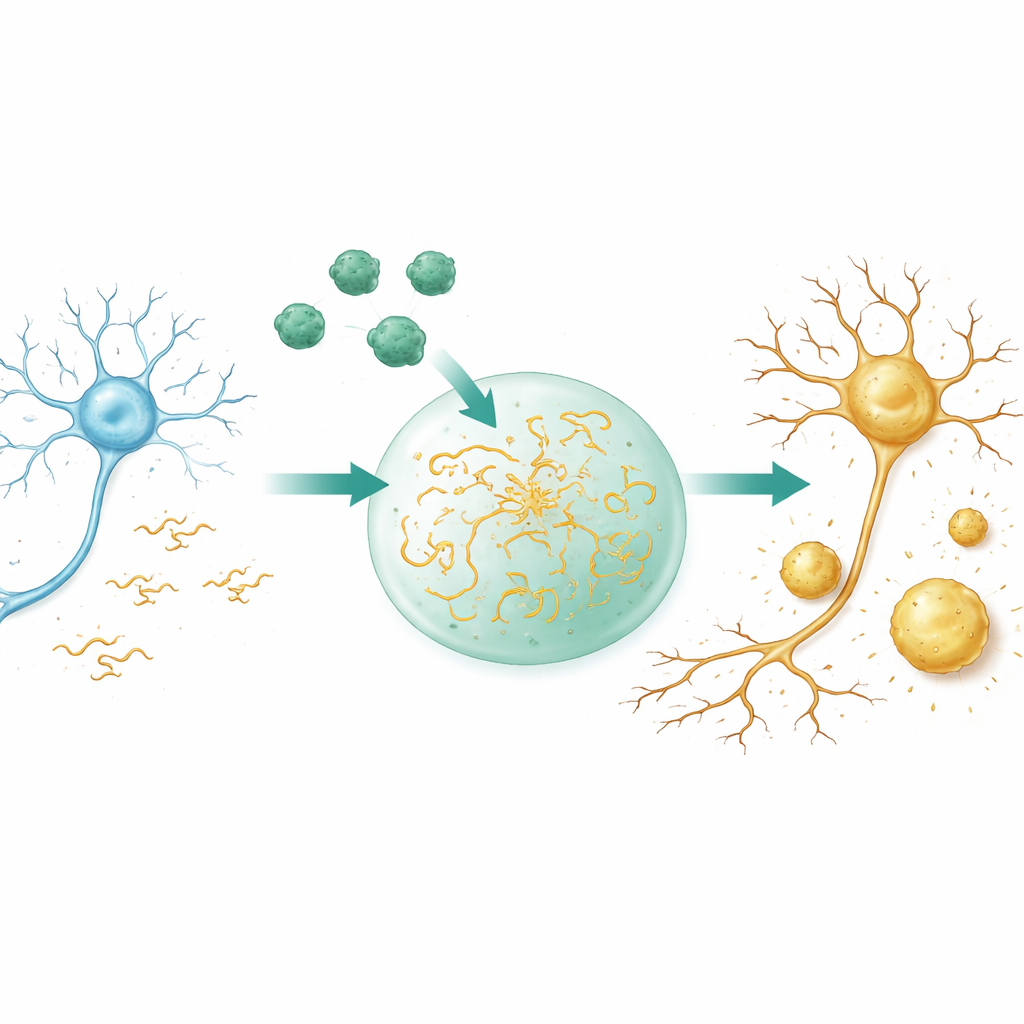
Von flüchtigen Tröpfchen zu verhärteten Klumpen
Viele Proteine in Zellen können sich in tröpfchenartige Kondensate trennen, ähnlich wie Öl in Wasser, ohne Membranen zu benötigen. Diese Tröpfchen konzentrieren Moleküle, beschleunigen Reaktionen und können später zu dauerhaft‑eren Ablagerungen verfestigen. Mit Hilfe von Mikroskopen und lichtbasierten Messungen zeigen die Forschenden, dass Aβ40 allein unter ihren Bedingungen solche flüssigen Tröpfchen nicht bildet, sondern direkt in fest‑ähnliche Partikel aggregiert. Tau dagegen bildet leicht flüssige Tröpfchen, deren Moleküle sich schnell bewegen und vermischen. Werden die beiden Proteine in einer dichten, zellähnlichen Umgebung kombiniert, wird Aβ40 in Tau‑Tröpfchen hineingezogen und verstärkt dramatisch die Neigung von Tau zur Kondensation. Tröpfchen entstehen bei niedrigeren Tau‑Konzentrationen, erscheinen schneller, wachsen größer und verlieren, entscheidend, ihre flüssige Natur schneller, werden gel‑ähnlich und schließlich starr.
Wie Aβ Tau im Nanomaßstab umgestaltet
Bevor sichtbare Tröpfchen entstehen, liegt Tau nicht nur als einzelne Moleküle vor; es bildet auch winzige, dynamische Nanokluster, die schwer nachzuweisen sind. Mithilfe empfindlicher Massemessungen und Kernspinresonanz findet das Team, dass Aβ40 zunächst diese Tau‑Nanokluster in kleinere, besser lösliche Spezies aufspaltet. Auf den ersten Blick klingt das schützend, doch Computersimulationen und weitere Experimente zeichnen ein anderes Bild. Sobald Aβ40 und Tau aufeinandertreffen, bilden sie gemischte Kondensate, in denen Tau‑Moleküle dichter gepackt sind und sich weniger bewegen, während Aβ40 relativ mobil bleibt. Detaillierte Modellierung zeigt, dass geladene und wasserabweisende Regionen beider Proteine einander anziehen und gleichzeitig Tau–Tau‑Kontakte stärken. Der Nettoeffekt ist eine Verringerung der Barriere für die Tau‑Kondensation und für die Verfestigung dieser Kondensate.

Von veränderten Tröpfchen zu größerem Zellschaden
Die Autorinnen und Autoren fragen dann, was diese veränderten Zustände für lebende Zellen bedeuten. Sie verfolgen amyloid‑artige Strukturen mit einem Farbstoff, der aufleuchtet, wenn Proteine die typischen gestapelten Formen von Fibrillen annehmen. Tau‑Tröpfchen allein zeigen kaum ein solches Signal, aber in Gegenwart von Aβ40 erscheint schnell heller, fibrillenähnlicher Stoff in den Kondensaten, und die übliche langsame „Latenzzeit“ vor dem Fibrillenwachstum wird nahezu aufgehoben. In in Schalen gezüchteten nervenähnlichen Zellen sind Gemische aus Tau und Aβ40, die eine Phasentrennung durchlaufen haben, deutlich toxischer als Tau allein. Ohne Crowding kann Aβ40 Tau‑Aggregate manchmal löslicher und etwas weniger schädlich machen, was darauf hindeutet, dass das Gleichgewicht zwischen schützenden und zerstörerischen Wechselwirkungen stark von den umgebenden Bedingungen abhängt — ähnlich wie in verschiedenen Regionen oder Stadien des Gehirns.
Was das für künftige Therapien bedeutet
In der Summe stützt die Arbeit eine schrittweise Sicht auf die Chemie von Alzheimer: Aβ40 löst zunächst frühe Tau‑Cluster auf, hilft dann, Tau und sich selbst in dichte Tröpfchen zu sammeln, und beschleunigt schließlich die Umwandlung dieser Tröpfchen in starre Fibrillen und toxische Assemblagen. In diesem Sinne verhält sich Aβ40 weniger wie ein einfacher Auslöser und mehr wie ein Katalysator, der Tau auf einem bestimmten Pfad zu krankheitsassoziierten Strukturen lenkt. Für Nicht‑Spezialisten ist die Kernbotschaft, dass der Schaden bei Alzheimer lange vor dem Auftreten sichtbarer Plaques und Verfilzungen entschieden wird — in einer verborgenen Welt nanoskaliger Tröpfchen und Cluster. Therapien, die Aβ–Tau‑Kontakt unterbrechen, Tau‑Kondensate in einem flüssigen, reversiblen Zustand halten oder deren Verhärtung zu festen Aggregaten verhindern, könnten neue Wege bieten, Neurodegeneration zu verlangsamen oder zu stoppen.
Zitation: Sun, X., Tang, Y., Wang, X. et al. Alzheimer’s Aβ catalyzes Tau phase separation and aggregation via early nanocluster solubilization. Nat Commun 17, 3755 (2026). https://doi.org/10.1038/s41467-026-70083-1
Schlüsselwörter: Alzheimer-Krankheit, Amyloid‑Beta, Tau‑Protein, Phasentrennung, Proteinaggregation