Clear Sky Science · ar
Aβ في مرض ألزهايمر يحفز انفصال الطور وتجميع بروتين تاو عبر إذابة النانو‑عناقيد المبكرة
لماذا هذا مهم لفهم ألزهايمر
يشتهر مرض ألزهايمر بنوعين من تراكمات البروتين الضارة في الدماغ: لويحات لزجة من الأميلويد‑بيتا (Aβ) خارج الخلايا العصبية وخيوط معقودة من بروتين يُدعى تاو بداخلها. يعرف الأطباء أن كلاهما يظهران معًا ويزيدان فقدان الذاكرة، لكن كيفية دفع أحدهما للآخر ظلت لغزًا طويل الأمد. تكشف هذه الدراسة عن مرحلة مبكرة خفية لشراكتهما، مبينة أن شكلًا شائعًا من Aβ يمكن أن يعمل كعامل محفز جزيئي يدفع تاو من حالة سائلة وقابلة للانعكاس إلى تكتلات صلبة وسامة. قد يفتح فهم هذا الانتقال طرقًا جديدة لإيقاف الضرر قبل تكوّن اللويحات والعقيدات بوضوح.
بروتَينان مُسبِّبان للمشاكل، وقصة واحدة مترابطة
عادة ما دُرِسا Aβ وتاو كأشرار منفصلين. يشكل Aβ شظايا قصيرة تتجمع لتكوّن لويحات، بينما يعمل تاو كمساعد لهياكل داخل الخلية ويمكن أن يلتف إلى ألياف تسد الخلايا العصبية. مع ذلك، فإن عبء اللويحات وحده لا يتطابق بدقة مع مدى تراجع قدرات التفكير لدى الشخص، بينما تُظهر عقد تاو ارتباطًا أوثق بالتدهور المعرفي. غذت هذه الصورة الفكرة القائلة بأن Aβ قد تمهّد الطريق وأن تاو يسبب الجزء الأكبر من الضرر. ومع ذلك، ما يحدث في الخطوات الأولى — عندما لا يزال كلا البروتينين يدوران في المحلول أو يتكثفان في قطرات صغيرة — ظل غامضًا. يركز المؤلفون على Aβ40، النوع الأكثر وفرة من Aβ في سوائل الدماغ، ويبحثون كيف يغيّر ميل تاو للتكثف والتصلب وفي النهاية تسميم الخلايا العصبية.
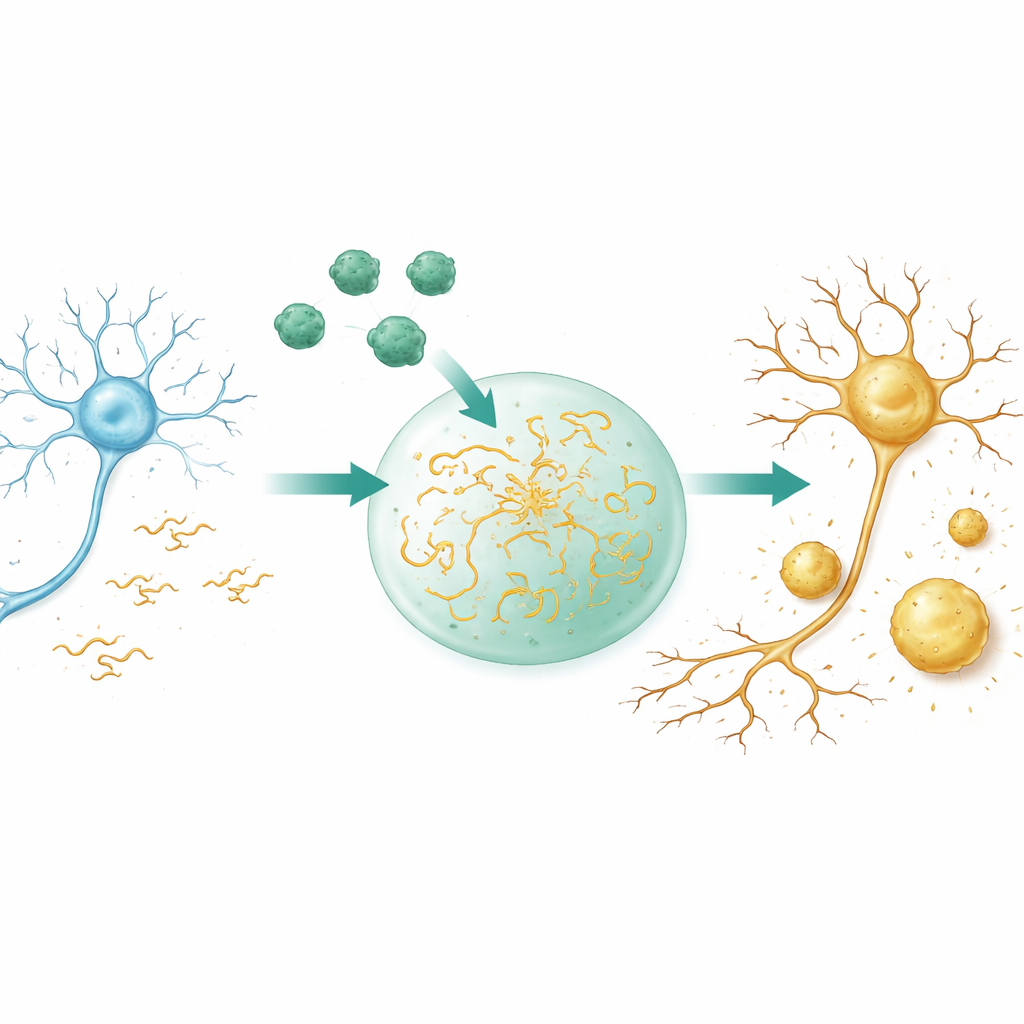
من قطرات عابرة إلى تكتلات متصلبة
يمكن لكثير من البروتينات في الخلايا أن تنفصل إلى مكثفات شبيهة بالقطرات، شبيهة إلى حد ما بزيت في ماء، دون الحاجة إلى أغشية. هذه القطرات تركز الجزيئات، تسرع التفاعلات، وقد تتصلّب لاحقًا إلى رواسب أكثر ديمومة. باستخدام المجاهر وقياسات ضوئية، يظهر الباحثون أن Aβ40 بمفرده لا يشكل مثل هذه القطرات السائلة في شروطهم؛ بل يتجمع مباشرة إلى جسيمات شبيهة بالصلابة. بالمقابل، يشكل تاو قطرات سائلة بسهولة حيث تتحرك جزيئاتها بسرعة وتختلط. عند خلط البروتينين في بيئة مكتظة تشبه الخلايا، يُجذَب Aβ40 إلى قطرات تاو ويعزز بشدة قابلية تاو على التكثف. تتكوّن القطرات عند مستويات تاو أقل، وتظهر أسرع، وتنمو أكبر، والأهم أنها تفقد طبيعتها السائلة بسرعة أكبر، فتتحول إلى هلام ثم إلى صلبة.
كيف يعيد Aβ تشكيل تاو على مستوى النانومتر
قبل ظهور أي قطرات مرئية، لا يطفو تاو فقط كجزيئات مفردة؛ بل يشكل أيضًا عناقيد نانوية صغيرة وديناميكية يصعب اكتشافها. باستخدام قياسات كتل حساسة والرنين المغناطيسي النووي، يجد الفريق أن Aβ40 يكسر في البداية هذه النانو‑عناقيد لتشكيلات أصغر وأكثر قابلية للذوبان. من الوهلة الأولى قد يبدو ذلك حماية، لكن المحاكاة الحاسوبية والتجارب الإضافية تكشف صورة مختلفة. بمجرد أن يلتقي Aβ40 وتاو، يبنون مكثفات مختلطة حيث تتكدّس جزيئات تاو بإحكام أكثر وتتحرك أقل، بينما يبقى Aβ40 أكثر حركة نسبياً داخلها. تُظهر النمذجة التفصيلية أن المناطق المشحونة والمناهضة للماء على كلا البروتينين تجذب بعضها البعض وفي الوقت نفسه تقوّي اتصالات تاو–تاو. التأثير الصافي هو خفض الحاجز أمام تكثف تاو وتصلب تلك المكثفات.

من قطرات متغيرة إلى ضرر خلوي أكبر
ثم يسأل المؤلفون ماذا تعني هذه الحالات المتغيرة للخلايا الحية. يتتبعون هياكل شبيهة بالأميلويد بصبغة تتوهج عندما تتخذ البروتينات الأشكال المكدسة النموذجية للألياف. تظهر قطرات تاو وحدها إشارة قليلة من هذا النوع، لكن عندما يكون Aβ40 حاضرًا، يظهر داخل المكثفات مادة ساطعة تشبه الألياف بسرعة، ويكاد يُمحى التأخير البطيء المعتاد قبل نمو الألياف. في خلايا شبيهة بالعصب تنمو في أطباق، تكون مخاليط تاو وAβ40 التي خضعت لانفصال الطور أكثر سمية بصورة ملحوظة من تاو وحده. بدون تكديس، يمكن أن يجعل Aβ40 أحيانًا تجمعات تاو أكثر قابلية للذوبان وأقل ضررًا قليلًا، مما يوحي بأن التوازن بين التفاعلات الوقائية والمدمرة يعتمد بشدة على الظروف المحيطة — تمامًا كما يحدث في مناطق أو مراحل مختلفة من الدماغ.
ما يعنيه هذا للعلاجات المستقبلية
بشكل مجمل، تدعم هذه الأعمال رؤية مرحلية لكيمياء ألزهايمر: يبدد Aβ40 أولًا عناقيد تاو المبكرة، ثم يساعد في جمع تاو ونفسه إلى قطرات كثيفة، وأخيرًا يسرّع تحول تلك القطرات إلى ألياف صلبة وتجميعات سامة. بهذا المعنى، يتصرف Aβ40 أقل كزناد بسيط وأكثر كعامل محفز يوجّه تاو عبر مسار معين نحو هياكل مرتبطة بالمرض. للمتخصصين غير المتخصصين، الرسالة الأساسية أن الضرر في ألزهايمر قد يتحدد قبل بوقت طويل من ظهور اللويحات والعقيدات المرئية، في عالم خفي من القطرات والعناقيد النانوية. قد توفر علاجات تقطع تلامس Aβ–Tau، تحافظ على مكثفات تاو في حالة سائلة وقابلة للانعكاس، أو تمنع تصلبها إلى تجمعات صلبة، طرائق جديدة لإبطاء أو إيقاف التنكس العصبي.
الاستشهاد: Sun, X., Tang, Y., Wang, X. et al. Alzheimer’s Aβ catalyzes Tau phase separation and aggregation via early nanocluster solubilization. Nat Commun 17, 3755 (2026). https://doi.org/10.1038/s41467-026-70083-1
الكلمات المفتاحية: مرض ألزهايمر, أميلويد‑بيتا, بروتين تاو, انفصال الطور, تجميع البروتين