Clear Sky Science · nl
Alzheimer’s Aβ katalyseert Tau-faseovergang en aggregatie via vroege oplossingsvorming van nanoclusters
Waarom dit belangrijk is voor het begrijpen van Alzheimer
De ziekte van Alzheimer staat bekend om twee typen schadelijke eiwitophopingen in de hersenen: kleverige amyloïd‑beta (Aβ) plaques buiten zenuwcellen en verwarde strengen van een eiwit genaamd Tau binnenin die cellen. Artsen weten dat beide tegelijk voorkomen en geheugenverlies verergeren, maar hoe het ene het andere aanjaagt bleef lange tijd een raadsel. Deze studie onthult een verborgen, vroeg stadium van hun samenspel en laat zien dat een veelvoorkomende vorm van Aβ kan optreden als een moleculaire katalysator die Tau van een vloeibare, omkeerbare toestand naar stijve, toxische klonten duwt. Begrijpen hoe die verschuiving plaatsvindt kan nieuwe wegen openen om schade te stoppen lang voordat zichtbare plaques en verstrikkingen ontstaan.
Twee probleemgevende eiwitten, één samenhangend verhaal
Aβ en Tau zijn meestal afzonderlijk bestudeerd als boosdoeners. Aβ vormt korte fragmenten die zich verzamelen tot plaques, terwijl Tau, een hulp bij het interne cel‑skelet, in vezels kan draaien die neuronen verstoppen. De hoeveelheid plaques alleen correleert echter niet sterk met hoe ernstig iemands denken verslechtert, terwijl Tau‑verstrikkingen dat wel doen. Dat patroon voedt het idee dat Aβ het decor kan bereiden en dat Tau veel van de schade levert. Toch was onduidelijk wat er in de allervroegste stappen gebeurt—wanneer beide eiwitten nog in oplossing zweven of geconcentreerd zijn in microscopische druppels. De auteurs richten zich op Aβ40, de meest voorkomende Aβ‑variant in hersenvocht, en onderzoeken hoe deze de neiging van Tau om te condenseren, te verharden en uiteindelijk zenuwcellen te vergiftigen, verandert.
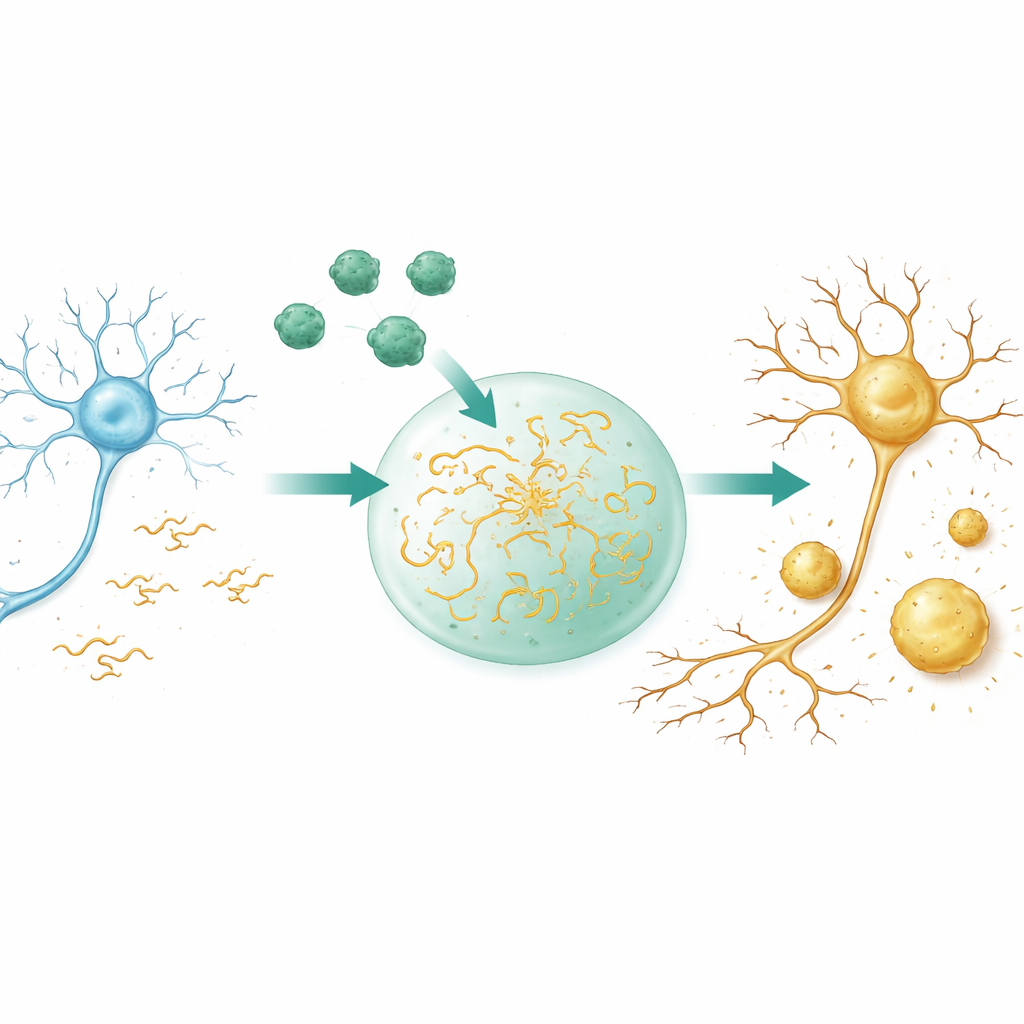
Van vluchtige druppels naar verharde klonten
Veel eiwitten in cellen kunnen zich zonder membranen scheiden in druppelachtige condensaten, enigszins vergelijkbaar met olie in water. Deze druppels concentreren moleculen, versnellen reacties en kunnen later verharden tot meer permanente afzettingen. Met behulp van microscopen en lichtgebaseerde metingen tonen de onderzoekers aan dat Aβ40 op zichzelf onder hun omstandigheden geen zulke vloeibare druppels vormt; in plaats daarvan aggregeert het rechtstreeks tot deeltjes met vaste eigenschappen. Tau vormt daarentegen gemakkelijk vloeibare druppels waarvan de moleculen zich snel verplaatsen en mengen. Wanneer de twee eiwitten in een drukbezette, celachtige omgeving worden gecombineerd, wordt Aβ40 in Tau‑druppels opgenomen en vergroot het dramatisch hoe gemakkelijk Tau condenseert. Druppels ontstaan bij lagere Tau‑concentraties, verschijnen sneller, groeien groter en verliezen—cruciaal—snel hun vloeibare aard, eerst gelachtig en vervolgens rigide.
Hoe Aβ Tau op nanoschaal herschikt
Voordat zichtbare druppels verschijnen, ligt Tau niet alleen als losse moleculen voor; het vormt ook kleine, dynamische clusters die moeilijk te detecteren zijn. Met gevoelige massametingen en kernspinresonantie vindt het team dat Aβ40 aanvankelijk deze Tau‑nanoclusters uiteenrafelt in kleinere, beter oplosbare soorten. Dat lijkt op het eerste gezicht beschermend, maar computersimulaties en aanvullende experimenten schetsen een ander beeld. Zodra Aβ40 en Tau elkaar ontmoeten, bouwen ze gemengde condensaten op waarin Tau‑moleculen dichter op elkaar gaan zitten en minder bewegen, terwijl Aβ40 relatief mobiel blijft. Details van modellering tonen aan dat geladen en waterafstotende regio’s op beide eiwitten elkaar aantrekken en tegelijkertijd Tau–Tau‑contacten versterken. Het netto‑effect is dat de drempel voor Tau‑condensatie en het verstenen van die condensaten wordt verlaagd.

Van veranderde druppels naar meer celschade
De auteurs vragen vervolgens wat deze veranderende toestanden betekenen voor levende cellen. Ze volgen amyloïde‑achtige structuren met een kleurstof die oplicht wanneer eiwitten de gestapelde vormen aannemen die kenmerkend zijn voor fibrillen. Tau‑druppels op zichzelf tonen weinig van zo’n signaal, maar wanneer Aβ40 aanwezig is, verschijnt er snel helder, fibril‑achtig materiaal binnen de condensaten en is de gebruikelijke trage “vertraging” voor fibrilgroei vrijwel verdwenen. In zenuw‑achtige cellen die in schaaltjes zijn gekweekt, zijn mengsels van Tau en Aβ40 die fase‑scheiding hebben ondergaan aanzienlijk toxischer dan Tau alleen. Zonder drukbezette omgeving kan Aβ40 soms Tau‑aggregaten oplosbaarder en iets minder schadelijk maken, wat suggereert dat het evenwicht tussen beschermende en destructieve interacties sterk afhangt van de omringende omstandigheden—net zoals dat in verschillende hersengebieden of ziektestadia het geval zou zijn.
Wat dit betekent voor toekomstige behandelingen
Gezamenlijk ondersteunen de resultaten een stapsgewijze kijk op de scheikunde van Alzheimer: Aβ40 verspreidt eerst vroege Tau‑clusters, helpt daarna Tau en zichzelf samen te brengen in dichte druppels, en versnelt uiteindelijk de transformatie van die druppels naar stijve fibrillen en toxische assemblages. In die zin gedraagt Aβ40 zich minder als een eenvoudige trigger en meer als een katalysator die Tau langs een bepaald pad naar ziekte‑gerelateerde structuren stuurt. Voor niet‑specialisten is de kernboodschap dat de schade bij Alzheimer mogelijk al wordt bepaald lang voordat zichtbare plaques en verstrikkingen verschijnen, in een verborgen wereld van nanoschaal‑druppels en clusters. Therapieën die Aβ–Tau‑contacten onderbreken, Tau‑condensaten vloeibaar en omkeerbaar houden, of hun verharding tot vaste aggregaten voorkomen, zouden nieuwe manieren kunnen bieden om neurodegeneratie te vertragen of te stoppen.
Bronvermelding: Sun, X., Tang, Y., Wang, X. et al. Alzheimer’s Aβ catalyzes Tau phase separation and aggregation via early nanocluster solubilization. Nat Commun 17, 3755 (2026). https://doi.org/10.1038/s41467-026-70083-1
Trefwoorden: Ziekte van Alzheimer, amyloïd‑beta, Tau‑eiwit, faseovergang, eiwitaggregatie