Clear Sky Science · tr
CircIQGAP1-CARM1 ekseni, glikolitik yeniden programlama yoluyla böbrek hücreli karsinom progresyonunu teşvik eder
Böbrek Kanserinin Şeker Alışkanlığı Neden Önemli
Böbrek kanseri, özellikle yaygın clear cell (temiz hücre) tipi, dünya genelinde artış göstermekle birlikte sıklıkla yayılana kadar fark edilmiyor. Pek çok tümörde olduğu gibi bu kanserler de şeker kullanım yollarını yeniden düzenleyerek, oksijen mevcut olsa bile glukozu yüksek hızda yakarlar. Bu çalışma, böbrek kanseri hücrelerinin bu şeker bağımlılığına dayanmasını, daha hızlı büyümesini ve daha saldırgan hale gelmesini sağlayan gizli bir moleküler devreyi ortaya koyuyor—ayrıca hekimlerin tümörün enerji kaynağını kesebileceği veya hangi hastaların daha kötü sonuçlarla karşılaşacağını daha iyi öngörebileceği yeni yaklaşımlara işaret ediyor.
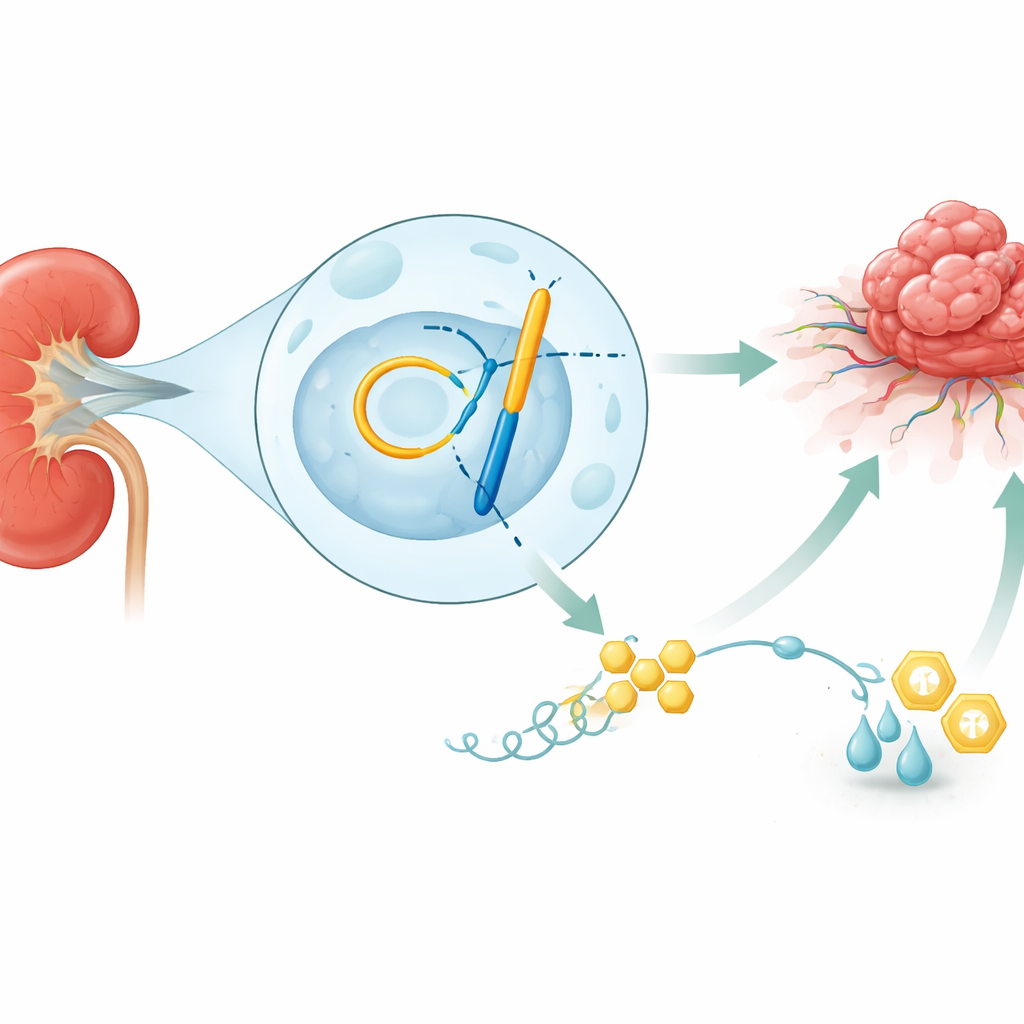
Şekeri Seven Bir Kanser
Böbreklerimiz gece gündüz sessizce kanı filtreler, ancak böbrek hücreli karsinom geliştiğinde bu hücrelerin bazıları şekerle beslenen fabrikalara dönüşür. Enerji üretmek için verimli, oksijene bağımlı yolu kullanmak yerine glukozu laktata çeviren hızlı ve daha az verimli yolu tercih ederler. Bu "turbo mod" yalnızca hızlı büyümeyi sürdürecek yakıt ve yapı taşlarını sağlamaz; aynı zamanda çevreyi asitleştirir ve yakınlardaki bağışıklık hücrelerini zayıflatır. Çalışma, bu hızlanmış metabolizmaya sahip böbrek tümörlerinin genellikle daha invaziv, tedaviye daha dirençli ve hasta sağkalımı açısından daha kötüye bağlı olduğunu gösteriyor; bu da bu metabolik anahtarın ne zaman ve nasıl açıldığını anlamanın neden hayati olduğunu vurguluyor.
Sahneye Çıkan Dairesel Bir Molekül
Araştırmacılar, böbrek kanseri hücreleri glukozdan yoksun bırakıldığında değişen alışılmadık RNA moleküllerini aradılar. Öne çıkan bir tanesini keşfettiler: circIQGAP1 adındaki dairesel RNA. Tipik lineer RNA’dan farklı olarak bu molekül kapalı bir halka oluşturur ve hücrede çok daha kararlı olur. Düşük şeker stresinde, U2AF2 adlı bir splicing proteininin üretimini artırmasıyla kanser hücreleri circIQGAP1’i yükseltir. Laboratuvar testleri, ekstra circIQGAP1’in böbrek kanseri hücrelerinin daha hızlı bölünmesine, daha kolay hareket etmesine, çevre dokuya daha fazla invaze olmasına ve önemlisi glikolitik—yani şeker yakma—aktivitesini artırmasına neden olduğunu gösterdi. circIQGAP1 susturulduğunda hücreler daha az laktat ve ATP üretti, büyümeleri yavaşladı ve ölme olasılıkları arttı; glikoliz engellendiğinde ise circIQGAP1’in tümörü teşvik edici etkisinin büyük kısmı ortadan kayboldu.
Anahtarı Stabilize Eden Bir Protein Koruyucu
Daha derine inildiğinde, ekip bu dairesel RNA’nın kanser metabolizmasını nasıl yeniden şekillendirdiğini sordu. circIQGAP1’in CARM1 adındaki bir protein enzime fiziksel olarak bağlandığı bulundu; CARM1 diğer proteinleri değiştirerek hangi genlerin aktif olduğuna etki etmesiyle bilinir. Normalde CARM1, yok edilmesini işaretleyen moleküler “etiketlerle” işaretlenir. circIQGAP1 bu etiketlerden birinin CARM1’e bağlanmasını engelleyerek bir kalkan görevi görür. Sonuç olarak CARM1 hücrede daha uzun süre kalır ve birikir. Bu stabilize olmuş CARM1 böbrek kanseri hastalarında kötü sağkalımla güçlü şekilde ilişkilendirildi ve araştırmacılar CARM1 düzeylerini azalttıklarında circIQGAP1’in tetiklediği büyüme ve glikolitik sıçramayı zayıflatabildiler; bu da dairesel RNA ile enzimin birlikte işleyen bir fonksiyonel birim olduğunu gösteriyor.
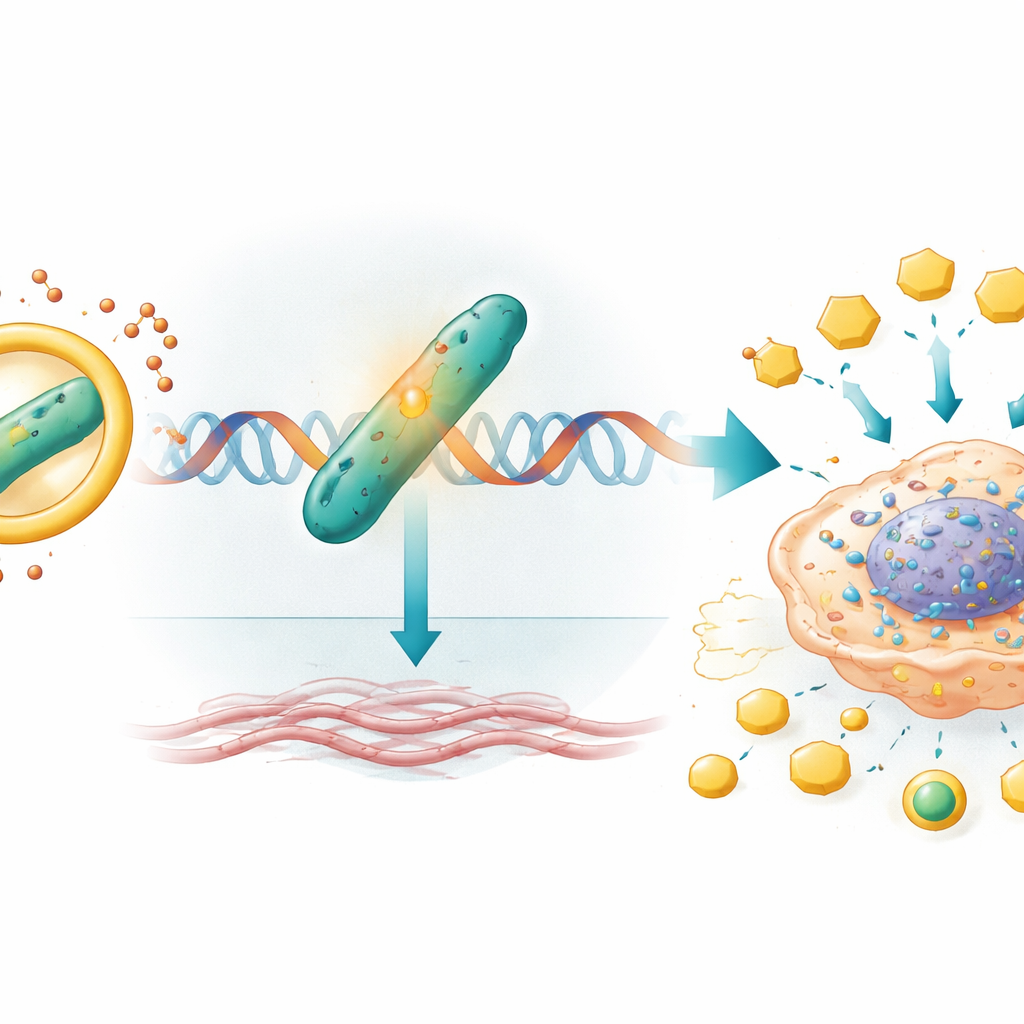
Gen Anahtarlarından Sertleşmiş Bir Tümör Ortamına
circIQGAP1 tarafından korunduktan sonra CARM1 hücrenin genetik materyaline gider ve COL5A1 adlı bir genin aktivitesini artırır. Bu gen kolajenin bir bileşenini kodlar; kolajen tümör çevresindeki iskeletin oluşmasına yardımcı olan yapısal bir proteindir. CARM1, COL5A1 anahtarının yakınındaki histonları kimyasal olarak değiştirerek (DNA’yı paketleyen proteinler) o genin okunmasını kolaylaştırır ve daha aktif transkripsiyon sağlar. Yüksek COL5A1 seviyeleri daha sert, daha invaziv tümörlerle ilişkilendirilir ve böbrek kanseri ile diğer malignitelerde daha kötü sonuçlarla bağdaştırılmıştır. Bu çalışmada COL5A1 kapatıldığında laktat ve ATP üretimi azaldı ve circIQGAP1 ile CARM1’in sağladığı glikoliz, büyüme, göç ve invazyon artışı tamamen ortadan kalktı; bu da COL5A1’i bu metabolik yeniden programlamanın önemli bir aşağı akış sürücüsü olarak işaretliyor.
Hastalar İçin Anlamı
Araştırmacılar yüksek circIQGAP1’e sahip böbrek kanseri hücrelerini farelere naklettiklerinde hayvanlarda CARM1, COL5A1 ve bir proliferasyon belirteci açısından zengin, daha büyük ve daha hızlı büyüyen tümörler gelişti. İnsan böbrek hücreli karsinomlu hastalarda da kanda daha yüksek circIQGAP1 seviyeleri görüldü ve bu dairesel RNA daha fazla olanların hayatta kalma süresi genellikle daha kötüydu. Bulgular birlikte açık bir olay zincirini özetliyor: U2AF2 circIQGAP1’i artırıyor, circIQGAP1 CARM1’i stabilize ediyor, CARM1 COL5A1’i açıyor ve bu üçlü böbrek kanseri hücrelerini şekerle beslenen, agresif bir duruma itiyor. Bu eksendeki her adım teoride hedef alınabilir—RNA tabanlı yaklaşımlar, enzim inhibitörleri veya kolajen yeniden düzenlemesini bozan ilaçlarla—dolayısıyla bu çalışma glukoz metabolizmasında değişikliklere dayanan böbrek kanserlerini izlemek ve tedavi etmek için yeni stratejilere işaret ediyor.
Atıf: Jia, R., Zou, B., Liang, Y. et al. CircIQGAP1-CARM1 axis promotes renal cell carcinoma progression through glycolytic reprogramming. Cell Death Dis 17, 414 (2026). https://doi.org/10.1038/s41419-026-08661-w
Anahtar kelimeler: böbrek hücreli karsinom, kanser metabolizması, dairesel RNA, CARM1, glikoliz