Clear Sky Science · de
CircIQGAP1-CARM1-Achse fördert das Fortschreiten von Nierenzellkarzinom durch glykolytische Umprogrammierung
Warum die Zucker-Vorliebe von Nierenkrebs wichtig ist
Nierenkrebs, insbesondere der häufige Klarzellig-Typ, nimmt weltweit zu und bleibt oft unbemerkt, bis er bereits gestreut hat. Wie viele Tumoren verändern diese Krebszellen ihre Nutzung von Zucker und verbrennen Glukose in hohem Tempo, selbst wenn ausreichend Sauerstoff vorhanden ist. Diese Studie enthüllt einen verborgenen molekularen Kreislauf, der es Nierenkrebszellen ermöglicht, sich an diese Zuckerabhängigkeit anzulehnen, schneller zu wachsen und aggressiver zu werden — und sie deutet auf neue Ansätze hin, mit denen Ärztinnen und Ärzte dem Tumor die Energie abschneiden oder besser vorhersagen könnten, welche Patientinnen und Patienten schlechtere Aussichten haben.
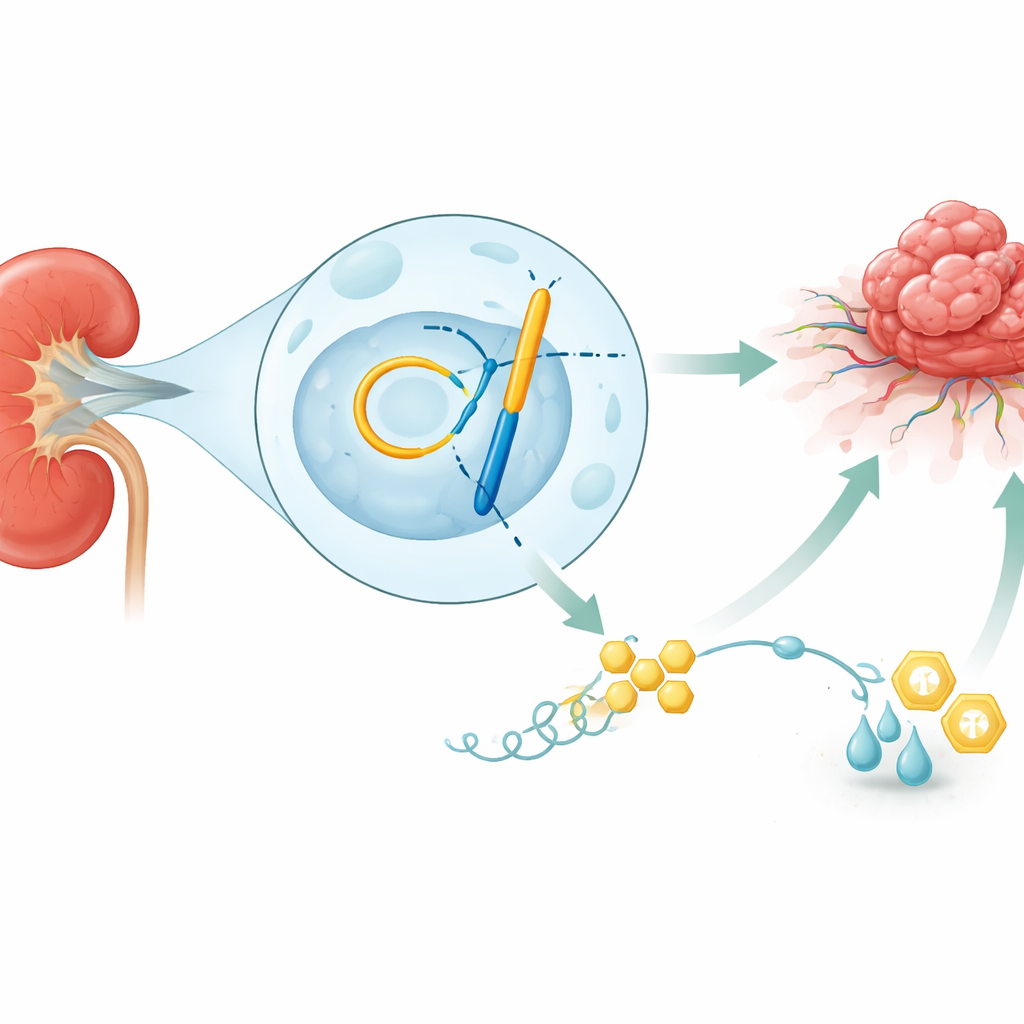
Ein Krebs, der Zucker liebt
Unsere Nieren filtern kontinuierlich Blut, doch wenn sich ein Nierenzellkarzinom entwickelt, verwandeln sich einige dieser Zellen in zuckerhungrige Fabriken. Anstatt den effizienten, sauerstoffabhängigen Weg zur Energiegewinnung zu nutzen, bevorzugen sie einen schnellen, weniger sauberen Weg, der Glukose in Laktat umwandelt. Dieser „Turbolader“-Modus liefert nicht nur ausreichend Brennstoff und Bausteine für schnelles Wachstum, er säuert auch die Umgebung an und schwächt benachbarte Immunzellen. Die Studie zeigt, dass Nierentumoren mit diesem hochgefahrenen Stoffwechsel tendenziell invasiver, therapieresistenter und mit schlechterer Patientenüberlebensrate verbunden sind, was unterstreicht, warum es entscheidend ist zu verstehen, was diesen Stoffwechsel-Schalter umlegt.
Ein zirkuläres Molekül rückt ins Rampenlicht
Die Forschenden suchten nach ungewöhnlichen RNA-Molekülen, die sich verändern, wenn Nierenkrebszellen Glukose entzogen wird. Sie entdeckten einen auffälligen Kandidaten: eine zirkuläre RNA namens circIQGAP1. Im Gegensatz zu typischen linearen RNAs bildet dieses Molekül eine geschlossene Schleife, was es in Zellen sehr stabil macht. Unter niedrigem Zuckerstress erhöhen Krebszellen die Produktion von circIQGAP1, unterstützt durch ein Spleißprotein namens U2AF2, das seine Entstehung fördert. Labortests zeigten, dass zusätzliches circIQGAP1 Nierenkrebszellen schneller teilen, sich leichter bewegen, umliegendes Gewebe invasieren und vor allem ihre glykolytische — also zuckerverbrennende — Aktivität steigern lässt. Wurde circIQGAP1 stillgelegt, produzierten die Zellen weniger Laktat und ATP, verlangsamten ihr Wachstum und starben eher; das Blockieren der Glykolyse nahm circIQGAP1 zudem einen Großteil seiner tumorfördernden Wirkung.
Ein Proteinwächter, der einen wichtigen Schalter stabilisiert
Bei tiefergehenden Untersuchungen fragten die Forschenden, wie diese zirkuläre RNA den Krebsstoffwechsel umgestaltet. Sie fanden heraus, dass circIQGAP1 physisch an ein Protein-Enzym namens CARM1 bindet, das dafür bekannt ist, andere Proteine zu modifizieren und so die Genaktivität zu verändern. Normalerweise wird CARM1 mit molekularen „Markierungen“ versehen, die seinen Abbau signalisieren. CircIQGAP1 wirkt wie ein Schutzschild und verhindert, dass eine bestimmte Art dieser Abbausmarkierung an CARM1 angeheftet wird. Folglich verweilt CARM1 länger und häuft sich in der Zelle an. Dieses stabilisierte CARM1 ist stark mit schlechterem Überleben bei Nierenkrebspatienten verknüpft; reduzierten die Forschenden CARM1, konnte das durch circIQGAP1 angetriebene Wachstum und die glykolytische Steigerung abgeschwächt werden, sodass die zirkuläre RNA und das Enzym zusammen als funktionale Einheit agieren.
Von Gen‑Schaltern zu einer verfestigten Tumorumgebung
Einmal von circIQGAP1 geschützt, wandert CARM1 zum genetischen Material der Zelle und erhöht die Aktivität eines Gens namens COL5A1. Dieses Gen kodiert einen Bestandteil von Kollagen, einem Strukturprotein, das am Aufbau des umgebenden Tumorsgerüsts beteiligt ist. CARM1 modifiziert chemisch Histone — Proteine, die DNA verpacken — in der Nähe des COL5A1‑Schalters, wodurch dieses Gen leichter zugänglich und aktiver transkribiert wird. Höhere COL5A1‑Spiegel sind mit festeren, invasiveren Tumoren verbunden und wurden bei Nierenkrebs und anderen Malignomen mit schlechteren Ergebnissen assoziiert. In dieser Studie verringerte das Ausschalten von COL5A1 die Laktat‑ und ATP‑Produktion und löschte vollständig die Steigerung von Glykolyse, Wachstum, Migration und Invasion, die circIQGAP1 und CARM1 üblicherweise vermitteln, womit COL5A1 als entscheidender nachgeschalteter Treiber dieser metabolischen Umprogrammierung markiert ist.
Was das für Patientinnen und Patienten bedeutet
Als die Forschenden Nierenkrebszellen mit hohem circIQGAP1 in Mäuse implantierten, entwickelten die Tiere größere, schneller wachsende Tumoren mit reichlich CARM1, COL5A1 und einem Proliferationsmarker. Auch bei Menschen mit Nierenzellkarzinom fanden sich erhöhte circIQGAP1‑Spiegel im Blut, und diejenigen mit mehr dieser zirkulären RNA hatten tendenziell ein schlechteres Überleben. Zusammen zeichnen die Ergebnisse eine klare Ereigniskette: U2AF2 fördert circIQGAP1, circIQGAP1 stabilisiert CARM1, CARM1 schaltet COL5A1 ein, und dieses Trio treibt Nierenkrebszellen in einen zuckergetriebenen, aggressiven Zustand. Da jeder Schritt dieser Achse prinzipiell angreifbar ist — etwa mit RNA‑basierten Ansätzen, Enzyminhibitoren oder Wirkstoffen, die die Kollagen‑Umgestaltung stören — weist diese Arbeit auf neue Strategien hin, um Nierenkrebserkrankungen zu überwachen und zu behandeln, die stark auf veränderten Glukosestoffwechsel angewiesen sind.
Zitation: Jia, R., Zou, B., Liang, Y. et al. CircIQGAP1-CARM1 axis promotes renal cell carcinoma progression through glycolytic reprogramming. Cell Death Dis 17, 414 (2026). https://doi.org/10.1038/s41419-026-08661-w
Schlüsselwörter: Nierenzellkarzinom, Krebsstoffwechsel, zirkuläre RNA, CARM1, Glykolyse