Clear Sky Science · pt
Eixo CircIQGAP1-CARM1 promove progressão do carcinoma de células renais por meio do reprogramamento glicolítico
Por que o hábito de consumir açúcar pelo câncer renal importa
O câncer renal, especialmente o tipo claro mais comum, está aumentando em todo o mundo e muitas vezes passa despercebido até já ter se espalhado. Como muitos tumores, esses cânceres reprogramam o uso de açúcar, queimando glicose em alta velocidade mesmo quando há oxigênio disponível. Este trabalho revela um circuito molecular oculto que permite às células do câncer renal se apoiarem nessa dependência de açúcar, crescerem mais rápido e se tornarem mais agressivas — e sugere novas maneiras de os médicos cortarem o fornecimento de energia do tumor ou preverem melhor quais pacientes terão um prognóstico pior.
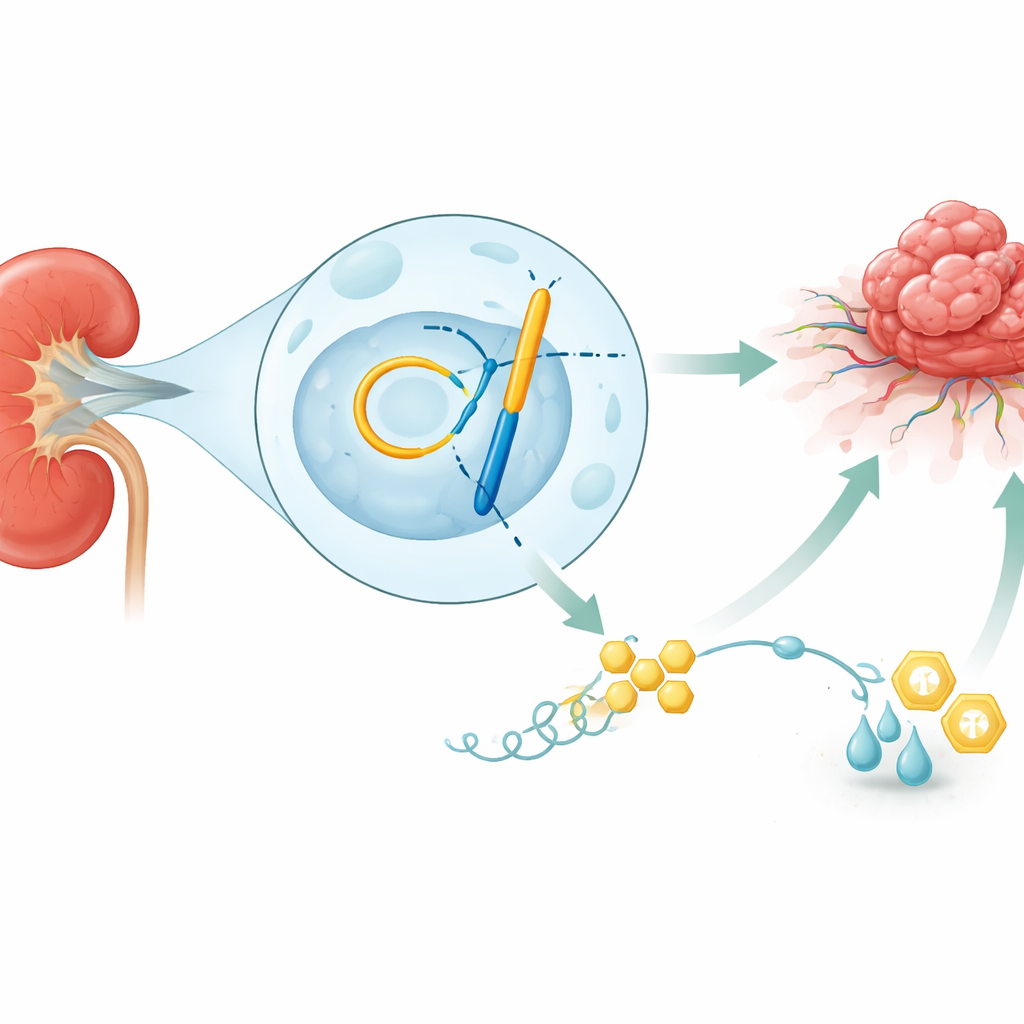
Um câncer que adora açúcar
Os rins filtram o sangue silenciosamente o tempo todo, mas quando surge o carcinoma de células renais, algumas dessas células se transformam em fábricas famintas por açúcar. Em vez de usar a via eficiente e dependente de oxigênio para gerar energia, elas preferem uma rota rápida e menos eficiente que converte glicose em lactato. Esse “modo turbo” não apenas fornece combustível e blocos de construção suficientes para sustentar o crescimento rápido, como também acidifica o ambiente e enfraquece células imunes próximas. O estudo mostra que tumores renais com esse metabolismo acelerado tendem a ser mais invasivos, mais resistentes ao tratamento e associados a piores taxas de sobrevivência, o que reforça por que é vital entender o que aciona esse interruptor metabólico.
Uma molécula circular assume o centro do palco
Os pesquisadores procuraram por moléculas de RNA incomuns que mudam quando células de câncer renal ficam sem glicose. Eles descobriram um destaque: um RNA circular chamado circIQGAP1. Ao contrário do RNA linear típico, essa molécula forma um loop fechado, tornando-se altamente estável nas células. Sob estresse por baixo nível de açúcar, as células cancerosas aumentam a produção de circIQGAP1, com a ajuda de uma proteína de splicing chamada U2AF2 que impulsiona sua formação. Testes em laboratório mostraram que a presença extra de circIQGAP1 faz com que células de câncer renal se dividam mais rápido, se movam com mais facilidade, invadam tecidos ao redor e, crucialmente, aumentem sua atividade glicolítica — ou seja, queima de açúcar. Quando o circIQGAP1 foi silenciado, as células produziram menos lactato e ATP, seu crescimento desacelerou e ficaram mais propensas a morrer; e bloquear a glicólise apagou grande parte do poder tumoral promovido pelo circIQGAP1.
Um guardião proteico que estabiliza um interruptor chave
Ao aprofundar a investigação, a equipe perguntou como esse RNA circular remodela o metabolismo do câncer. Eles descobriram que o circIQGAP1 se liga fisicamente a uma enzima proteica chamada CARM1, conhecida por modificar outras proteínas e alterar quais genes são ativados. Normalmente, a CARM1 é marcada com “sinais” moleculares que indicam sua degradação. O circIQGAP1 atua como um escudo, impedindo que um tipo específico de etiqueta de degradação se prenda à CARM1. Como resultado, a CARM1 persiste por mais tempo e se acumula dentro da célula. Essa CARM1 estabilizada está fortemente associada a pior sobrevida em pacientes com câncer renal, e quando os pesquisadores reduziram os níveis de CARM1, conseguiram atenuar o crescimento e o surto glicolítico conduzidos pelo circIQGAP1, mostrando que o RNA circular e a enzima atuam juntos como uma unidade funcional.
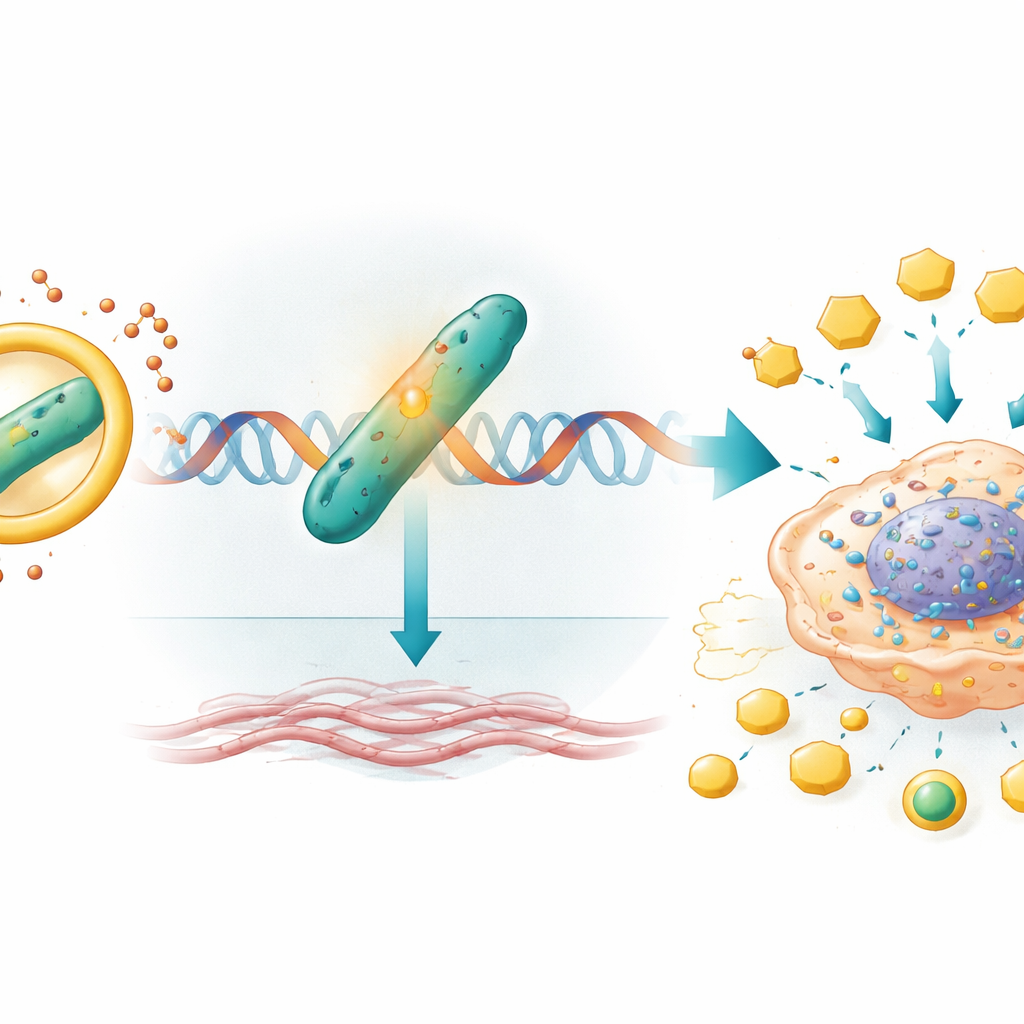
De interruptores gênicos a um ambiente tumoral endurecido
Uma vez protegida pelo circIQGAP1, a CARM1 viaja até o material genético da célula e aumenta a atividade de um gene chamado COL5A1. Esse gene codifica um componente do colágeno, uma proteína estrutural que ajuda a formar a matriz que envolve o tumor. A CARM1 modifica quimicamente histonas — proteínas que compactam o DNA — próximas ao interruptor do COL5A1, tornando esse gene mais acessível e mais ativamente transcrito. Níveis maiores de COL5A1 estão ligados a tumores mais rígidos e invasivos e têm sido associados a piores desfechos no câncer renal e em outras malignidades. Neste estudo, a inativação do COL5A1 reduziu a produção de lactato e ATP e apagou completamente o aumento da glicólise, do crescimento, da migração e da invasão que o circIQGAP1 e a CARM1 normalmente promovem, marcando o COL5A1 como um motor a jusante crucial desse reprogramamento metabólico.
O que isso significa para os pacientes
Quando os pesquisadores implantaram células de câncer renal com altos níveis de circIQGAP1 em camundongos, os animais desenvolveram tumores maiores e de crescimento mais rápido, ricos em CARM1, COL5A1 e um marcador de proliferação. Pacientes humanos com carcinoma de células renais também apresentaram níveis mais altos de circIQGAP1 no sangue, e aqueles com mais desse RNA circular tendiam a ter pior sobrevida. Em conjunto, as descobertas delineiam uma cadeia clara de eventos: U2AF2 aumenta o circIQGAP1, o circIQGAP1 estabiliza a CARM1, a CARM1 ativa o COL5A1, e esse trio empurra as células do câncer renal para um estado agressivo alimentado por glicose. Como cada etapa desse eixo pode, em princípio, ser alvo de intervenção — com abordagens baseadas em RNA, inibidores enzimáticos ou drogas que perturbam a remodelação do colágeno — este trabalho aponta para novas estratégias para monitorar e tratar cânceres renais que dependem fortemente do metabolismo de glicose alterado.
Citação: Jia, R., Zou, B., Liang, Y. et al. CircIQGAP1-CARM1 axis promotes renal cell carcinoma progression through glycolytic reprogramming. Cell Death Dis 17, 414 (2026). https://doi.org/10.1038/s41419-026-08661-w
Palavras-chave: carcinoma de células renais, metabolismo do câncer, RNA circular, CARM1, glicólise