Clear Sky Science · it
L’asse CircIQGAP1-CARM1 promuove la progressione del carcinoma renale attraverso il riprogrammamento glicolitico
Perché l’abitudine allo zucchero del cancro al rene è importante
Il cancro al rene, in particolare il tipo più comune a cellule chiare, è in aumento nel mondo e spesso viene scoperto solo dopo essersi già diffuso. Come molti tumori, queste neoplasie riorganizzano l’uso degli zuccheri, consumando glucosio a ritmo elevato anche quando l’ossigeno è abbondante. Questo lavoro svela un circuito molecolare nascosto che permette alle cellule del cancro renale di assecondare quella dipendenza dal glucosio, crescere più rapidamente e diventare più aggressive — e suggerisce nuovi modi in cui i medici potrebbero tagliare l’apporto energetico del tumore o prevedere meglio quali pazienti avranno esiti peggiori.
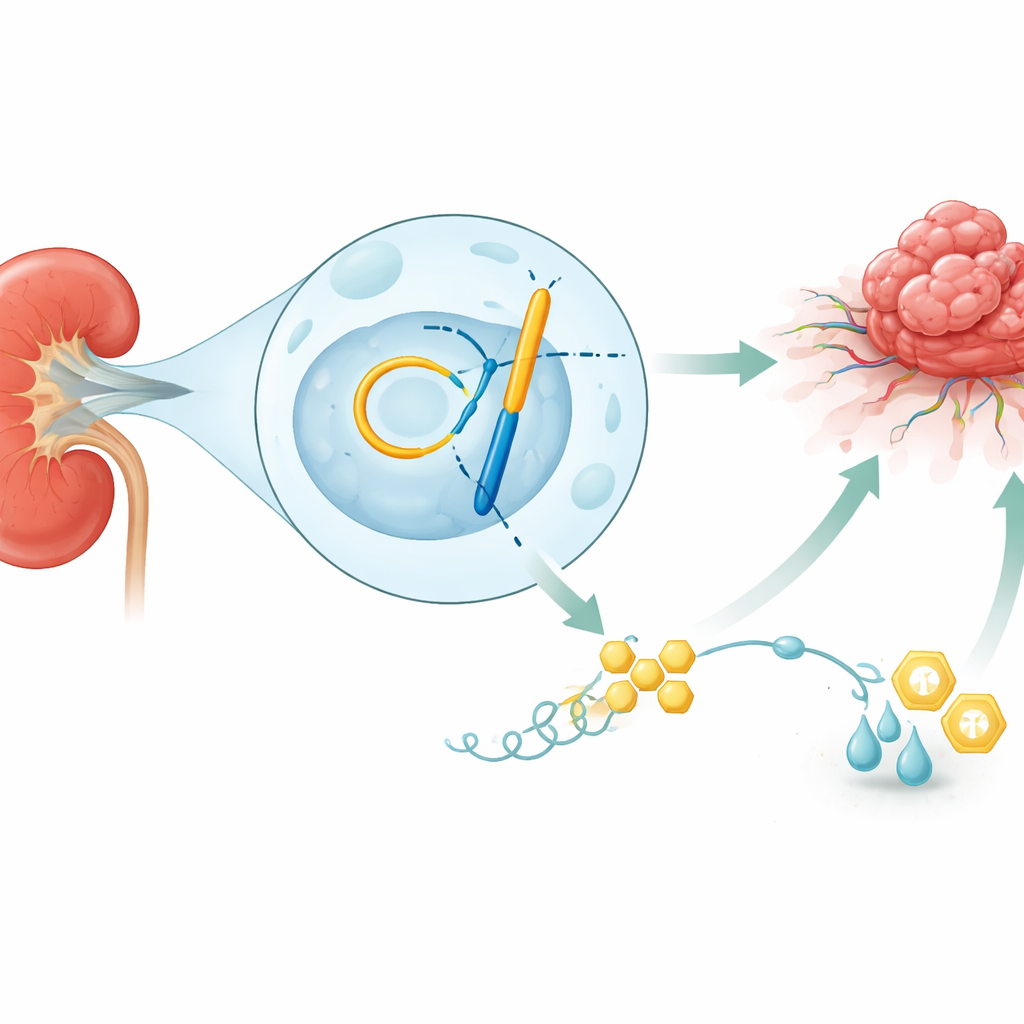
Un cancro che ama lo zucchero
I nostri reni filtrano il sangue senza sosta, ma quando si sviluppa un carcinoma renale alcune di quelle cellule si trasformano in fabbriche affamate di zucchero. Anziché usare la via efficiente e dipendente dall’ossigeno per produrre energia, preferiscono un percorso rapido e meno pulito che converte il glucosio in lattato. Questa «modalità turbo» non solo genera carburante e mattoni sufficienti a sostenere una crescita rapida, ma acidifica l’ambiente e indebolisce le cellule immunitarie vicine. Lo studio mostra che i tumori renali con questo metabolismo accelerato tendono a essere più invasivi, più resistenti alle terapie e associati a una sopravvivenza dei pazienti peggiore, sottolineando perché è fondamentale capire cosa aziona questo interruttore metabolico.
Una molecola circolare sotto i riflettori
I ricercatori hanno cercato RNA insoliti che cambiano quando le cellule del cancro renale sono private di glucosio. Hanno scoperto un protagonista: un RNA circolare chiamato circIQGAP1. A differenza degli RNA lineari tipici, questa molecola forma un anello chiuso, che la rende molto stabile nelle cellule. In condizioni di carenza di zuccheri, le cellule tumorali aumentano la produzione di circIQGAP1, con l’aiuto di una proteina di splicing chiamata U2AF2 che ne potenzia la biogenesi. Test di laboratorio hanno mostrato che un eccesso di circIQGAP1 fa sì che le cellule del carcinoma renale si dividano più rapidamente, migrino più facilmente, invadano i tessuti circostanti e, cosa cruciale, aumentino la loro attività glicolitica — cioè il consumo di zuccheri. Quando circIQGAP1 veniva silenziato, le cellule producevano meno lattato e ATP, rallentavano la crescita e tendevano a morire di più; e bloccare la glicolisi annullava gran parte del potere tumorale promuovente di circIQGAP1.
Una proteina guardiana che stabilizza un interruttore chiave
Approfondendo, il gruppo ha indagato come questo RNA circolare rimodelli il metabolismo tumorale. Hanno scoperto che circIQGAP1 si lega fisicamente a un enzima proteico chiamato CARM1, noto per modificare altre proteine e alterare l’attività genica. Normalmente, CARM1 viene marcato da «segnali» molecolari che ne indicano la degradazione. CircIQGAP1 agisce come uno scudo, impedendo l’attacco di un tipo specifico di tag di degradazione su CARM1. Di conseguenza, CARM1 persiste più a lungo e si accumula nella cellula. Questo CARM1 stabilizzato è fortemente associato a una sopravvivenza peggiore nei pazienti con carcinoma renale, e quando i ricercatori riducevano i livelli di CARM1 riuscivano ad attenuare la crescita e la spinta glicolitica indotte da circIQGAP1, dimostrando che l’RNA circolare e l’enzima agiscono insieme come un’unità funzionale.
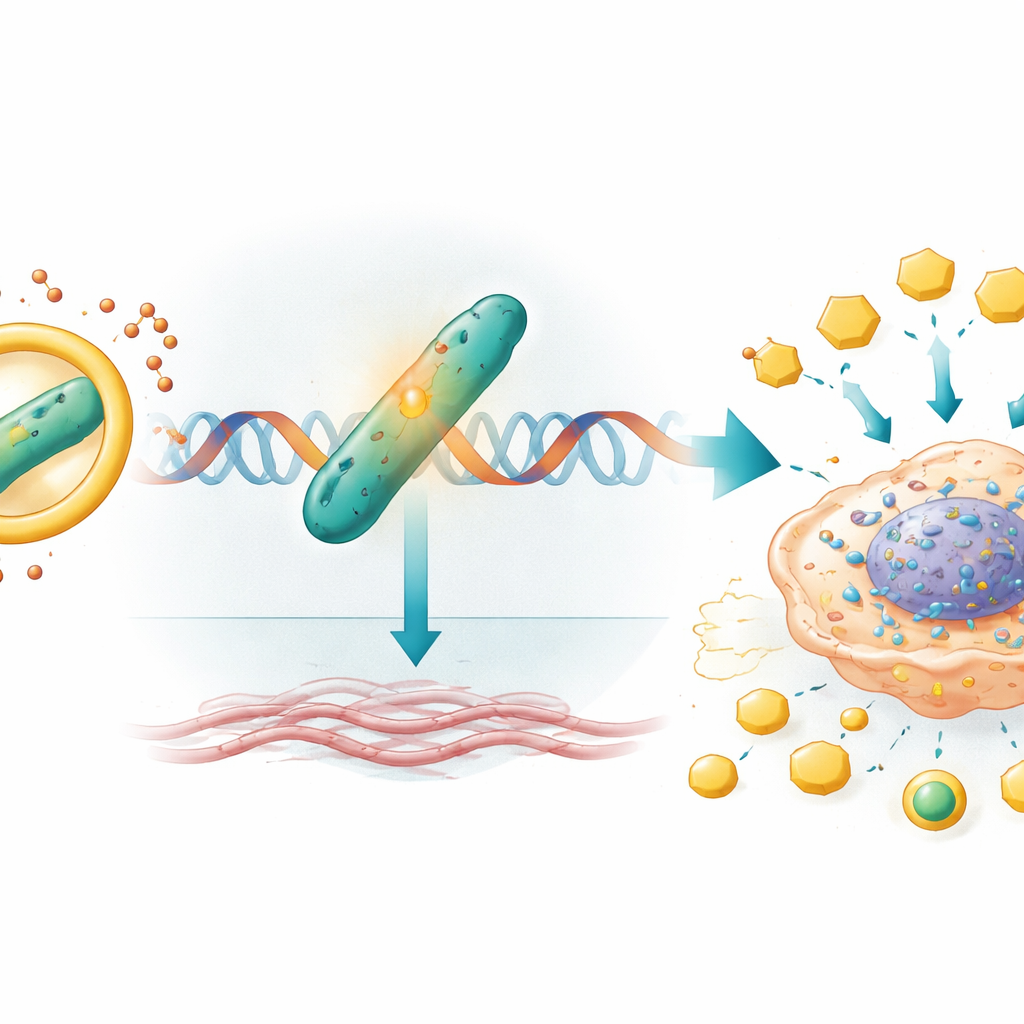
Dagli interruttori genici a un microambiente tumorale irrigidito
Una volta protetto da circIQGAP1, CARM1 si sposta nel materiale genetico della cellula e aumenta l’attività di un gene chiamato COL5A1. Questo gene codifica per un componente del collagene, una proteina strutturale che contribuisce a formare l’impalcatura intorno al tumore. CARM1 modifica chimicamente le istoni — le proteine che compattano il DNA — vicino all’interruttore di COL5A1, rendendo quel gene più accessibile e più attivamente trascritto. Livelli più alti di COL5A1 sono legati a tumori più rigidi e invasivi e sono stati associati a esiti peggiori nel carcinoma renale e in altre neoplasie. In questo studio, spegnere COL5A1 riduceva la produzione di lattato e ATP e annullava completamente l’aumento di glicolisi, crescita, migrazione e invasione che circIQGAP1 e CARM1 normalmente promuovono, indicando COL5A1 come un importante effettore a valle di questo riprogrammamento metabolico.
Cosa significa questo per i pazienti
Quando i ricercatori impiantarono cellule di carcinoma renale con alti livelli di circIQGAP1 nei topi, gli animali svilupparono tumori più grandi e più rapidi, ricchi di CARM1, COL5A1 e di un marcatore di proliferazione. I pazienti umani con carcinoma renale mostravano anch’essi livelli più elevati di circIQGAP1 nel sangue, e chi presentava maggiori quantità di questo RNA circolare tendeva ad avere una sopravvivenza peggiore. Complessivamente, i risultati delineano una catena chiara di eventi: U2AF2 aumenta circIQGAP1, circIQGAP1 stabilizza CARM1, CARM1 attiva COL5A1, e questo trio spinge le cellule del cancro renale verso uno stato aggressivo alimentato dallo zucchero. Poiché ogni passaggio di questo asse è, in linea di principio, bersagliabile — con approcci basati su RNA, inibitori enzimatici o farmaci che interferiscono con il rimodellamento del collagene — questo lavoro indica nuove strategie per monitorare e trattare i carcinomi renali che fanno affidamento su un metabolismo del glucosio alterato.
Citazione: Jia, R., Zou, B., Liang, Y. et al. CircIQGAP1-CARM1 axis promotes renal cell carcinoma progression through glycolytic reprogramming. Cell Death Dis 17, 414 (2026). https://doi.org/10.1038/s41419-026-08661-w
Parole chiave: carcinoma renale, metabolismo del cancro, RNA circolare, CARM1, glicolisi