Clear Sky Science · es
El eje CircIQGAP1-CARM1 promueve la progresión del carcinoma renal mediante la reprogramación glucolítica
Por qué importa la afición del cáncer renal por el azúcar
El cáncer de riñón, especialmente el tipo más frecuente de células claras, aumenta en todo el mundo y con frecuencia pasa desapercibido hasta que ya se ha diseminado. Como muchos tumores, estas neoplasias reprograman su uso de la glucosa, consumiéndola a gran velocidad incluso cuando hay oxígeno disponible. Este trabajo desvela un circuito molecular oculto que permite a las células de cáncer renal aprovechar esa adicción al azúcar, crecer más rápido y volverse más agresivas, y sugiere nuevas maneras en que los médicos podrían cortar el suministro energético del tumor o predecir mejor qué pacientes tienen peor pronóstico.
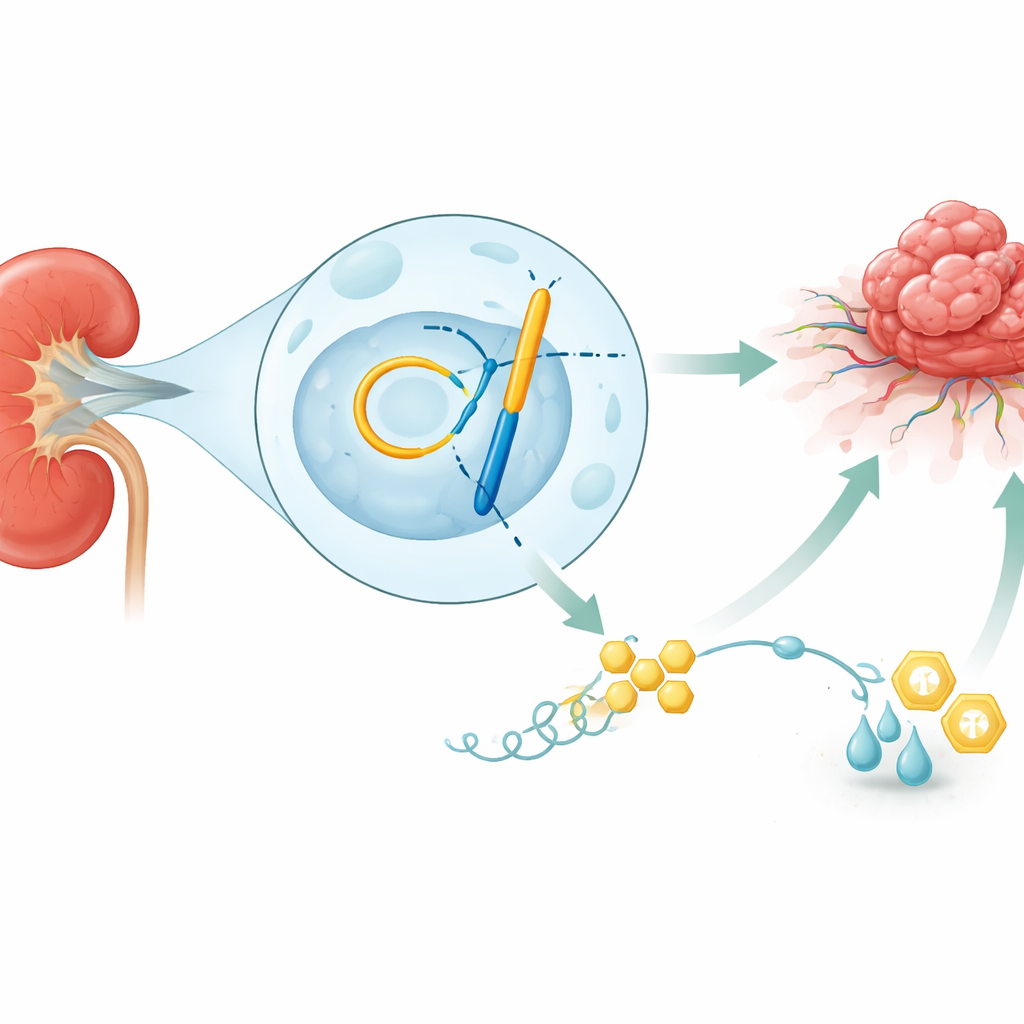
Un cáncer que ama el azúcar
Los riñones filtran la sangre de forma continua, pero cuando se desarrolla un carcinoma renal, algunas de esas células se convierten en fábricas hambrientas de azúcar. En vez de usar la vía eficiente dependiente de oxígeno para generar energía, prefieren una ruta rápida y menos eficiente que convierte la glucosa en lactato. Este “modo turbo” no solo produce suficiente combustible y bloques de construcción para sostener un crecimiento rápido, sino que también acidifica el entorno y debilita a las células inmunitarias cercanas. El estudio muestra que los tumores renales con este metabolismo intensificado tienden a ser más invasivos, más resistentes al tratamiento y están asociados a una supervivencia peor, lo que subraya la importancia de entender qué activa este interruptor metabólico.
Una molécula circular entra en escena
Los investigadores buscaron moléculas de ARN inusuales que cambian cuando las células de cáncer renal se quedan sin glucosa. Descubrieron una destacada: un ARN circular llamado circIQGAP1. A diferencia del ARN lineal típico, esta molécula forma un lazo cerrado, lo que la hace altamente estable en las células. Bajo estrés por baja disponibilidad de azúcar, las células cancerosas incrementan circIQGAP1, con la ayuda de una proteína de empalme llamada U2AF2 que potencia su producción. Pruebas de laboratorio mostraron que un exceso de circIQGAP1 hace que las células de carcinoma renal se dividan más rápido, se desplacen con mayor facilidad, invadan tejidos circundantes y, crucialmente, aumenten su actividad glucolítica —es decir, su consumo de azúcar—. Cuando se silenció circIQGAP1, las células produjeron menos lactato y ATP, disminuyeron su crecimiento y tuvieron más probabilidad de morir; además, bloquear la glucólisis eliminó gran parte del poder tumorigénico de circIQGAP1.
Un guardián proteico que estabiliza un interruptor clave
Al profundizar, el equipo se preguntó cómo este ARN circular remodela el metabolismo canceroso. Encontraron que circIQGAP1 se une físicamente a una enzima proteica llamada CARM1, conocida por modificar otras proteínas y alterar qué genes se activan. Normalmente, CARM1 recibe “marcas” moleculares que señalan su destrucción. CircIQGAP1 actúa como un escudo, impidiendo que un tipo específico de etiqueta de degradación se adhiera a CARM1. Como resultado, CARM1 permanece más tiempo y se acumula dentro de la célula. Esta CARM1 estabilizada se asocia fuertemente con una peor supervivencia en pacientes con cáncer renal, y cuando los investigadores redujeron los niveles de CARM1 pudieron atenuar el crecimiento y el aumento glucolítico impulsado por circIQGAP1, demostrando que el ARN circular y la enzima actúan juntos como una unidad funcional.
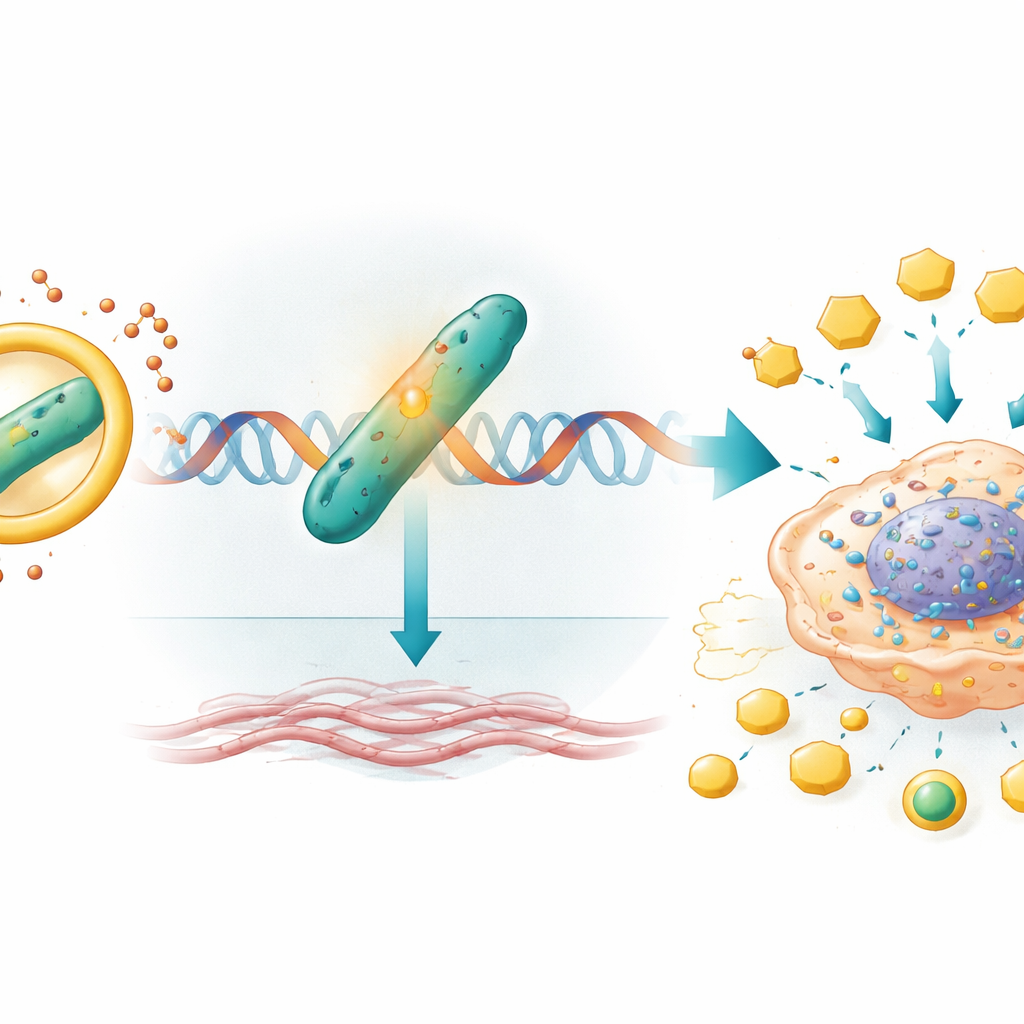
De los interruptores génicos a un entorno tumoral endurecido
Una vez protegido por circIQGAP1, CARM1 viaja al material genético de la célula y aumenta la actividad de un gen llamado COL5A1. Este gen codifica un componente del colágeno, una proteína estructural que ayuda a formar el andamiaje que rodea el tumor. CARM1 modifica químicamente las histonas —proteínas que empaquetan el ADN— cerca del interruptor de COL5A1, facilitando la lectura y la transcripción activa de ese gen. Niveles más altos de COL5A1 están vinculados a tumores más rígidos y agresivos y se han asociado con peores resultados en el cáncer renal y otras malignidades. En este estudio, desactivar COL5A1 redujo la producción de lactato y ATP y eliminó por completo el impulso en glucólisis, crecimiento, migración e invasión que normalmente proporcionan circIQGAP1 y CARM1, señalando a COL5A1 como un impulsor descendente crucial de esta reprogramación metabólica.
Qué significa esto para los pacientes
Cuando los investigadores implantaron células de carcinoma renal con altos niveles de circIQGAP1 en ratones, los animales desarrollaron tumores más grandes y de crecimiento más rápido, ricos en CARM1, COL5A1 y un marcador de proliferación. Pacientes humanos con carcinoma renal también mostraron niveles más altos de circIQGAP1 en sangre, y aquellos con mayor cantidad de este ARN circular tendieron a tener una supervivencia peor. En conjunto, los hallazgos describen una cadena clara de eventos: U2AF2 potencia circIQGAP1, circIQGAP1 estabiliza CARM1, CARM1 activa COL5A1, y este trío empuja a las células de carcinoma renal hacia un estado agresivo y alimentado por glucosa. Dado que cada paso de este eje puede, en principio, ser diana terapéutica —con enfoques basados en ARN, inhibidores enzimáticos o fármacos que alteren la remodelación del colágeno—, este trabajo apunta a nuevas estrategias para monitorizar y tratar los cánceres renales que dependen en gran medida de la alteración del metabolismo de la glucosa.
Cita: Jia, R., Zou, B., Liang, Y. et al. CircIQGAP1-CARM1 axis promotes renal cell carcinoma progression through glycolytic reprogramming. Cell Death Dis 17, 414 (2026). https://doi.org/10.1038/s41419-026-08661-w
Palabras clave: carcinoma renal, metabolismo del cáncer, ARN circular, CARM1, glucólisis