Clear Sky Science · fr
L’axe CircIQGAP1-CARM1 favorise la progression du carcinome rénal via un reprogrammation glycolytique
Pourquoi l’appétit sucré du cancer du rein compte
Le cancer du rein, en particulier le type fréquent à cellules claires, augmente dans le monde et reste souvent indétecté jusqu’à diffusion. Comme de nombreuses tumeurs, ces cancers réorientent leur utilisation du glucose, brûlant le sucre à grande vitesse même en présence d’oxygène. Ce travail met au jour un circuit moléculaire caché qui permet aux cellules du cancer rénal d’exploiter cette dépendance au sucre, de croître plus vite et de devenir plus agressives — et suggère de nouvelles approches pour couper l’approvisionnement énergétique de la tumeur ou mieux prédire quels patients risquent un mauvais pronostic.
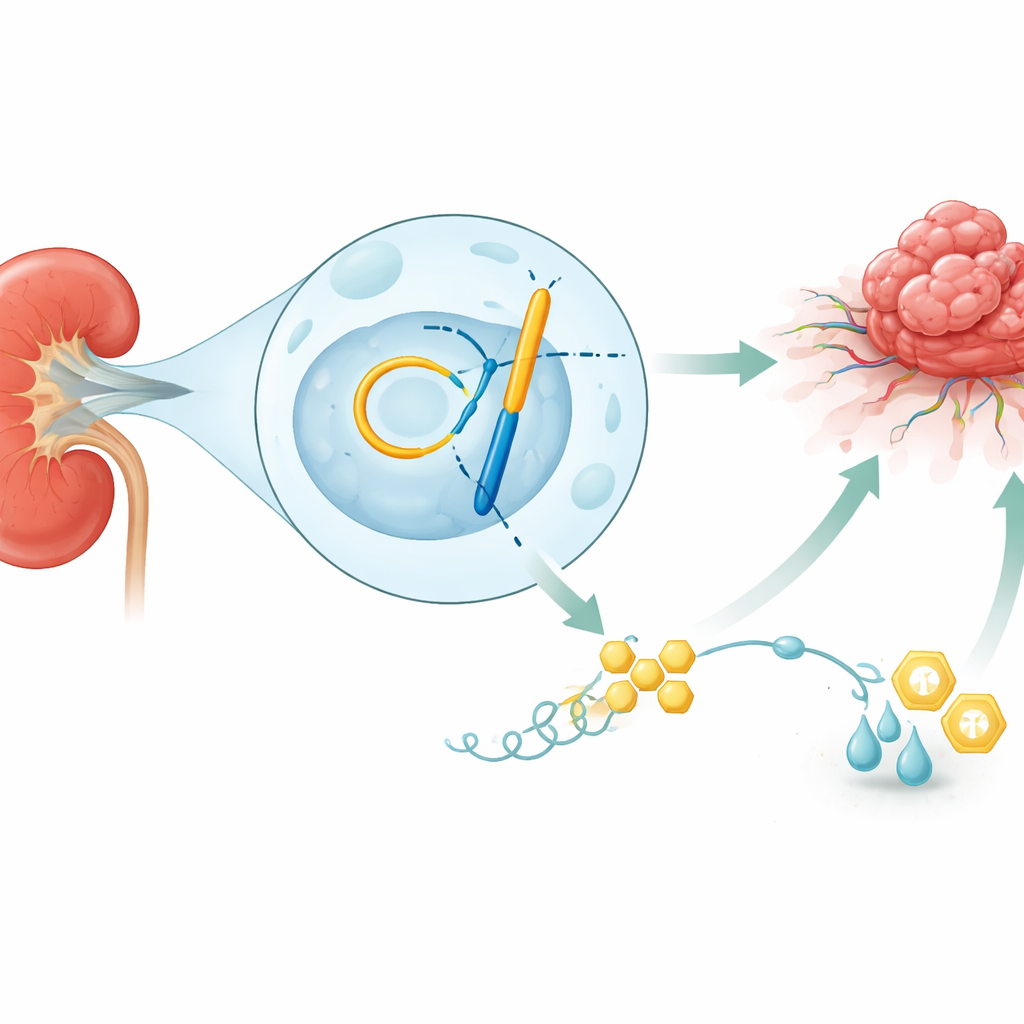
Un cancer qui aime le sucre
Nos reins filtrent silencieusement le sang en permanence, mais lorsque le carcinome rénal se développe, certaines cellules deviennent des usines avides de sucre. Plutôt que d’emprunter la voie efficace dépendante de l’oxygène pour produire de l’énergie, elles privilégient une filière rapide et peu exigeante qui convertit le glucose en lactate. Ce «mode turbo» fournit non seulement suffisamment de carburant et de briques pour soutenir une croissance rapide, il acidifie aussi l’environnement et affaiblit les cellules immunitaires voisines. L’étude montre que les tumeurs rénales présentant ce métabolisme amplifié tendent à être plus invasives, plus résistantes aux traitements et associées à une survie moindre des patients, ce qui souligne l’importance de comprendre ce qui déclenche cet interrupteur métabolique.
Une molécule circulaire sous les projecteurs
Les chercheurs ont cherché des ARN inhabituels qui changent quand les cellules cancéreuses rénales sont privées de glucose. Ils ont découvert un candidat remarquable : un ARN circulaire nommé circIQGAP1. À la différence des ARN linéaires habituels, cette molécule forme une boucle fermée, ce qui la rend très stable dans la cellule. En situation de stress lié au manque de sucre, les cellules cancéreuses augmentent la production de circIQGAP1, aidées par une protéine d’épissage appelée U2AF2 qui favorise sa génération. Des tests en laboratoire ont montré qu’un excès de circIQGAP1 rendait les cellules du cancer rénal plus prolifératives, plus mobiles, plus invasives et, surtout, augmentait leur activité glycolytique — c’est‑à‑dire leur consommation de sucre. Lorsque circIQGAP1 était silencieux, les cellules produisaient moins de lactate et d’ATP, leur croissance ralentissait et elles étaient plus enclines à mourir ; bloquer la glycolyse annulait une grande partie du pouvoir tumorigène de circIQGAP1.
Un gardien protéique qui stabilise un commutateur clé
En creusant plus loin, l’équipe a cherché comment cet ARN circulaire reconfigure le métabolisme tumoral. Ils ont découvert que circIQGAP1 se lie physiquement à une enzyme protéique appelée CARM1, connue pour modifier d’autres protéines et influencer l’expression génétique. Normalement, CARM1 est étiquetée par des marqueurs moléculaires signalant sa destruction. CircIQGAP1 agit comme un bouclier, empêchant l’ajout d’un type spécifique d’étiquette de dégradation sur CARM1. En conséquence, CARM1 persiste plus longtemps et s’accumule dans la cellule. Cette stabilisation de CARM1 s’associe fortement à une survie réduite chez les patients atteints de cancer du rein, et lorsque les chercheurs ont réduit le niveau de CARM1, ils ont pu atténuer la croissance et l’essor glycolytique induits par circIQGAP1, montrant que l’ARN circulaire et l’enzyme fonctionnent ensemble comme une unité fonctionnelle.
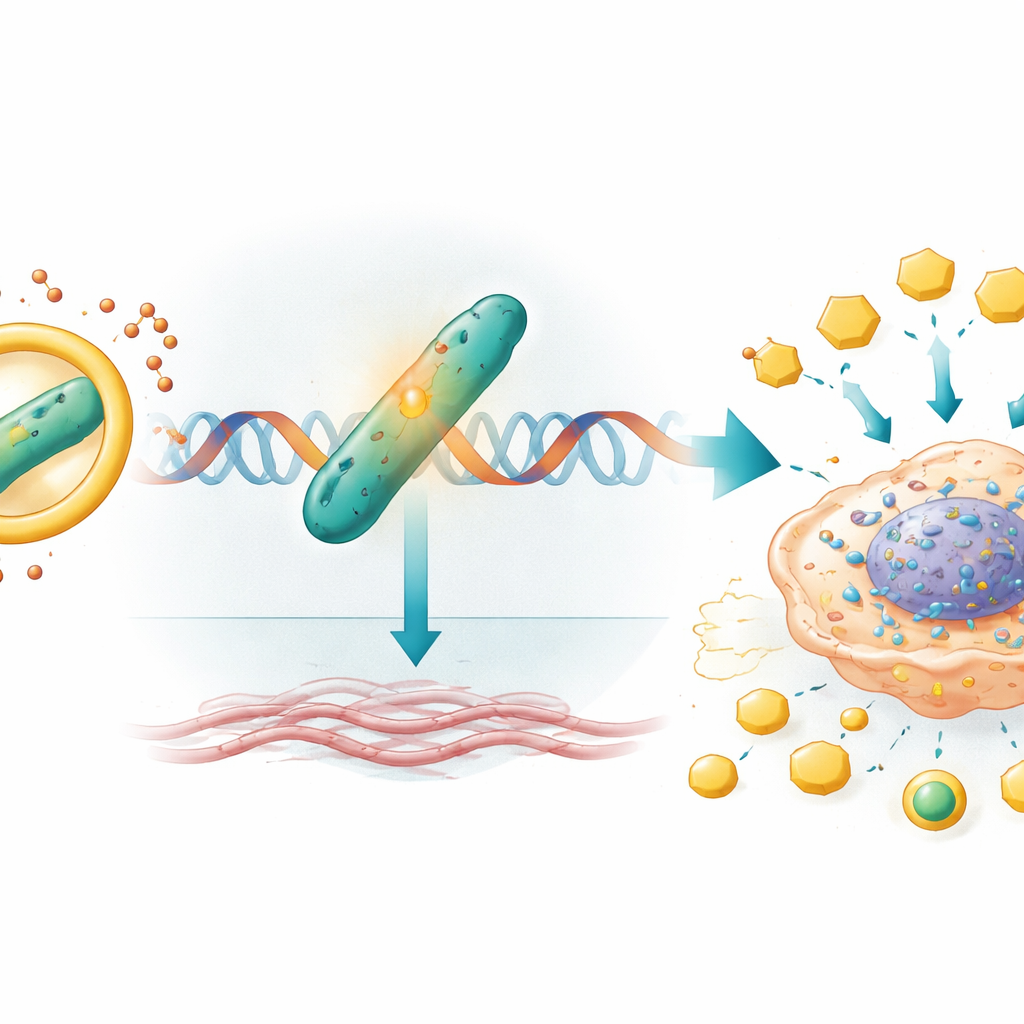
Des commutateurs génétiques à un environnement tumoral durci
Une fois protégé par circIQGAP1, CARM1 se rend au matériel génétique de la cellule et augmente l’activité d’un gène appelé COL5A1. Ce gène code pour un composant du collagène, une protéine structurale qui contribue à former l’échafaudage entourant la tumeur. CARM1 modifie chimiquement les histones — les protéines qui emballent l’ADN — à proximité du «commutateur» COL5A1, rendant ce gène plus accessible et davantage transcrit. Des niveaux élevés de COL5A1 sont liés à des tumeurs plus rigides et plus invasives et ont été associés à un pronostic plus sombre dans le cancer du rein et d’autres tumeurs. Dans cette étude, l’inhibition de COL5A1 réduisait la production de lactate et d’ATP et annulait complètement le stimulant de glycolyse, de croissance, de migration et d’invasion généralement apporté par circIQGAP1 et CARM1, positionnant COL5A1 comme un moteur critique en aval de cette reprogrammation métabolique.
Ce que cela signifie pour les patients
Lorsque les chercheurs ont implanté des cellules de cancer du rein riches en circIQGAP1 chez la souris, les animaux ont développé des tumeurs plus volumineuses et plus rapides à croître, riches en CARM1, COL5A1 et en marqueurs de prolifération. Des patients humains atteints de carcinome rénal présentaient également des niveaux accrus de circIQGAP1 dans leur sang, et ceux ayant davantage de cet ARN circulaire avaient tendance à une survie plus mauvaise. Ensemble, les résultats décrivent une chaîne d’événements claire : U2AF2 augmente circIQGAP1, circIQGAP1 stabilise CARM1, CARM1 active COL5A1, et ce trio pousse les cellules du cancer rénal vers un état agressif alimenté par le glucose. Parce que chaque étape de cet axe peut, en principe, être ciblée — par des approches à base d’ARN, des inhibiteurs d’enzymes ou des médicaments perturbant le remodelage du collagène — ce travail ouvre des pistes pour mieux surveiller et traiter les cancers du rein dépendants d’un métabolisme du glucose altéré.
Citation: Jia, R., Zou, B., Liang, Y. et al. CircIQGAP1-CARM1 axis promotes renal cell carcinoma progression through glycolytic reprogramming. Cell Death Dis 17, 414 (2026). https://doi.org/10.1038/s41419-026-08661-w
Mots-clés: carcinome rénal, métabolisme du cancer, ARN circulaire, CARM1, glycolyse