Clear Sky Science · pl
Oś CircIQGAP1-CARM1 sprzyja progresji raka nerki poprzez przeprogramowanie glikolityczne
Dlaczego nawyk cukrowy raka nerki ma znaczenie
Rak nerki, zwłaszcza powszechny typ z komórek jasnych, rośnie na całym świecie i często pozostaje niezauważony, dopóki nie rozprzestrzeni się dalej. Podobnie jak wiele guzów, nowotwory te przestawiają sposób wykorzystania cukru, spalając glukozę bardzo szybko nawet przy dostępie tlenu. Praca ta ujawnia ukrytą molekularną pętlę, która pozwala komórkom raka nerki pogłębiać to uzależnienie od cukru, rosnąć szybciej i stawać się bardziej agresywnymi — oraz sugeruje nowe sposoby, w jakie lekarze mogliby odciąć dostawy energii guza lub lepiej przewidzieć, którzy pacjenci mają gorsze rokowanie.
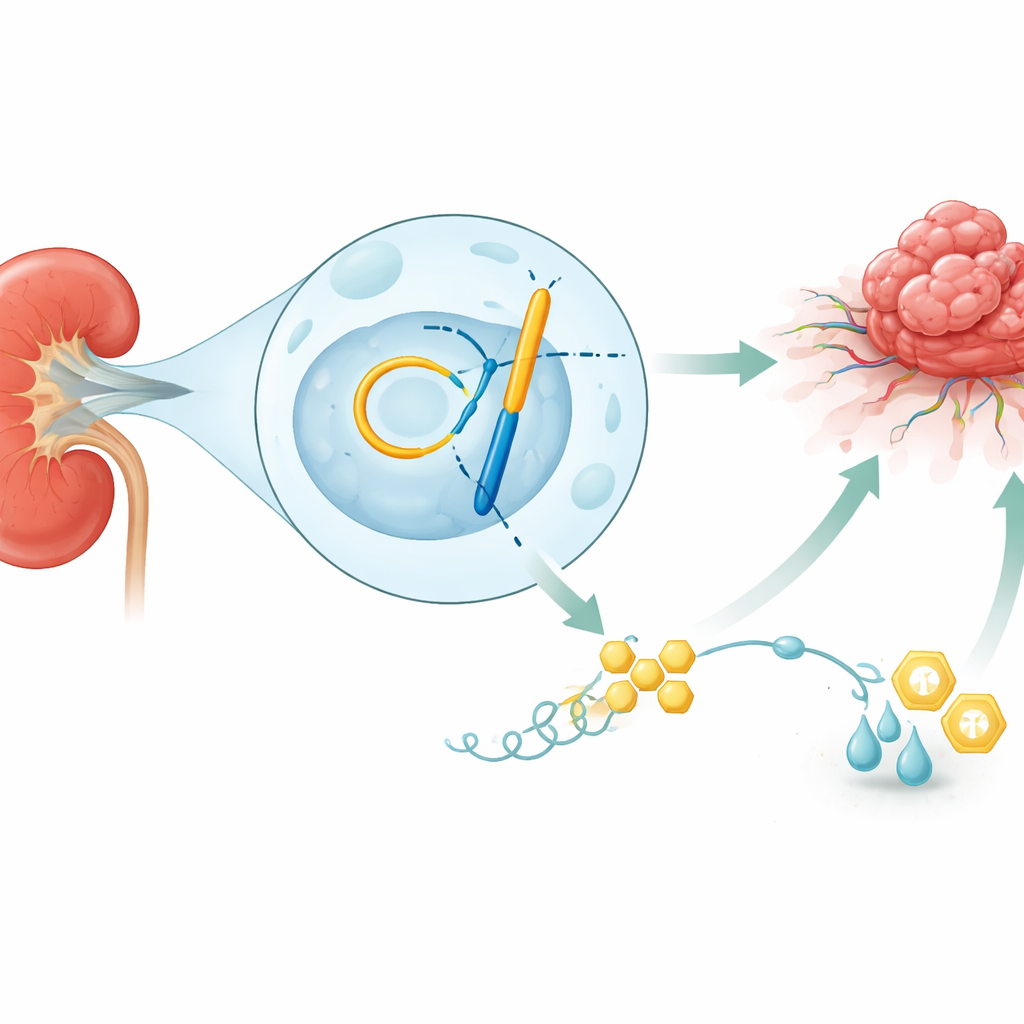
Rak, który kocha cukier
Nasze nerki nieustannie filtrują krew, ale gdy rozwija się rak nerkowokomórkowy, część komórek zmienia się w fabryki łaknące cukru. Zamiast korzystać z wydajnej, zależnej od tlenu ścieżki pozyskiwania energii, preferują szybką i mało dokładną drogę, przekształcając glukozę w mleczan. Ten „tryb turbo” nie tylko dostarcza wystarczająco paliwa i bloków budulcowych do szybkiego wzrostu, lecz także zakwasza otoczenie i osłabia pobliskie komórki odpornościowe. Badanie pokazuje, że nowotwory nerek z takim przyspieszonym metabolizmem mają tendencję do bycia bardziej inwazyjnymi, bardziej odpornymi na leczenie i wiążą się z gorszym przeżyciem pacjentów, co podkreśla, dlaczego istotne jest zrozumienie, co przełącza ten metaboliczny wyłącznik.
W centrum uwagi pojawia się cząsteczka kolista
Naukowcy poszukiwali nietypowych cząsteczek RNA, które zmieniają się, gdy komórki raka nerki są pozbawione glukozy. Odkryli jedną wyróżniającą się: RNA kolistą o nazwie circIQGAP1. W przeciwieństwie do typowego liniowego RNA, ta cząsteczka tworzy zamkniętą pętlę, co czyni ją wysoce stabilną w komórkach. Pod wpływem niskiej dostępności cukru komórki nowotworowe zwiększają produkcję circIQGAP1, przy wsparciu białka splicingowego U2AF2, które podbija jej wytwarzanie. Testy laboratoryjne wykazały, że dodatkowy circIQGAP1 powoduje, że komórki raka nerki dzielą się szybciej, poruszają się łatwiej, naciekają otaczające tkanki i, co kluczowe, zwiększają aktywność glikolityczną — czyli spalanie cukru. Gdy circIQGAP1 został wyciszony, komórki produkowały mniej mleczanu i ATP, wolniej rosły i częściej ulegały śmierci, a zablokowanie glikolizy wygaszało dużą część prozapalnego działania circIQGAP1.
Białkowy strażnik stabilizujący kluczowy wyłącznik
Zagłębiając się dalej, zespół zapytał, jak to RNA koliste przekształca metabolizm raka. Odkryli, że circIQGAP1 fizycznie wiąże się z enzymem białkowym CARM1, znanym z modyfikowania innych białek i zmieniania aktywności genów. Zwykle CARM1 jest oznaczany molekularnymi „flagami”, które kierują go na drogę degradacji. CircIQGAP1 działa jak tarcza, zapobiegając przyłączeniu jednego konkretnego typu znacznika degradacyjnego do CARM1. W rezultacie CARM1 utrzymuje się dłużej i kumuluje w komórce. Ta stabilizacja CARM1 jest silnie związana z gorszym przeżyciem pacjentów z rakiem nerki, a gdy badacze zmniejszyli poziom CARM1, mogli stłumić wzrost i glikolityczny przypływ napędzany przez circIQGAP1, pokazując, że RNA koliste i enzym działają razem jako funkcjonalna jednostka.
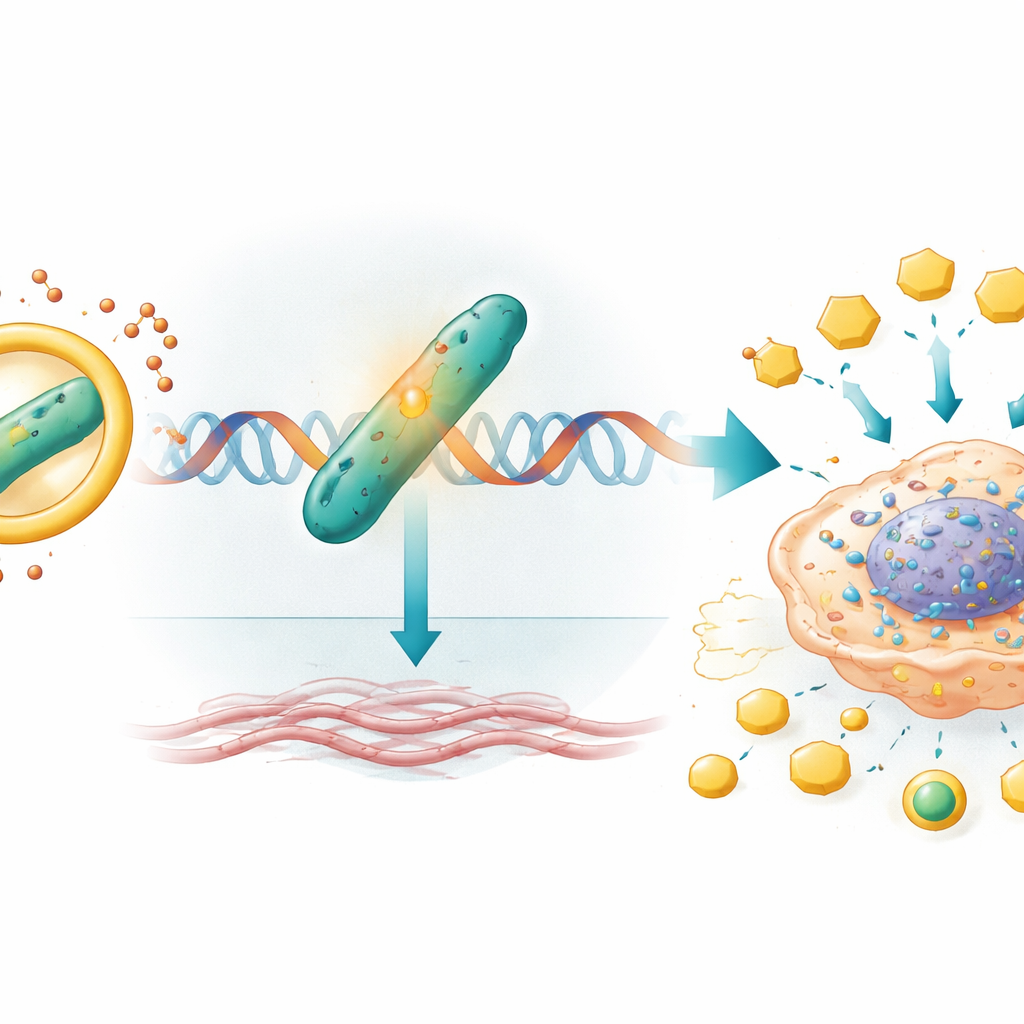
Od przełączników genowych do utwardzonego mikrośrodowiska guza
Gdy CARM1 jest chroniony przez circIQGAP1, trafia do materiału genetycznego komórki i zwiększa aktywność genu o nazwie COL5A1. Gen ten koduje składnik kolagenu, białka strukturalnego, które pomaga tworzyć rusztowanie otaczające guz. CARM1 chemicznie modyfikuje histony — białka pakujące DNA — w pobliżu przełącznika COL5A1, co ułatwia odczyt tego genu i zwiększa jego transkrypcję. Wyższe poziomy COL5A1 wiążą się ze sztywniejszymi, bardziej inwazyjnymi guzami i zostały skorelowane z gorszymi wynikami w raku nerki i innych nowotworach. W tym badaniu wyłączenie COL5A1 zmniejszyło produkcję mleczanu i ATP oraz całkowicie zniwelowało wzrost glikolizy, proliferacji, migracji i inwazji typowo wywoływany przez circIQGAP1 i CARM1, wskazując COL5A1 jako kluczowego pośrednika tego przeprogramowania metabolicznego.
Co to oznacza dla pacjentów
Gdy badacze wszczepili komórki raka nerki o wysokim poziomie circIQGAP1 do myszy, zwierzęta rozwijały większe, szybciej rosnące guzy bogate w CARM1, COL5A1 oraz marker proliferacji. Pacjenci z rakiem nerkowokomórkowym mieli również wyższe poziomy circIQGAP1 we krwi, a osoby z większą ilością tego RNA kolistego miały tendencję do gorszego przeżycia. Razem wyniki opisują jasny ciąg wydarzeń: U2AF2 zwiększa circIQGAP1, circIQGAP1 stabilizuje CARM1, CARM1 włącza COL5A1, a ta triada popycha komórki raka nerki w stronę stanu napędzanego przez cukier i agresywności. Ponieważ każdy etap tej osi może w zasadzie być celem terapii — za pomocą podejść opartych na RNA, inhibitorów enzymów lub leków zakłócających przebudowę kolagenu — praca ta wskazuje nowe strategie monitorowania i leczenia raków nerek silnie polegających na zmienionym metabolizmie glukozy.
Cytowanie: Jia, R., Zou, B., Liang, Y. et al. CircIQGAP1-CARM1 axis promotes renal cell carcinoma progression through glycolytic reprogramming. Cell Death Dis 17, 414 (2026). https://doi.org/10.1038/s41419-026-08661-w
Słowa kluczowe: rak nerki, metabolizm nowotworu, RNA koliste, CARM1, glikoliza