Clear Sky Science · tr
Protein kinaz DYRK1B, p53 hedef geni olarak tanımlandı ve transkripsiyon faktörü RFX7’nin negatif geri besleme düzenleyicisi olarak işlev görüyor
Kanser tedavisi için bunun önemi
Çoğu kanserde, genomun ünlü “bekçisi” olan p53 proteini hasar görmüştür. Bu bekçi normalde hücrelerin duraklamasına, DNA’larını onarmasına veya işler ters gittiğinde kendini yok etmesine yardımcı olur. Burada özetlenen çalışma, kanser hücrelerinin bu koruyucu sistemi başka bir protein olan DYRK1B adlı kinaz aracılığıyla nasıl zayıflatabildiğine dair yeni bir yol ortaya koyuyor ve DYRK1B’yi bloke etmenin tümör hücrelerini kemoterapiye karşı daha savunmasız hâle getirebileceğini gösteriyor.
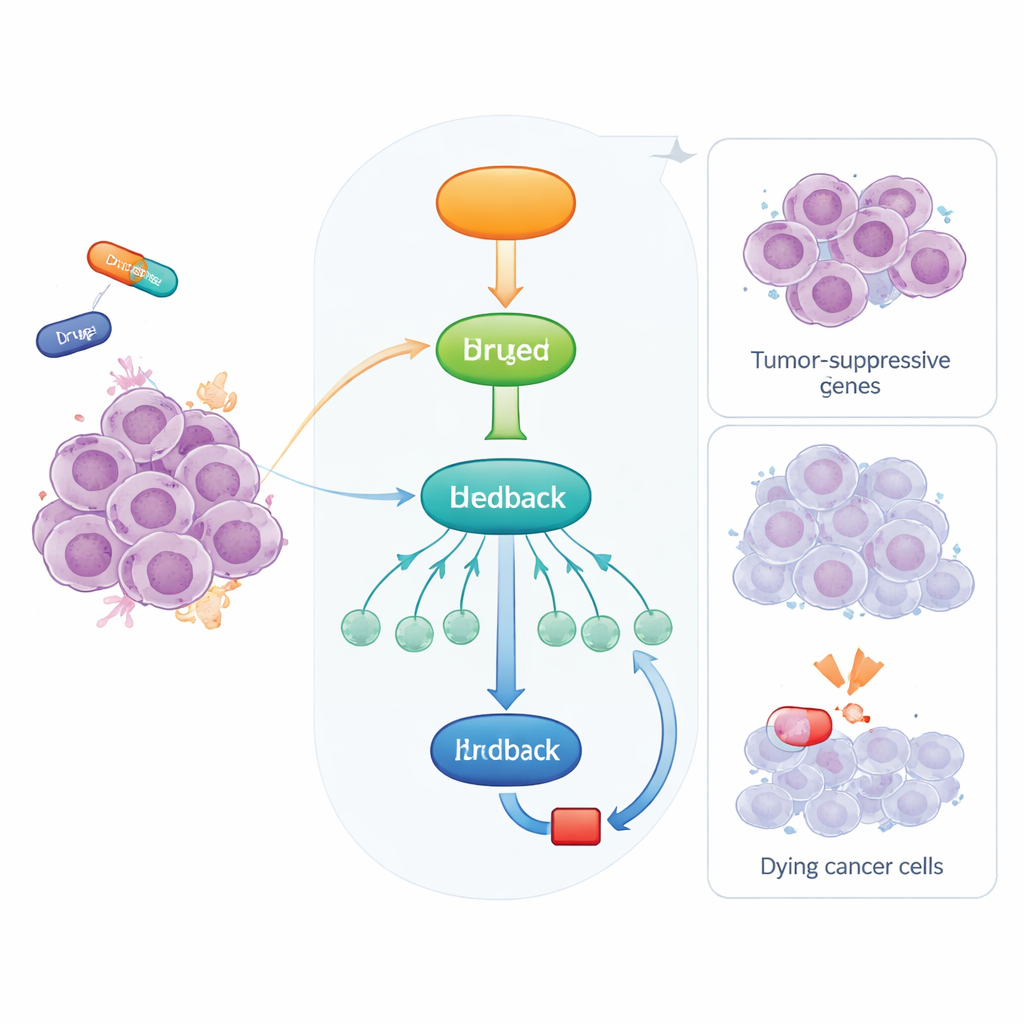
Hücrelerimizde yerleşik bir alarm sistemi
Hücreler DNA hasarı gibi streslerle karşılaştığında ya da yeni hücresel bileşenlerin yapılmasında sorunlar olduğunda, p53 devreye girer ve acil durum programını başlatır. Bunu büyük ölçüde diğer genleri açıp kapatarak yapar. Bu genlerin bazıları doğrudan hücre döngüsünü durdurur veya hücre ölümünü tetikler, ama p53 ayrıca birçok aşağı akış genini düzenleyen ek kontrol proteinleri aracılığıyla da çalışır. Bunlardan biri RFX7’dir; transkripsiyon faktörü olarak yakın zamanda önemli bir tümör baskılayıcı olarak öne çıkmıştır. RFX7, tümör büyümesini sınırlayan bir gen ağını etkinleştirmeye yardımcı olur ve insan kanserlerinde sıkça bozulur veya etkisizleşir.
Odağımızdaki hayatta kalmayı destekleyen kinaz
DYRK1B, diğer proteinlere fosfat grubu ekleyen ve böylece bunların davranışını değiştiren bir enzimdir. Önceki çalışmalar, DYRK1B’nin kanser hücrelerinin zor koşullara dayanmasına, düşük aktivite durumunu korumasına ve DNA hasarını onarmasına yardım ettiğini gösterdi. Birçok solid tümörde anormal derecede yüksek düzeylerde bulunur ve deneysel modellerde bloke edilmesi kanser hücrelerini kemoterapi veya radyasyona karşı daha hassas hâle getirebilir. Yine de birçok diğer kanser ilişkili enzimle kıyaslandığında DYRK1B görece az anlaşılmıştır; bu nedenle ona “karanlık kinaz” etiketi takılmıştır. Yeni çalışma, DYRK1B’nin nasıl kontrol edildiğini ve p53 tarafından yönetilen daha geniş stres yanıtı devrelerine nasıl entegre olduğunu açıklamayı hedefledi.
p53’ten RFX7’ye, oradan DYRK1B’ye
Araştırmacılar, p53’ü aktive eden iki kemoterapi ilacı olan doksorubisin ve aktinomisin D ile çeşitli kanser hücre hatlarını muamele etti. Tedavi sonrası DYRK1B düzeylerinin güçlü şekilde arttığını, buna karşın yakını olan DYRK1A’nın artmadığını gözlemlediler. p53’ü DNA hasarı olmadan etkinleştiren Nutlin-3a adlı bir ilaç kullanarak, p53 her aktive edildiğinde DYRK1B’nin uyarıldığını doğruladılar. p53 genetik olarak ortadan kaldırıldığında DYRK1B’deki bu artış kayboldu ve hasta tümör verilerinin analizi, birçok kanser türünde DYRK1B ifadesinin p53 düzeyleriyle paralellik gösterme eğiliminde olduğunu ortaya koydu. Ekip daha sonra bu uyarının dolaylı olduğunu gösterdi: p53 önce RFX7’yi uyarıyor, RFX7 ise DYRK1B’yi yükseltiyor. RFX7’yi yok etmek veya onun çekirdeğe giriş yeteneğini devre dışı bırakmak DYRK1B uyarımını keskin şekilde azaltırken, DYRK1B seviyeleri hem RNA hem de protein düzeyinde artarak gerçek bir gen aktivasyonunu doğruladı.
Tümör baskılayıcı üzerinde moleküler bir fren
Üretildikten sonra DYRK1B sadece boş oturmaz. Çalışma, DYRK1B’nin hücrelerde fiziksel olarak RFX7 ile ilişkiye girdiğini ve onu değiştirdiğini ortaya koyuyor. p53 RFX7’yi aktive ettiğinde, protein güçlü gen etkinleştirme aktivitesiyle ilişkili bir forma kayar. Küçük moleküllerle DYRK1B’yi inhibe etmek veya hedefe yönelik bir degrader ile azaltmak, bu aktif RFX7 formunu güçlendirirken; DYRK1B’yi fazla ifade etmek, RFX7’yi daha az aktif bir forma geri çevirir ve PDCD4 dahil olmak üzere birkaç RFX7 kontrollü tümör baskılayıcı proteinin üretimini azaltır. Biyokimyasal deneyler, DYRK1B’nin RFX7’nin kuyruk bölgesini fosforile ettiğini, bunun jel üzerinde farklı göç etmesine ve transkripsiyonel etkinliğini kaybetmesine neden olduğunu gösteriyor. Özünde, DYRK1B negatif bir geri besleme halkası oluşturuyor: p53 RFX7’yi açar, RFX7 DYRK1B’yi yükseltir ve DYRK1B de RFX7’yi dizginler.
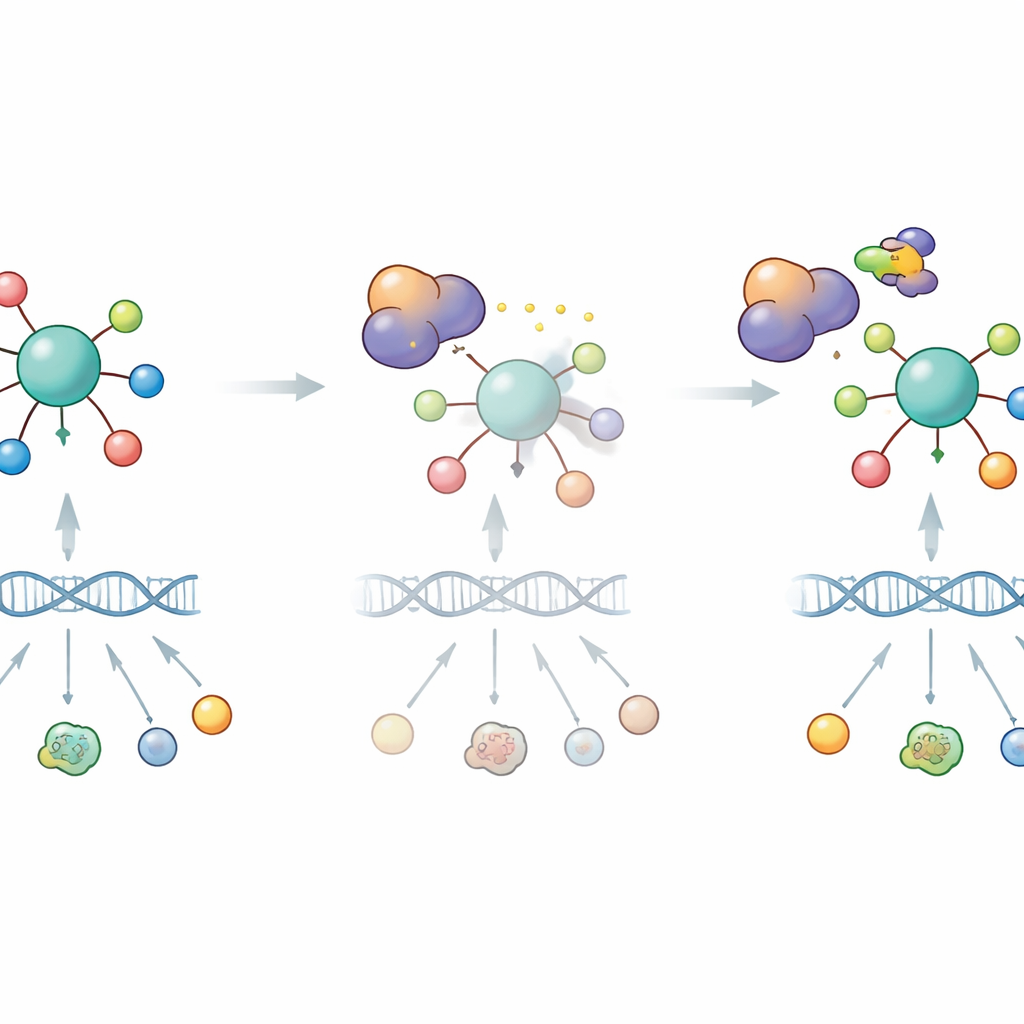
Bir zayıflığı terapötik fırsata çevirmek
DYRK1B bir tümör baskılayıcısının aktivitesini kısıtladığı için yazarlar, DYRK1B’yi bloke etmenin RFX7’nin koruyucu rolunu geri kazandırıp kazandıramayacağını ve kanser hücrelerini kemoterapiye karşı daha hassas hâle getirip getiremeyeceğini test ettiler. DYRK1B’yi aşırı üreten akciğer kanseri hücrelerinde, iki farklı DYRK1 inhibitörü RFX7’yi yeniden etkinleştirebildi, tümör baskılayıcı protein düzeylerini artırdı ve DYRK1B’nin p53 kaynaklı yanıtlar üzerindeki bastırıcı etkisini tersine çevirdi. DYRK1 kinazlarını seçici olarak hedefleyen özel bir bileşik de hücreleri doksorubisin kaynaklı ölüme karşı daha savunmasız kıldı ve bu kemosensitize edici etki RFX7 yok olduğunda azaldı. Birlikte, bu bulgular birçok tümörün p53–RFX7 tümör baskılayıcı sinyalini zayıflatmak için DYRK1B’den yararlanabileceğini ve farmakolojik olarak DYRK1B hedeflenmesinin bu yolu yeniden uyandırmaya yardımcı olabileceğini öne sürüyor. Hastalar açısından bu, gelecekte standart kemoterapi ile birlikte kullanılabilecek DYRK1B inhibitörlerinin kanser hücreleri içindeki dengeyi hayatta kalmadan ziyade hücre ölümüne doğru kaydırma olasılığını gündeme getiriyor.
Atıf: Wilms, G., Schwandt, K., Düsterhöft, S. et al. The protein kinase DYRK1B is a p53 target gene and functions as a negative feedback regulator of the transcription factor RFX7. Cell Death Dis 17, 386 (2026). https://doi.org/10.1038/s41419-026-08660-x
Anahtar kelimeler: p53 sinyalizasyonu, DYRK1B kinazı, RFX7 tümör baskılayıcısı, kanser stres yanıtı, kemosensitize etme