Clear Sky Science · sv
Proteinkinasen DYRK1B är ett p53-målgene och fungerar som en negativ återkopplingsregulator av transkriptionsfaktorn RFX7
Varför detta är viktigt för cancerbehandling
De flesta cancerformer har skador i den välkända ”genomets väktare”, ett protein kallat p53. Denna väktare hjälper normalt celler att pausa, reparera sitt DNA eller självdö när något går fel. Studien som sammanfattas här avslöjar en ny mekanism där cancerceller kan försvaga detta skyddssystem via ett annat protein, en kinas kallad DYRK1B, och visar att blockering av DYRK1B kan göra tumörceller mer sårbara för cytostatika.
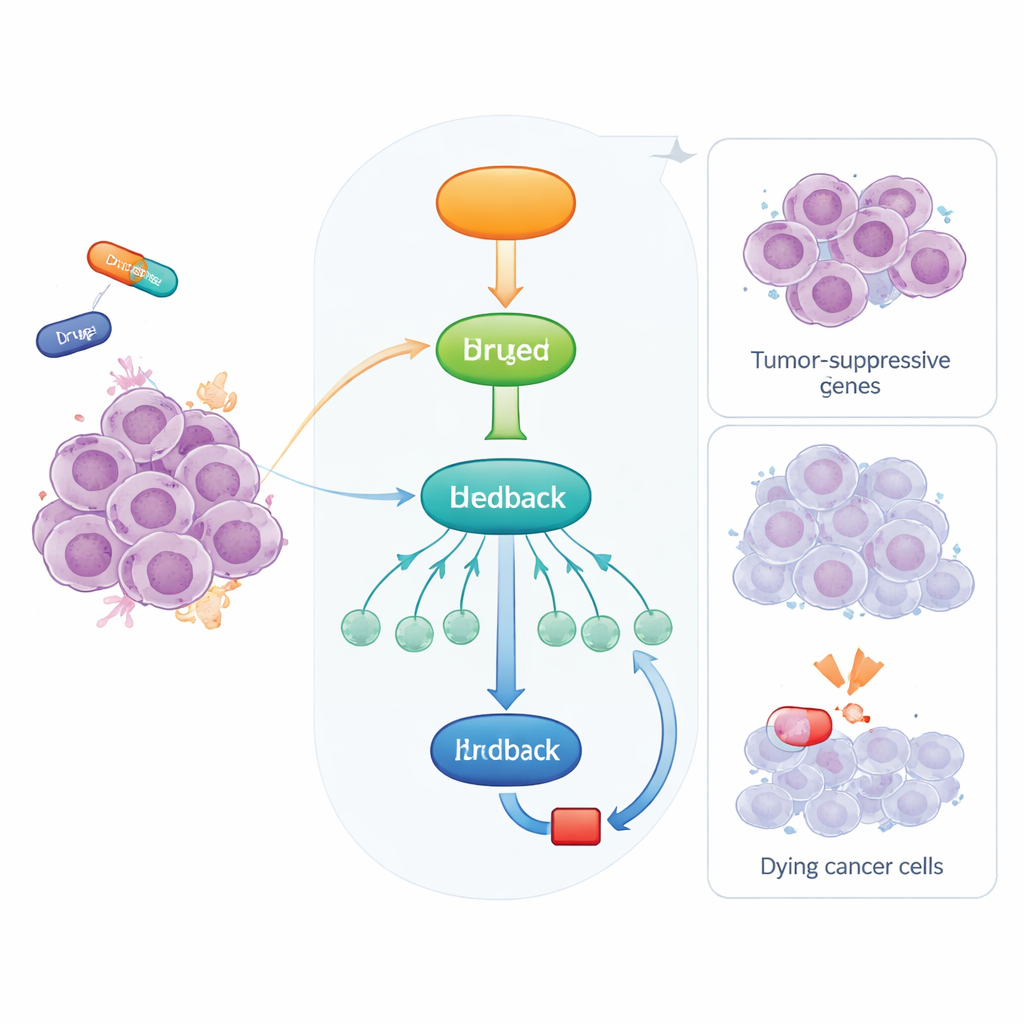
Ett inbyggt larm i våra celler
När celler utsätts för stress, såsom DNA-skada eller problem med att tillverka nya cellulära komponenter, aktiveras p53 och startar ett nödläge. Det gör den till stor del genom att slå på eller av andra gener. Några av dessa gener stoppar direkt cellcykeln eller utlöser celldöd, men p53 verkar också via ytterligare styrproteiner som i sin tur reglerar många downstream-gener. En av dessa är RFX7, en transkriptionsfaktor som nyligen framkommit som en viktig tumörsuppressor. RFX7 hjälper till att aktivera ett nätverk av gener som hämmar tumörtillväxt och är ofta störd eller nedtonad i mänskliga cancerformer.
En överlevnadsfrämjande kinas i rampljuset
DYRK1B är ett enzym som fäster fosfatgrupper på andra proteiner och därigenom ändrar deras beteende. Tidigare arbete visade att DYRK1B hjälper cancerceller att uthärda svåra förhållanden, hålla ett lågt aktivitetsläge och reparera DNA-skador. Det återfinns ofta i onormalt höga nivåer i flera solida tumörer, och att hämma det kan göra cancerceller mer känsliga för kemoterapi eller strålbehandling i experimentella modeller. Jämfört med många andra cancerrelaterade enzymer har dock DYRK1B förblivit dåligt förstått och kallats en ”mörk kinas”. Den nya studien syftade till att klarlägga hur DYRK1B regleras och hur det passar in i den bredare stressresponskretsen som styrs av p53.
Från p53 till RFX7 till DYRK1B
Forskarna behandlade olika cancercellinjer med två cytostatika, doxorubicin och actinomycin D, som båda aktiverar p53. De observerade att DYRK1B-nivåerna ökade kraftigt efter behandling, medan den nära släktingen DYRK1A inte gjorde det. Med hjälp av ett läkemedel kallat Nutlin-3a, som aktiverar p53 utan att orsaka DNA-skada, bekräftade de att DYRK1B induceras när p53 aktiveras. När p53 genetiskt togs bort försvann denna ökning i DYRK1B, och analys av tumördata från patienter visade att DYRK1B‑uttryck tenderar att korrelera med p53-nivåer över många cancerformer. Teamet visade sedan att denna induktion är indirekt: p53 stimulerar först RFX7, och RFX7 ökar i sin tur DYRK1B. Att slå ut RFX7 eller inaktivera dess förmåga att gå in i kärnan minskade kraftigt DYRK1B-induktionen, och DYRK1B-nivåerna steg både på RNA- och proteinnivå, vilket bekräftar äkta genaktivering.
En molekylär broms på en tumörsuppressor
När DYRK1B väl produceras är det inte passivt. Studien visar att DYRK1B fysiskt associerar med RFX7 i celler och modifierar det. När p53 aktiverar RFX7 antar proteinet en form som är kopplad till stark genaktiverande aktivitet. Att hämma DYRK1B med små molekyler eller avlägsna det med en riktad degrader stärker denna aktiva form av RFX7, medan överuttryck av DYRK1B omvandlar RFX7 tillbaka till ett mindre aktivt tillstånd och dämpar produktionen av flera RFX7‑styrda tumörsuppressorproteiner, inklusive PDCD4. Biokemiska experiment visar att DYRK1B fosforylerar RFX7:s svansregion, vilket gör att det migrerar annorlunda i geler och förlorar transkriptionell kraft. I praktiken bildar DYRK1B en negativ återkopplingsslinga: p53 sätter på RFX7, RFX7 ökar DYRK1B, och DYRK1B håller sedan RFX7 i schack.
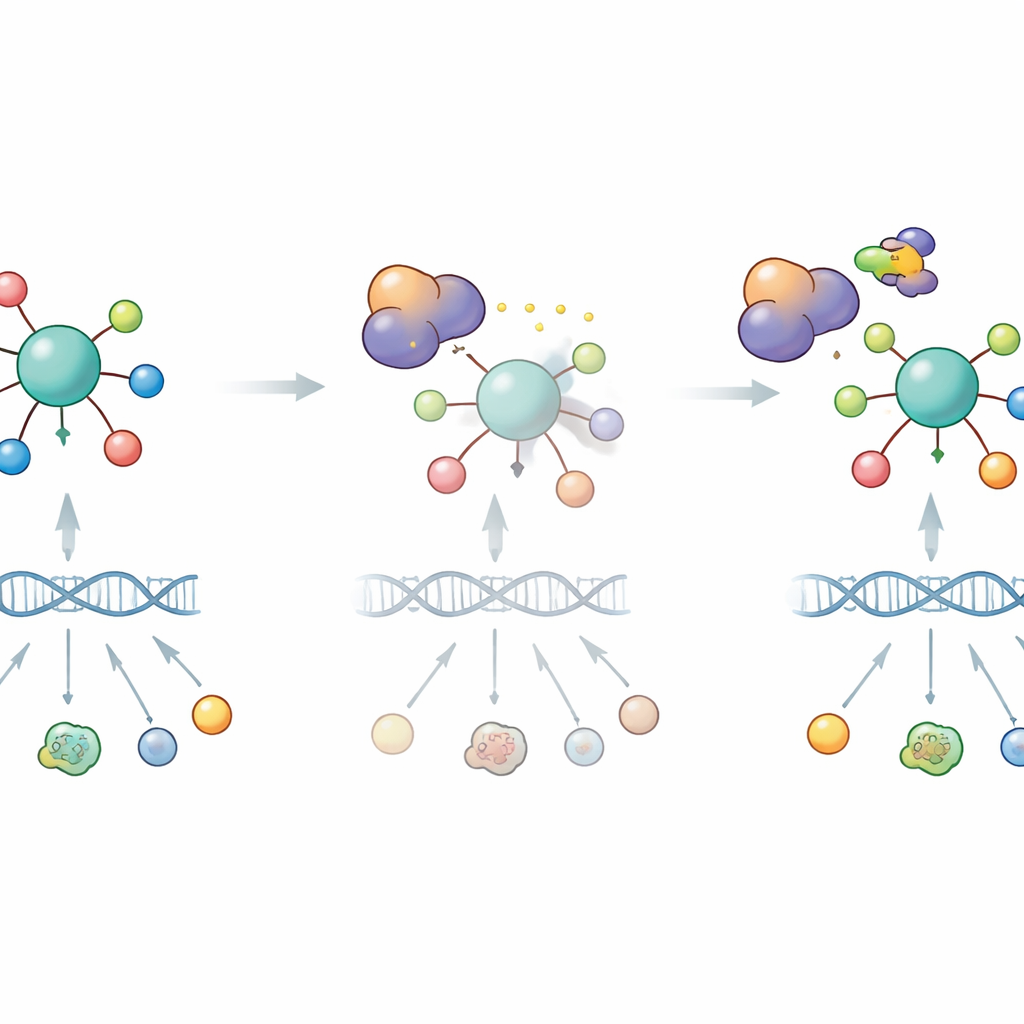
Att vända en svaghet till en terapeutisk möjlighet
Eftersom DYRK1B dämpar aktiviteten hos en tumörsuppressor testade författarna om blockering av DYRK1B kunde återställa RFX7:s skyddande roll och göra cancerceller mer känsliga för kemoterapi. I lungceller konstruerade för att överuttrycka DYRK1B kunde två olika DYRK1‑hämmare återaktivera RFX7, öka nivåerna av tumörsuppressiva proteiner och upphäva DYRK1B:s dämpande effekt på p53‑drivna svar. En specialiserad förening som selektivt degraderar DYRK1‑kinaser gjorde också cellerna mer sårbara för doxorubicininducerad död, och denna kemosensibiliserande effekt minskade när RFX7 saknades. Tillsammans tyder fynden på att många tumörer kan utnyttja DYRK1B för att dämpa p53–RFX7‑tumörsuppressorsignalering, och att farmakologiskt riktade DYRK1B‑hämmare kan hjälpa till att återaktivera denna väg. För patienter öppnar detta möjligheten att framtida DYRK1B‑hämmare, använda tillsammans med standardkemoterapi, kan flytta balansen i cancercellerna tillbaka mot celldöd snarare än överlevnad.
Citering: Wilms, G., Schwandt, K., Düsterhöft, S. et al. The protein kinase DYRK1B is a p53 target gene and functions as a negative feedback regulator of the transcription factor RFX7. Cell Death Dis 17, 386 (2026). https://doi.org/10.1038/s41419-026-08660-x
Nyckelord: p53-signalering, DYRK1B-kinas, RFX7 tumörsuppressor, cancerstressrespons, kemosensibilisering