Clear Sky Science · pl
Kinaza białkowa DYRK1B jest genem docelowym p53 i działa jako ujemne sprzężenie zwrotne dla czynnika transkrypcyjnego RFX7
Dlaczego ma to znaczenie dla leczenia raka
Większość nowotworów nosi uszkodzenia w słynnym „strażniku genomu”, białku zwanym p53. Ten strażnik zwykle pomaga komórkom zatrzymać się, naprawić DNA lub powiązać mechanizmy samobójczej śmierci, gdy coś idzie nie tak. Badanie opisane tutaj ujawnia nowy sposób, w jaki komórki nowotworowe mogą osłabiać ten ochronny system za pośrednictwem innego białka — kinazy DYRK1B — i pokazuje, że blokowanie DYRK1B może zwiększyć wrażliwość komórek nowotworowych na chemioterapię.
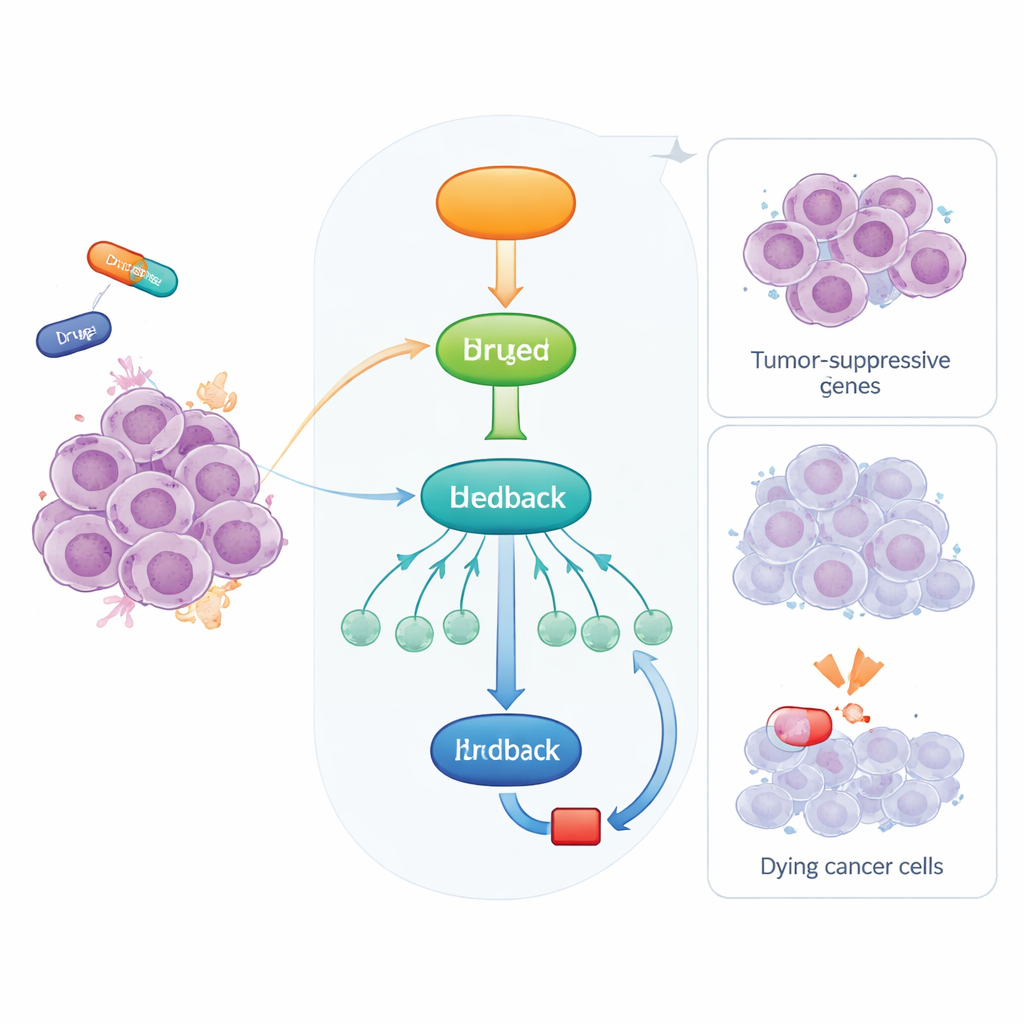
Wbudowany system alarmowy w naszych komórkach
Gdy komórki doświadczają stresu, takiego jak uszkodzenie DNA czy problemy z biogenezą składników komórkowych, p53 włącza program awaryjny. Działa to głównie przez włączanie lub wyłączanie innych genów. Niektóre z tych genów bezpośrednio zatrzymują cykl komórkowy albo uruchamiają śmierć komórki, lecz p53 działa też poprzez dodatkowe białka regulatorowe, które z kolei kontrolują wiele genów downstream. Jednym z takich czynników jest RFX7, czynnik transkrypcyjny, który w ostatnim czasie wyłonił się jako istotny supresor nowotworowy. RFX7 pomaga aktywować sieć genów hamujących wzrost guza i często jest zaburzony lub stłumiony w ludzkich nowotworach.
Kinaza sprzyjająca przeżyciu w centrum uwagi
DYRK1B to enzym przyłączający grupy fosforanowe do innych białek, zmieniając w ten sposób ich funkcję. Wcześniejsze badania wykazały, że DYRK1B pomaga komórkom nowotworowym przetrwać trudne warunki, utrzymać stan o niskiej aktywności i naprawiać uszkodzenia DNA. Często stwierdza się jego podwyższony poziom w kilku nowotworach litych, a jego zahamowanie może w modelach doświadczalnych zwiększać wrażliwość komórek nowotworowych na chemioterapię lub radioterapię. Mimo to, w porównaniu z wieloma innymi enzymami związanymi z rakiem, DYRK1B pozostawał słabo rozpoznany, zyskał więc miano „ciemnej kinazy”. Nowe badanie miało na celu wyjaśnienie, jak regulowana jest DYRK1B i jak wpisuje się ona w szersze obwody reakcji na stres sterowane przez p53.
Od p53 przez RFX7 do DYRK1B
Naukowcy potraktowali różne linie komórek nowotworowych dwoma lekami chemioterapeutycznymi, doksorubicyną i actinomyciną D, które aktywują p53. Zaobserwowali, że poziomy DYRK1B znacząco wzrosły po leczeniu, podczas gdy jej bliski krewny DYRK1A nie. Używając mieszaniny Nutlin-3a, która aktywuje p53 bez wywoływania uszkodzeń DNA, potwierdzili, że DYRK1B jest indukowana za każdym razem, gdy p53 jest aktywne. Gdy p53 zostało genetycznie usunięte, wzrost DYRK1B zanikał, a analiza danych z guzów pacjentów wykazała, że ekspresja DYRK1B zwykle koreluje z poziomami p53 w wielu typach nowotworów. Zespół pokazał następnie, że ta indukcja jest pośrednia: p53 najpierw stymuluje RFX7, a RFX7 z kolei zwiększa DYRK1B. Wyłączenie RFX7 lub unieruchomienie jego wejścia do jądra komórkowego znacząco ograniczało indukcję DYRK1B, a poziomy DYRK1B rosły zarówno na poziomie RNA, jak i białka, co potwierdza prawdziwą aktywację genu.
Cząsteczkowy hamulec na supresorze nowotworowym
Po wytworzeniu DYRK1B nie pozostaje bierna. Badanie ujawnia, że DYRK1B fizycznie wiąże się z RFX7 w komórkach i modyfikuje je. Gdy p53 aktywuje RFX7, białko przyjmuje formę związaną z silną aktywnością aktywującą geny. Hamowanie DYRK1B małocząsteczkowymi inhibitorami lub jego usuwanie za pomocą ukierunkowanych degraderów wzmacnia tę aktywną formę RFX7, podczas gdy nadekspresja DYRK1B przywraca RFX7 do mniej aktywnego stanu i tłumi wytwarzanie kilku białek supresorowych kontrolowanych przez RFX7, w tym PDCD4. Eksperymenty biochemiczne pokazują, że DYRK1B fosforyluje region końcowy (ogon) RFX7, powodując zmianę jego migracji w żelach i utratę zdolności transkrypcyjnej. W istocie DYRK1B tworzy ujemne sprzężenie zwrotne: p53 włącza RFX7, RFX7 podnosi DYRK1B, a DYRK1B potem ogranicza aktywność RFX7.
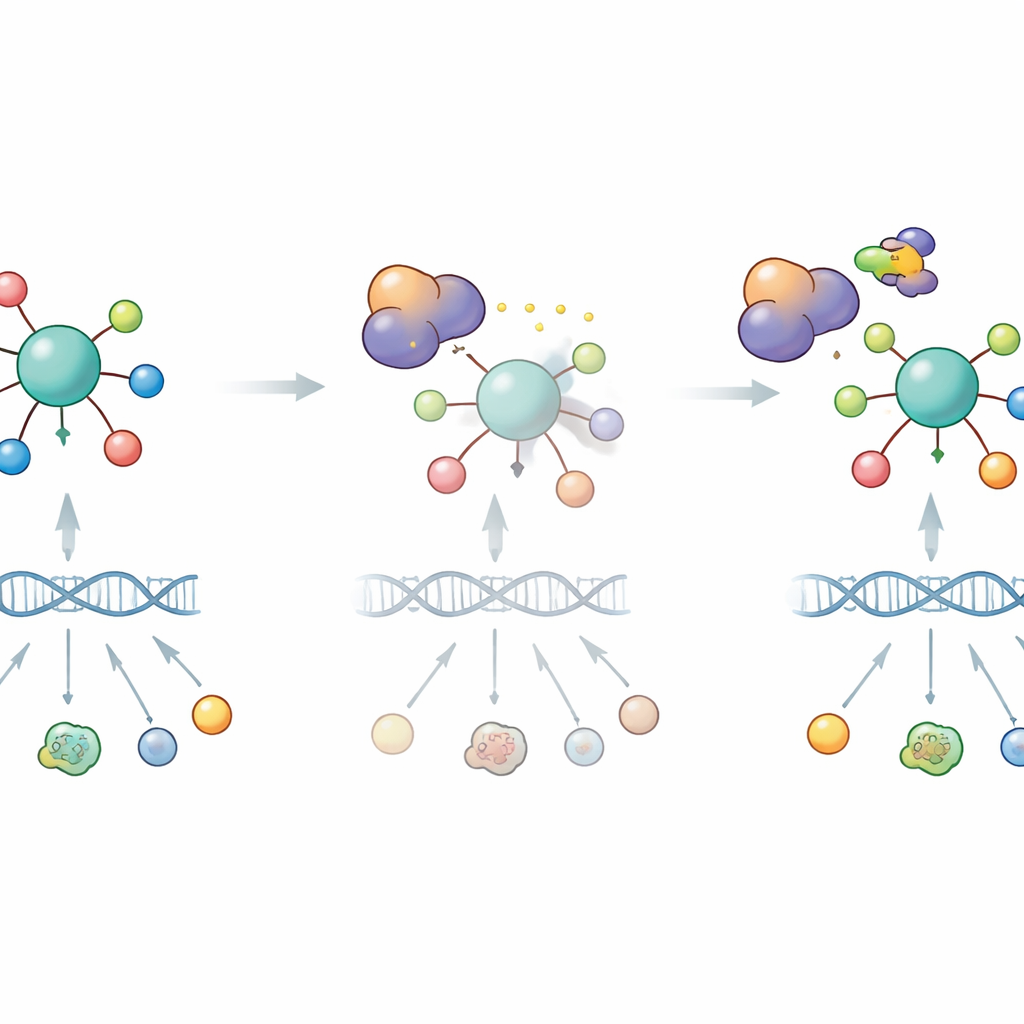
Zmiana słabości w okazję terapeutyczną
Ponieważ DYRK1B ogranicza aktywność supresora nowotworowego, autorzy sprawdzili, czy jego blokada może przywrócić ochronną rolę RFX7 i uczulić komórki nowotworowe na chemioterapię. W komórkach raka płuca zmodyfikowanych tak, by nadmiernie wytwarzały DYRK1B, dwa różne inhibitory DYRK1 potrafiły reaktywować RFX7, zwiększyć poziomy białek o działaniu supresorowym i odwrócić tłumiący wpływ DYRK1B na odpowiedzi napędzane przez p53. Specjalny związek selektywnie degradujący kinazy DYRK1 również zwiększał podatność komórek na śmierć indukowaną doksorubicyną, a efekt chemosensybilizujący był osłabiony przy braku RFX7. Razem te ustalenia sugerują, że wiele guzów może wykorzystywać DYRK1B do tłumienia sygnalizacji p53–RFX7, a farmakologiczne celowanie w DYRK1B mogłoby pomóc w przywróceniu tej ścieżki. Dla pacjentów otwiera się perspektywa, że przyszłe inhibitory DYRK1B, stosowane razem z konwencjonalną chemioterapią, mogą przesunąć równowagę w komórkach nowotworowych z przetrwania ku śmierci komórkowej.
Cytowanie: Wilms, G., Schwandt, K., Düsterhöft, S. et al. The protein kinase DYRK1B is a p53 target gene and functions as a negative feedback regulator of the transcription factor RFX7. Cell Death Dis 17, 386 (2026). https://doi.org/10.1038/s41419-026-08660-x
Słowa kluczowe: sygnalizacja p53, kinaza DYRK1B, supresor nowotworowy RFX7, reakcja na stres w nowotworze, chemosensybilizacja