Clear Sky Science · ru
Киназа белка DYRK1B — ген-мишень для p53 и негативный регулятор транскрипционного фактора RFX7
Почему это важно для лечения рака
У большинства опухолей нарушена работа знаменитого «стража генома», белка p53. Этот страж обычно помогает клеткам приостанавливаться, восстанавливать ДНК или уничтожать себя при критических повреждениях. В представленном исследовании выявлен новый механизм, с помощью которого раковые клетки могут ослаблять эту защитную систему через другой белок — киназу DYRK1B — и показано, что блокада DYRK1B может сделать опухолевые клетки более уязвимыми для химиотерапии.
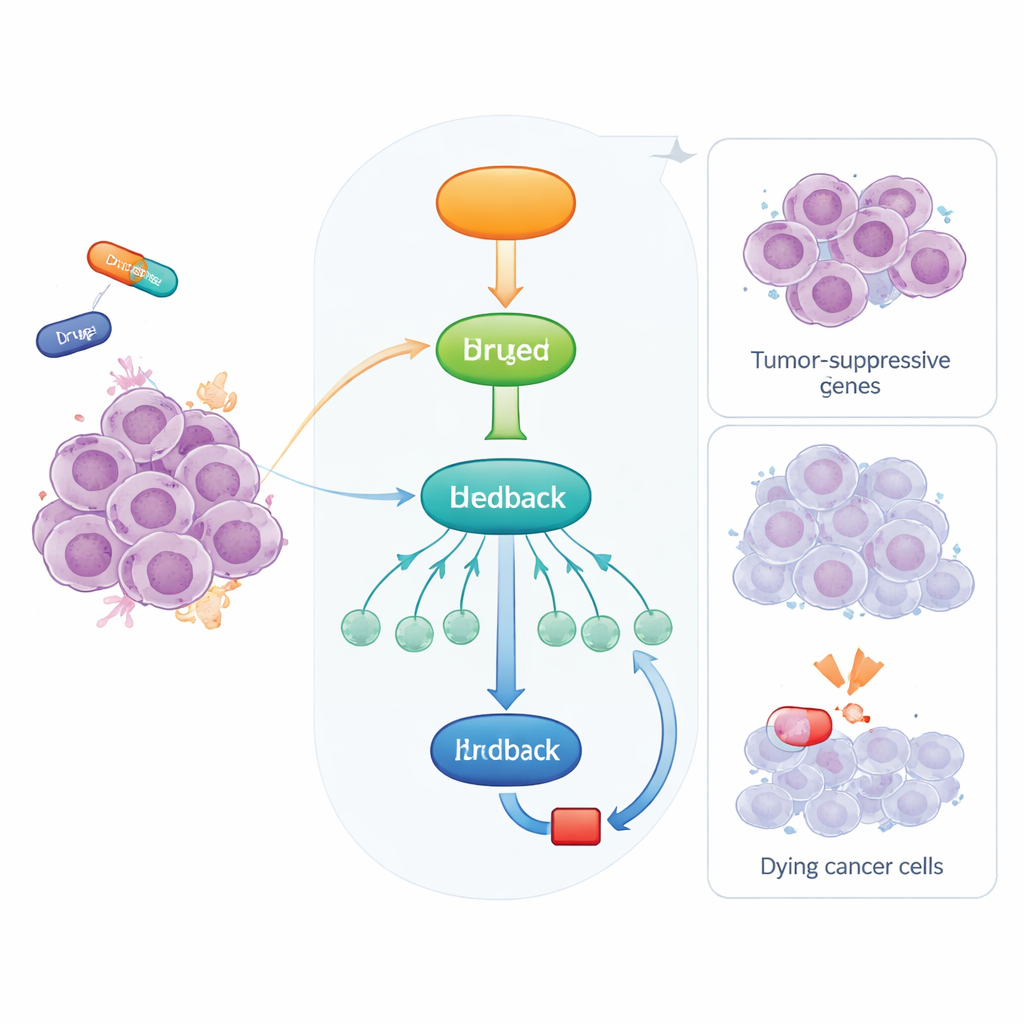
Встроенная сигнализация тревоги в наших клетках
Когда клетки испытывают стресс, например повреждение ДНК или проблемы с синтезом компонентов клетки, p53 включается и запускает аварийную программу. Это происходит главным образом через включение или выключение других генов. Некоторые из этих генов прямо тормозят клеточный цикл или инициируют гибель клетки, но p53 также действует через дополнительные регуляторные белки, которые сами контролируют множество downstream-генов. Один из таких регуляторов — RFX7, транскрипционный фактор, недавно признанный важным супрессором опухолей. RFX7 активирует сеть генов, сдерживающих рост опухоли, и часто нарушается или ослабляется в человеческих раках.
Киназа, способствующая выживанию, в центре внимания
DYRK1B — фермент, присоединяющий фосфатные группы к другим белкам, изменяя их поведение. Предыдущие работы показали, что DYRK1B помогает раковым клеткам переживать неблагоприятные условия, поддерживать низкоактивное состояние и восстанавливать повреждения ДНК. Его часто обнаруживают в аномально высоких количествах в ряде солидных опухолей, а его ингибирование в экспериментальных моделях повышает чувствительность раковых клеток к химио- и радиотерапии. Тем не менее по сравнению со многими другими онкогенными киназами DYRK1B оставалась малоизученной — «тёмной киназой». Новое исследование поставило целью прояснить, как контролируется DYRK1B и как он вписывается в более широкую цепь ответа на стресс, управляемую p53.
От p53 через RFX7 к DYRK1B
Исследователи обработали различные линии раковых клеток двумя химиопрепаратами — доксорубицином и актиномицином D, — которые активируют p53. Они заметили, что уровень DYRK1B значительно повышался после лечения, в то время как близкий родственник DYRK1A — нет. С помощью препарата Nutlin-3a, стимулирующего p53 без повреждения ДНК, подтвердили, что DYRK1B индуцируется всякий раз при активации p53. При генетическом удалении p53 этого подъёма DYRK1B не наблюдалось, а анализ данных опухолей пациентов показал, что экспрессия DYRK1B часто коррелирует с уровнями p53 во многих типах рака. Команда затем показала, что индукция опосредована: p53 сначала стимулирует RFX7, а RFX7, в свою очередь, усиливает экспрессию DYRK1B. Нокаут RFX7 или блокировка его транспорта в ядро резко снижали индукцию DYRK1B, а повышение уровней DYRK1B наблюдалось и на уровне РНК, и на уровне белка, что подтверждает истинную активацию гена.
Молекулярный тормоз на супрессор опухолей
После синтеза DYRK1B не остаётся пассивным. В исследовании показано, что DYRK1B физически взаимодействует с RFX7 в клетках и модифицирует его. Когда p53 активирует RFX7, последний переходит в форму, ассоциированную с сильной транскрипционной активностью. Ингибирование DYRK1B малыми молекулами или его деградация с помощью целевого деградерa усиливают эту активную форму RFX7, тогда как переэкспрессия DYRK1B возвращает RFX7 в менее активное состояние и ослабляет выработку нескольких белков-супрессоров опухолей, контролируемых RFX7, включая PDCD4. Биохимические эксперименты показывают, что DYRK1B фосфорилирует хвостовую область RFX7, из-за чего он по-разному мигрирует в геле и теряет транскрипционную силу. По сути, DYRK1B формирует петлю негативной обратной связи: p53 включает RFX7, RFX7 повышает DYRK1B, а DYRK1B затем сдерживает RFX7.
Преобразование уязвимости в терапевтическую возможность
Поскольку DYRK1B сдерживает активность супрессора опухолей, авторы проверили, может ли блокада DYRK1B восстановить защитную роль RFX7 и повысить чувствительность раковых клеток к химиотерапии. В клетках рака лёгкого с искусственной переэкспрессией DYRK1B два различных ингибитора DYRK1 смогли реактивировать RFX7, увеличить уровни белков-супрессоров опухолей и обратить затухание p53-опосредованных ответов, вызванное DYRK1B. Специфическое соединение, избирательно деградирующее киназы DYRK1, также делало клетки более уязвимыми к гибели, вызванной доксорубицином, и этот эффект хемосенсибилизации ослаблялся при отсутствии RFX7. В совокупности результаты указывают на то, что многие опухоли могут использовать DYRK1B для подавления сигнальной оси p53–RFX7, и что фармакологическая мишень DYRK1B может помочь вновь активировать этот путь. Для пациентов это открывает перспективу, что будущие ингибиторы DYRK1B в сочетании со стандартной химиотерапией могут сместить баланс в раковых клетках в сторону гибели, а не выживания.
Цитирование: Wilms, G., Schwandt, K., Düsterhöft, S. et al. The protein kinase DYRK1B is a p53 target gene and functions as a negative feedback regulator of the transcription factor RFX7. Cell Death Dis 17, 386 (2026). https://doi.org/10.1038/s41419-026-08660-x
Ключевые слова: сигнальная система p53, киназа DYRK1B, подавитель опухолей RFX7, ответ на стресс при раке, хемосенсибилизация