Clear Sky Science · tr
MAGI3 eksikliği, β-katenin konformasyon değişikliğini açığa çıkararak ccRCC'de metastatik ilerlemeyi ve mTOR inhibitörüne direnci tetikliyor
Bu böbrek kanseri çalışması neden önemli
Clear cell (şeffaf hücreli) böbrek kanseri, sıklıkla yayılma gösterdiği ve tedaviye yanıtı kaybettiği için en ölümcül ürolojik kanserlerden biridir. Bu çalışma, böbrek tümörü hücreleri içinde daha önce fark edilmeyen bir “emniyet anahtarı”nı, güçlü bir büyüme sürücüsünü kontrol altında tutan MAGI3 adlı proteini ortaya çıkarıyor. Bu emniyet anahtarı kaybolduğunda, tümörler daha invaziv hale geliyor ve Everolimus gibi yaygın kullanılan mTOR inhibitörlerine direnç geliştiriyor. Bu bulgu, bazı hastaların neden daha kötü seyrettiğini açıklamakla kalmıyor; ayrıca mevcut ilaçların kombinasyonuyla terapinin nasıl iyileştirilebileceğine dair pratik bir yol gösteriyor.
Böbrek tümörlerinde eksik bir koruyucu
Araştırmacılar, şeffaf hücreli böbrek kanserinin metastaz yaptığında özellikle değişen genleri bulmak için büyük halka açık kanser veri kümelerini taramakla başladılar. Binlerce aday arasında MAGI3 öne çıktı: normal böbrek dokusunda aktivitesi tümör dokusuna göre daha yüksekti ve zaten yayılmış tümörlerde daha da düşüktü. Bu desenler hasta örneklerinde protein düzeyinde de doğrulandı; MAGI3 boyanması normal böbrek dokusunda en güçlü, primer tümörlerde daha zayıf ve metastatik yerleşimlerde en zayıftı. Tümörlerinde düşük MAGI3 olan hastalar, klasik genetik değişiklikler (ör. VHL mutasyonları) ne olursa olsun, daha ileri evre, daha yüksek dereceli hastalığa sahip olma ve anlamlı şekilde daha kısa sağkalım eğilimi gösterdi.
MAGI3, güçlü bir büyüme anahtarını nasıl frenliyor
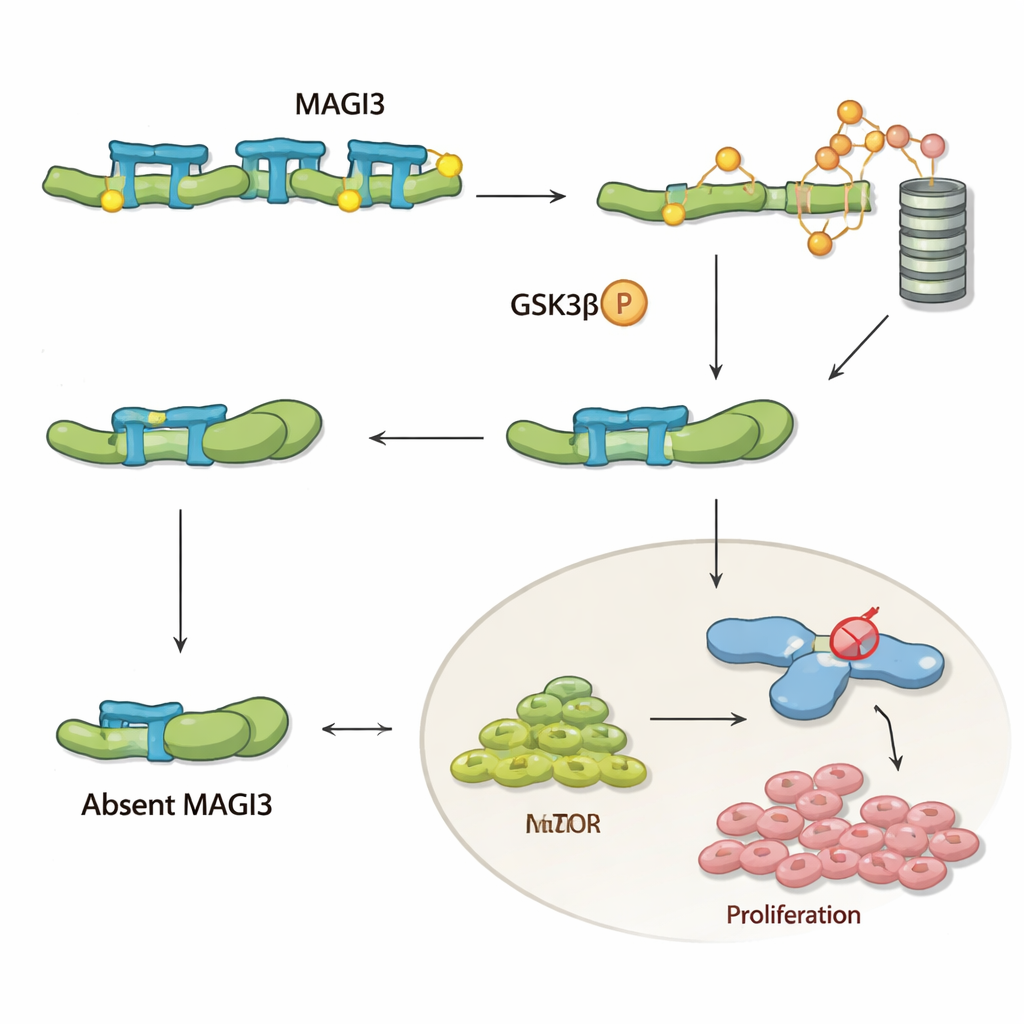
MAGI3'ün hücre içinde ne yaptığını anlamak için ekip, hücre büyümesi, hayatta kalması ve hareketini destekleyen Wnt sinyal yolunun kilit oyuncusu β‑katenine odaklandı. Birçok kanserde β‑katenin birikir ve hastalığı sürükler; ancak şeffaf hücreli böbrek kanserinde nadiren mutasyona uğradığı için kontrol sistemlerinin değişmiş olabileceği düşünülüyordu. Yazarlar, MAGI3'ün fiziksel olarak β‑kateninin kuyruk ucuna bağlandığını ve proteini daha “açık” bir şekle zorladığını gösteriyor. Bu, β‑kateninin karşı uçtaki hassas bölgeleri açığa çıkararak başka bir enzim olan GSK‑3β'nin onu hücrenin atık imha mekanizması için etiketlemesine izin veriyor. MAGI3 bulunduğunda β‑katenin sürekli işaretleniyor, parçalanıyor ve güvenli seviyelerde tutuluyor; MAGI3 kaybolduğunda ise β‑katenin katlanmış halde kalıyor, yok edilmekten kaçıyor, hücrede birikiyor ve tümörlerin büyümesini ve yayılmasını destekleyen genleri açıyor.
Hücre hareketinden ilaç direncine
Böbrek kanseri hücre hatlarında MAGI3 arttırıldığında laboratuvar deneylerinde göç ve invazyon azaldı; MAGI3 azaltıldığında ise ters etki gözlendi. MAGI3 eksik tümör hücreleri farelere enjekte edildiğinde çok daha fazla akciğer metastazı oluşturdu; bu da bu proteinin kaybını agresif davranışla doğrudan ilişkilendiriyor. Ekip daha sonra bu yolun mevcut tedavilerle nasıl kesiştiğini sordu. İleri evre şeffaf hücreli böbrek kanseri hastalarının birçoğu mTOR inhibitörleri (rapaloglar) alıyor, ancak yanıtlar sınırlı ve direnç yaygın. Burada MAGI3 kaybı, kanser hücrelerini Everolimus'e karşı çok daha az duyarlı hale getirdi; ilacın büyümeyi yavaşlatmak için gereken konsantrasyonunu birkaç kat artırdı. Kritik olarak, MAGI3‑eksik hücrelerde Wnt/β‑katenin sinyalini engellemek, Everolimus duyarlılığını geri getirdi ve invazyon yeteneklerini keskin şekilde azalttı.
Hastalar ve hayvan modellerinden kanıt
Bu laboratuvar bulgularının gerçek hastalara tercüme olup olmadığını test etmek için araştırmacılar Everolimus ile tedavi edilen metastatik şeffaf hücreli böbrek kanseri olan 53 kişinin tümörlerini inceledi. Hastalığı kontrol altında olanların tümörlerinde MAGI3 yüksek ve β‑katenin protein düzeyi düşüktü; hızlı ilerleyen hastalarda ise bunun tersi bir desen görülüyordu. Bu grupta düşük MAGI3, daha kısa genel sağkalımı öngördü. MAGI3‑düşük tümör taşıyan farelerde Everolimus tek başına veya yalnız başına bir Wnt yolu ilacı büyümeyi ancak sınırlı şekilde yavaşlattı. Ancak iki tedavinin kombinasyonu tümörleri dramatik şekilde küçülttü ve göze çarpan yan etkilere neden olmadı; bu da MAGI3 kaybının yol açtığı direncin bu yolların eşzamanlı hedeflenmesiyle aşılabileceğini gösteriyor.
Gelecek bakım için anlamı
Bu çalışma MAGI3'ü şeffaf hücreli böbrek kanserinde Wnt/β‑katenin büyüme anahtarını kontrol altında tutan kritik bir iç fren olarak ortaya koyuyor. MAGI3 kaybolduğunda β‑katenin yok edilmekten kaçıyor, metastazı besliyor ve tümörleri mTOR hedefli ilaçlara daha az duyarlı hale getiriyor. Bu nedenle tümör örneklerinde MAGI3 ve β‑katenin ölçümü, doktorların Everolimus'tan fayda görme olasılığı daha yüksek veya düşük olan hastaları belirlemesine yardımcı olabilir. Daha da önemlisi, çalışma mTOR inhibitörlerini Wnt/β‑katenin sinyalini bastıran ilaçlarla birleştirmenin agresif, tedaviye dirençli hastalar için güçlü yeni bir strateji sunabileceğini öne sürüyor.
Atıf: Gu, S., Wang, H., Liu, H. et al. MAGI3 deficiency unleashes β-catenin conformational change to drive metastatic progression and mTOR inhibitor resistance in ccRCC. Cell Death Dis 17, 372 (2026). https://doi.org/10.1038/s41419-026-08563-x
Anahtar kelimeler: clear cell renal cell carcinoma, MAGI3, beta-catenin, mTOR inhibitor resistance, Wnt signaling