Clear Sky Science · de
MAGI3-Mangel entfesselt eine Konformationsänderung von β‑Catenin, die das metastatische Fortschreiten und die Resistenz gegen mTOR‑Inhibitoren bei ccRCC antreibt
Warum diese Studie zum Nierenkrebs wichtig ist
Das klarzellige Nierenkarzinom gehört zu den tödlichsten urologischen Tumoren, da es häufig metastasiert und die Therapie versagt. Diese Studie deckt einen bisher verborgenen „Sicherheitsmechanismus“ in Nierentumorzellen auf — ein Protein namens MAGI3 — das einen starken Wachstums‑Treiber in Schach hält. Geht dieser Schutzmechanismus verloren, werden Tumoren invasiver und resistenter gegenüber einer gebräuchlichen Wirkstoffklasse, den mTOR‑Inhibitoren wie Everolimus. Die Arbeit erklärt nicht nur, warum manche Patientinnen und Patienten schlechtere Verläufe haben, sondern weist auch auf eine praktikable Möglichkeit hin, die Therapie durch Kombination bereits verfügbarer Wirkstoffe zu verbessern.
Ein fehlender Wächter in Nierentumoren
Die Forschenden begannen damit, große öffentliche Krebsdatensätze nach Genen zu durchsuchen, die speziell verändert sind, wenn das klarzellige Nierenkarzinom metastasiert. Unter Tausenden Kandidaten stach MAGI3 hervor: Seine Aktivität war im Tumorgewebe niedriger als im normalen Nierengewebe und in bereits metastasierten Tumoren noch weiter reduziert. Diese Muster bestätigten sich auf Proteinebene in Patientenproben: Die MAGI3‑Färbung war im normalen Nierengewebe am stärksten, in Primärtumoren schwächer und in Metastasen am schwächsten. Patientinnen und Patienten mit niedrigen MAGI3‑Werten in ihren Tumoren wiesen tendenziell fortgeschrittenere Stadien, höhergradige Tumoren und deutlich kürzere Überlebenszeiten auf — unabhängig von klassischen genetischen Veränderungen wie VHL‑Mutationen.
Wie MAGI3 einen mächtigen Wachstums‑Schalter bändigt
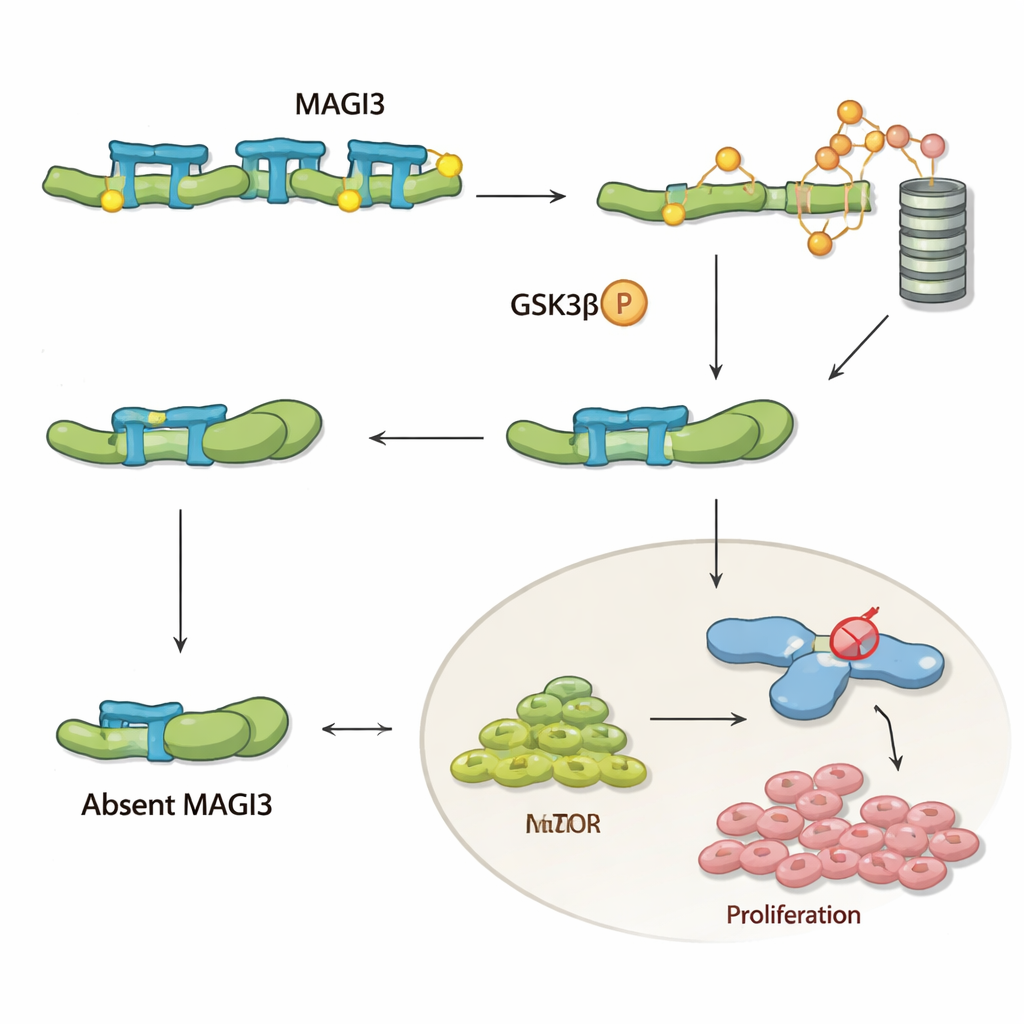
Um zu verstehen, was MAGI3 in der Zelle bewirkt, konzentrierte sich das Team auf β‑Catenin, einen Schlüsselspieler der Wnt‑Signalgebung, die Zellwachstum, Überleben und Migration fördert. In vielen Krebsarten sammelt sich β‑Catenin an und treibt die Krankheit voran, doch beim klarzelligen Nierenkarzinom ist es selten mutiert, was darauf hindeutet, dass stattdessen seine Kontrollmechanismen gestört sind. Die Autorinnen und Autoren zeigen, dass MAGI3 physikalisch an das C‑Ende von β‑Catenin bindet und das Protein in eine offenere Form zwingt. Dadurch werden empfindliche Stellen am gegenüberliegenden Ende von β‑Catenin freigelegt, sodass ein anderes Enzym, GSK‑3β, es für den Abbau durch die zellulären Recycling‑Mechanismen markieren kann. In Gegenwart von MAGI3 wird β‑Catenin fortlaufend markiert, abgebaut und auf sicheren Niveau gehalten; fehlt MAGI3, bleibt β‑Catenin gefaltet, entgeht dem Abbau, reichert sich in der Zelle an und schaltet Gene an, die Tumorwachstum und —ausbreitung fördern.
Von Zellbewegung bis zu Medikamentenresistenz
In Nierenkrebs‑Zelllinien führte eine Erhöhung von MAGI3 zu verringerter Migration und Invasion in Laborversuchen, während eine Reduktion von MAGI3 das Gegenteil bewirkte. Wurden MAGI3‑defiziente Tumorzellen Mäusen injiziert, bildeten sie deutlich mehr Lungenmetastasen, was den Verlust dieses Proteins direkt mit aggressivem Verhalten verknüpft. Das Team untersuchte dann, wie dieser Signalweg mit aktuellen Therapien interagiert. Viele Patientinnen und Patienten mit fortgeschrittenem klarzelligem Nierenkrebs erhalten mTOR‑Inhibitoren (häufig Rapalogs), doch die Ansprechraten sind begrenzt und Resistenzen häufig. Hier machte der MAGI3‑Verlust die Krebszellen deutlich weniger empfindlich gegenüber dem mTOR‑Inhibitor Everolimus und erhöhte die zur Wachstumshemmung benötigte Wirkstoffkonzentration um ein Vielfaches. Entscheidend war, dass die Blockade der Wnt/β‑Catenin‑Signalgebung in diesen MAGI3‑defizienten Zellen ihre Empfindlichkeit gegenüber Everolimus wiederherstellte und ihre Invasionsfähigkeit stark einschränkte.
Belege aus Patientenproben und Tiermodellen
Um zu prüfen, ob diese Laborbefunde auf reale Patientinnen und Patienten übertragbar sind, untersuchten die Forschenden Tumoren von 53 Personen mit metastasiertem klarzelligem Nierenkrebs, die mit Everolimus behandelt wurden. Bei denen, deren Erkrankung kontrolliert werden konnte, fanden sich hohe MAGI3‑ und niedrige β‑Catenin‑Proteinwerte in den Tumoren, während bei rasch fortschreitender Erkrankung das umgekehrte Muster vorlag. Niedrige MAGI3‑Spiegel sagten in dieser Kohorte ein kürzeres Gesamtüberleben voraus. In Mäusen mit MAGI3‑armen Tumoren verlangsamte Everolimus allein oder ein Wnt‑Weg‑Inhibitor allein das Tumorwachstum nur mäßig. Die Kombination beider Behandlungen hingegen verkleinerte die Tumoren dramatisch, ohne erkennbare Nebenwirkungen, was darauf hindeutet, dass die gleichzeitige Hemmung beider Wege die durch MAGI3‑Verlust vermittelte Resistenz überwinden kann.
Was das für die zukünftige Versorgung bedeutet
Die Studie identifiziert MAGI3 als eine entscheidende interne Bremse, die den Wnt/β‑Catenin‑Wachstumsschalter im klarzelligen Nierenkarzinom kontrolliert. Geht MAGI3 verloren, entgeht β‑Catenin dem Abbau, fördert Metastasierung und macht Tumoren weniger ansprechbar auf mTOR‑gerichtete Therapien. Die Messung von MAGI3 und β‑Catenin in Tumorproben könnte Ärztinnen und Ärzten daher helfen, Patientinnen und Patienten zu identifizieren, die eher oder weniger von Everolimus profitieren. Noch wichtiger zeigt die Arbeit, dass die Kombination von mTOR‑Inhibitoren mit Wirkstoffen, die die Wnt/β‑Catenin‑Signalgebung dämpfen, eine vielversprechende neue Strategie für Patientinnen und Patienten mit aggressiver, behandlungsresistenter Erkrankung sein könnte.
Zitation: Gu, S., Wang, H., Liu, H. et al. MAGI3 deficiency unleashes β-catenin conformational change to drive metastatic progression and mTOR inhibitor resistance in ccRCC. Cell Death Dis 17, 372 (2026). https://doi.org/10.1038/s41419-026-08563-x
Schlüsselwörter: klarzellige Nierenzellkarzinom, MAGI3, beta‑Catenin, Resistenz gegen mTOR‑Inhibitoren, Wnt‑Signalgebung