Clear Sky Science · es
La deficiencia de MAGI3 desencadena un cambio conformacional de β‑catenina que impulsa la progresión metastásica y la resistencia a inhibidores de mTOR en CCRCC
Por qué importa este estudio sobre el cáncer de riñón
El carcinoma de células claras de riñón es uno de los cánceres urológicos más letales porque con frecuencia se disemina y deja de responder al tratamiento. Este estudio descubre un “interruptor de seguridad” previamente oculto dentro de las células tumorales renales, una proteína llamada MAGI3, que mantiene bajo control a un potente motor de crecimiento. Cuando se pierde este interruptor, los tumores se vuelven más invasivos y resistentes a una clase de fármacos de uso común, los inhibidores de mTOR como Everolimus. El trabajo no solo explica por qué algunos pacientes evolucionan peor que otros, sino que también apunta a una forma práctica de mejorar la terapia mediante la combinación de fármacos existentes.
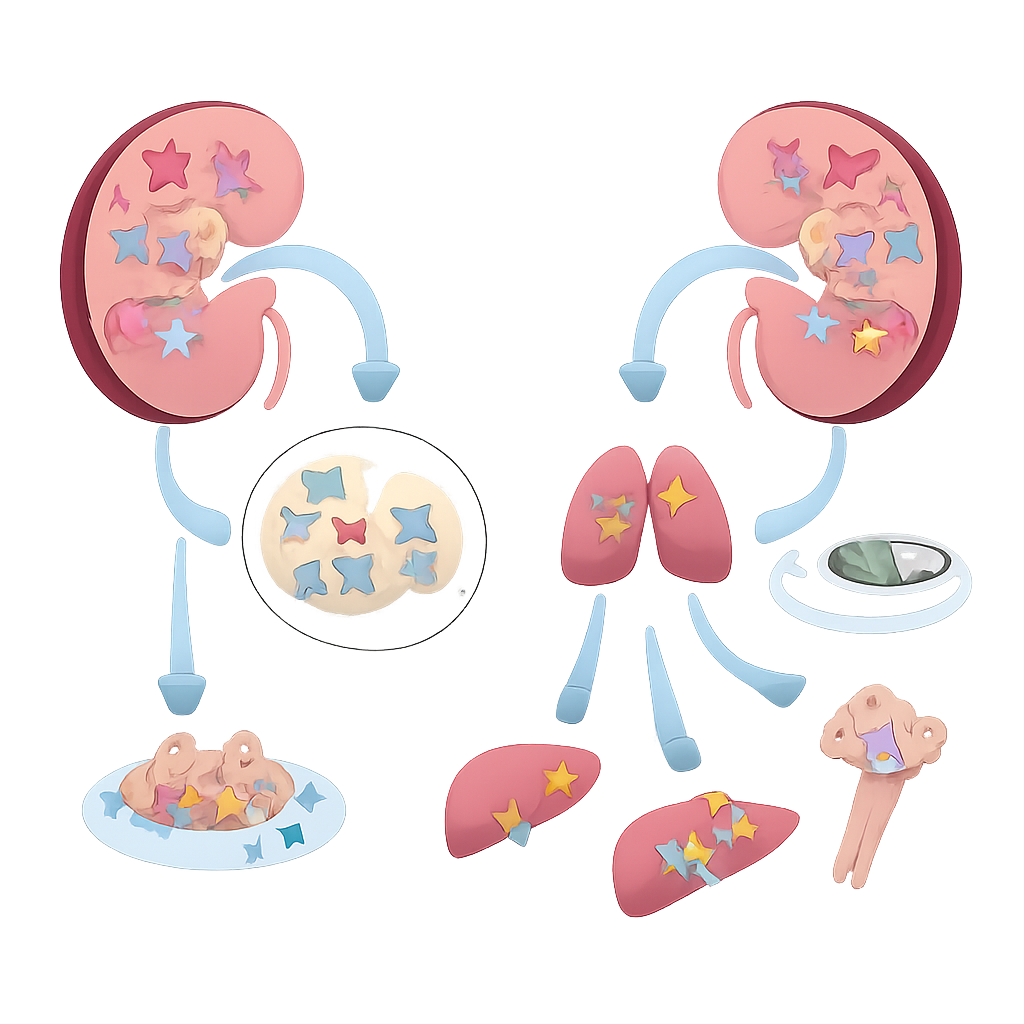
Un guardián ausente en los tumores renales
Los investigadores empezaron analizando grandes bases de datos públicas de cáncer para buscar genes que se alteran específicamente cuando el carcinoma de células claras de riñón se vuelve metastásico. Entre miles de candidatos, MAGI3 destacó: su actividad era menor en tejido tumoral que en riñón normal, y aún más baja en tumores que ya se habían diseminado. Estos patrones se confirmaron a nivel proteico en muestras de pacientes, donde la tinción de MAGI3 fue más intensa en tejido renal normal, más débil en tumores primarios y más baja en las metástasis. Los pacientes cuyos tumores tenían baja expresión de MAGI3 tendían a presentar estadios más avanzados, tumores de mayor grado y supervivencia significativamente más corta, independientemente de cambios genéticos clásicos como las mutaciones en VHL.
Cómo MAGI3 contiene un potente interruptor de crecimiento
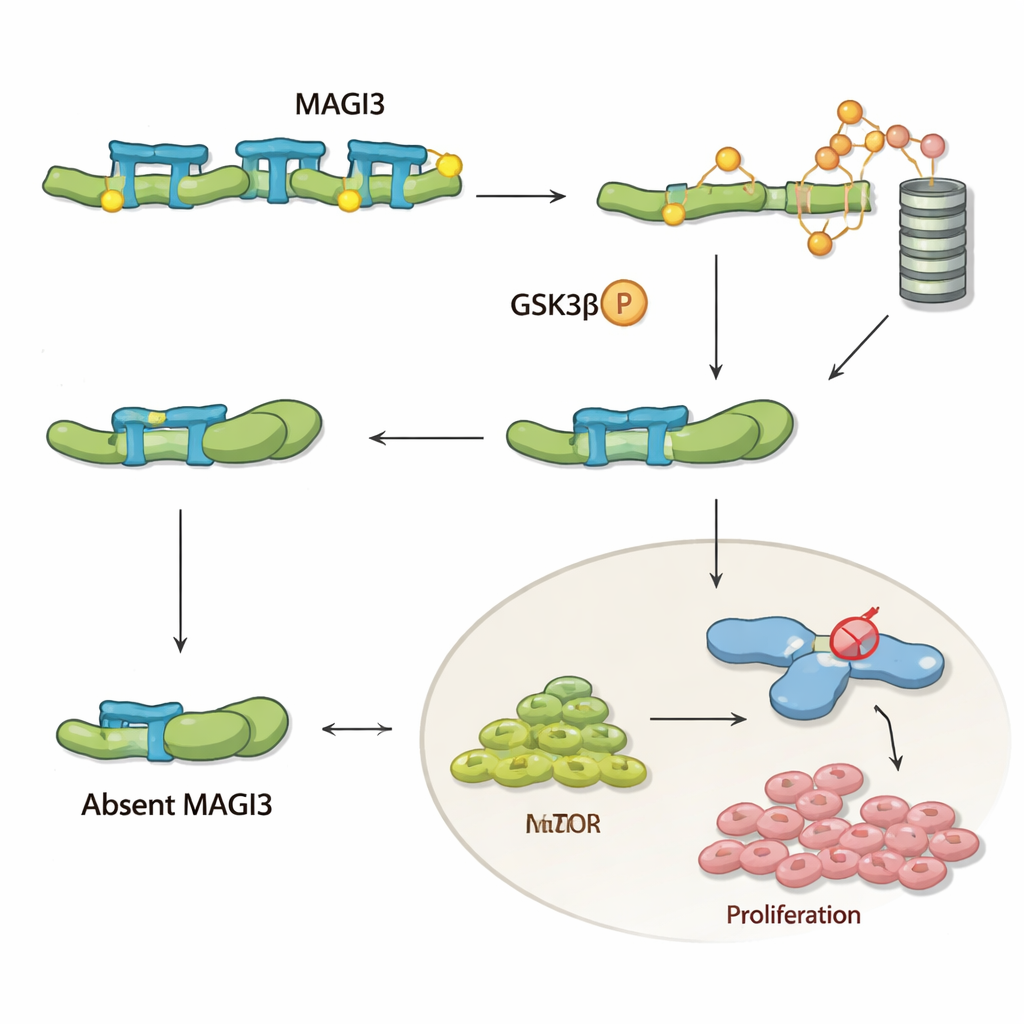
Para entender qué hace MAGI3 dentro de las células, el equipo se centró en la β‑catenina, un actor clave en la vía de señalización Wnt que promueve el crecimiento, la supervivencia y el movimiento celular. En muchos cánceres, la β‑catenina se acumula y dirige la enfermedad, pero en el carcinoma de células claras rara vez está mutada, lo que sugiere que sus sistemas de control están alterados. Los autores muestran que MAGI3 se une físicamente al extremo terminal de la β‑catenina y obliga a la proteína a adoptar una conformación más “abierta”. Esto expone sitios sensibles en el extremo opuesto de la β‑catenina, permitiendo a otra enzima, GSK‑3β, marcarla para su degradación por la maquinaria de eliminación celular. Cuando MAGI3 está presente, la β‑catenina se marca continuamente, se desmonta y se mantiene en niveles seguros; cuando MAGI3 falta, la β‑catenina permanece plegada, evade la degradación, se acumula en la célula y activa genes que ayudan a los tumores a crecer y diseminarse.
Del movimiento celular a la resistencia a fármacos
En líneas celulares de cáncer renal, aumentar MAGI3 redujo la migración y la invasión en ensayos de laboratorio, mientras que disminuir MAGI3 tuvo el efecto contrario. Cuando células tumorales deficientes en MAGI3 se inyectaron en ratones, formaron muchas más metástasis pulmonares, vinculando directamente la pérdida de esta proteína con un comportamiento agresivo. El equipo preguntó entonces cómo intersecta esta vía con los tratamientos actuales. Muchos pacientes con carcinoma de células claras avanzado reciben inhibidores de mTOR (a menudo llamados rapalogs), pero las respuestas son limitadas y la resistencia es común. Aquí, la pérdida de MAGI3 hizo que las células cancerosas fuesen mucho menos sensibles al inhibidor de mTOR Everolimus, aumentando varias veces la concentración de fármaco necesaria para frenar el crecimiento. De forma crucial, bloquear la señalización Wnt/β‑catenina en estas células deficientes en MAGI3 restauró su sensibilidad a Everolimus y redujo drásticamente su capacidad de invadir.
Pruebas en pacientes y modelos animales
Para comprobar si estos hallazgos de laboratorio se traducen a pacientes reales, los investigadores examinaron tumores de 53 personas con carcinoma de células claras metastásico tratadas con Everolimus. Aquellos cuyo tumor estaba controlado mostraron alta expresión de MAGI3 y baja β‑catenina en sus tumores, mientras que los pacientes cuyo cáncer progresó rápidamente presentaron el patrón opuesto. Baja MAGI3 predijo una supervivencia global más corta en este grupo. En ratones portadores de tumores con baja MAGI3, Everolimus solo o un fármaco dirigido solo a la vía Wnt ralentizaron el crecimiento de forma modesta. Sin embargo, la combinación de ambos tratamientos redujo drásticamente los tumores sin causar efectos secundarios evidentes, lo que sugiere que la doble inhibición de estas vías puede superar la resistencia impulsada por la pérdida de MAGI3.
Qué significa esto para la atención futura
Este estudio revela a MAGI3 como un freno interno crucial que mantiene bajo control el interruptor de crecimiento Wnt/β‑catenina en el carcinoma de células claras de riñón. Cuando MAGI3 se pierde, la β‑catenina evade la degradación, impulsa la metástasis y hace que los tumores respondan menos a fármacos dirigidos a mTOR. Medir MAGI3 y β‑catenina en muestras tumorales podría ayudar a los médicos a identificar a los pacientes con más o menos probabilidades de beneficiarse de Everolimus. Aún más importante, el trabajo sugiere que combinar inhibidores de mTOR con fármacos que atenúen la señalización Wnt/β‑catenina puede ofrecer una nueva estrategia eficaz para pacientes con enfermedad agresiva y resistente al tratamiento.
Cita: Gu, S., Wang, H., Liu, H. et al. MAGI3 deficiency unleashes β-catenin conformational change to drive metastatic progression and mTOR inhibitor resistance in ccRCC. Cell Death Dis 17, 372 (2026). https://doi.org/10.1038/s41419-026-08563-x
Palabras clave: carcinoma de células claras de riñón, MAGI3, beta‑catenina, resistencia a inhibidores de mTOR, señalización Wnt