Clear Sky Science · pl
Brak MAGI3 uwalnia zmianę konformacyjną β-kateniny, napędzając progresję przerzutową i oporność na inhibitory mTOR w ccRCC
Dlaczego to badanie raka nerek ma znaczenie
Rak jasnokomórkowy nerki jest jednym z najbardziej śmiertelnych nowotworów urologicznych, ponieważ często daje przerzuty i przestaje odpowiadać na leczenie. W tym badaniu odkryto wcześniej ukryty „wyłącznik bezpieczeństwa” w komórkach guza nerek — białko o nazwie MAGI3 — które hamuje silny czynnik wzrostu. Gdy ten wyłącznik znika, guzy stają się bardziej inwazyjne i odporne na powszechnie stosowaną klasę leków, inhibitory mTOR, takie jak everolimus. Praca nie tylko wyjaśnia, dlaczego niektórzy pacjenci mają gorsze rokowanie, lecz także wskazuje praktyczny sposób poprawy terapii przez łączenie istniejących leków.
Brakujący strażnik w guzach nerek
Naukowcy zaczęli od przeszukania dużych publicznych zbiorów danych onkologicznych w poszukiwaniu genów, które ulegają specyficznym zmianom, gdy rak jasnokomórkowy nerki przechodzi w postać przerzutową. Spośród tysięcy kandydatów wyróżnił się MAGI3: jego aktywność była niższa w tkance nowotworowej niż w zdrowej nerce, a jeszcze niższa w guzach, które już dały przerzuty. Wzorce te potwierdzono na poziomie białka w próbkach od pacjentów — barwienie MAGI3 było najsilniejsze w zdrowej tkance nerkowej, słabsze w guzach pierwotnych i najsłabsze w przerzutach. Pacjenci z guzami o niskim poziomie MAGI3 częściej mieli zaawansowane stadium choroby, wyższy stopień złośliwości i istotnie krótsze przeżycie, niezależnie od klasycznych zmian genetycznych, takich jak mutacje VHL.
Jak MAGI3 powstrzymuje silny przełącznik wzrostu
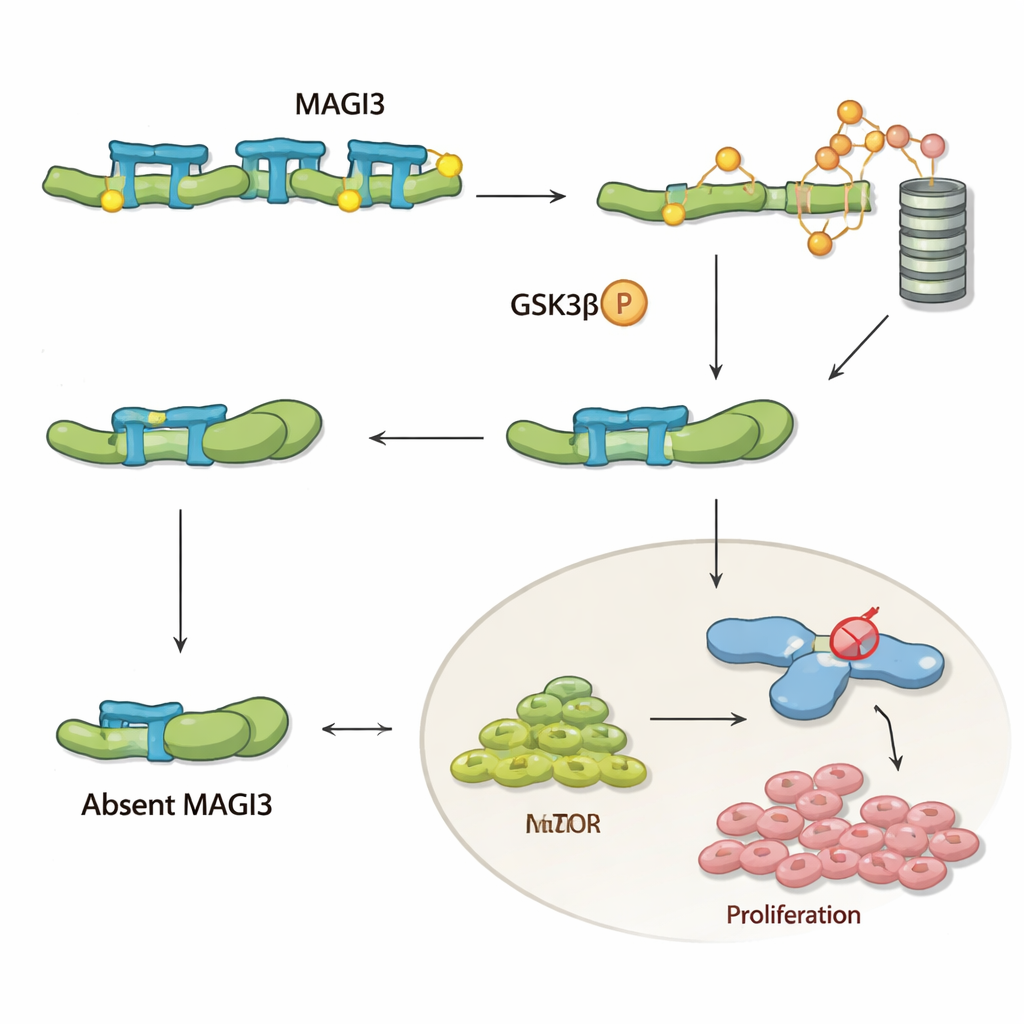
Aby zrozumieć funkcję MAGI3 w komórkach, zespół skupił się na β‑kateninie, kluczowym elemencie szlaku sygnalizacji Wnt, który sprzyja wzrostowi, przeżyciu i migracji komórek. W wielu nowotworach β‑katenina się kumuluje i napędza chorobę, ale w raku jasnokomórkowym nerki rzadko ulega mutacjom, co sugeruje, że problem leży w mechanizmach jej regulacji. Autorzy pokazują, że MAGI3 fizycznie wiąże się z końcem ogonowym β‑kateniny i wymusza na białku bardziej „otwartą” konformację. To odsłania wrażliwe miejsca na przeciwnym końcu β‑kateniny, pozwalając innemu enzymowi, GSK‑3β, znakować ją do zniszczenia przez komórkowe mechanizmy degradacji. Gdy MAGI3 jest obecne, β‑katenina jest ciągle oznaczana, rozkładana i utrzymywana na bezpiecznym poziomie; gdy MAGI3 znika, β‑katenina pozostaje w złożonej formie, unika degradacji, gromadzi się w komórce i aktywuje geny sprzyjające wzrostowi i rozprzestrzenianiu się guza.
Od ruchu komórek do oporności na leki
W liniach komórkowych raka nerek zwiększenie poziomu MAGI3 zmniejszało migrację i inwazyjność w testach laboratoryjnych, natomiast obniżenie MAGI3 dawało efekt odwrotny. Gdy komórki nowotworowe pozbawione MAGI3 zostały wstrzyknięte do myszy, powstawało znacznie więcej przerzutów do płuc, co bezpośrednio łączy utratę tego białka z agresywnym zachowaniem. Zespół zbadał następnie, jak ten szlak przecina się z obecnymi terapiami. Wielu pacjentów z zaawansowanym rakiem jasnokomórkowym otrzymuje inhibitory mTOR (tzw. rapalogi), ale odpowiedzi są ograniczone, a oporność powszechna. W tym badaniu utrata MAGI3 uczyniła komórki nowotworowe znacznie mniej wrażliwymi na everolimus, zwiększając stężenie leku potrzebne do spowolnienia wzrostu wielokrotnie. Co istotne, zablokowanie sygnalizacji Wnt/β‑kateniny w komórkach pozbawionych MAGI3 przywracało ich wrażliwość na everolimus i wyraźnie ograniczało zdolność do inwazji.
Dowody od pacjentów i w modelach zwierzęcych
Aby sprawdzić, czy obserwacje z laboratorium przekładają się na rzeczywistych pacjentów, badacze przeanalizowali guzy od 53 osób z przerzutowym rakiem jasnokomórkowym leczonych everolimusem. U pacjentów, u których choroba była opanowana, w guzach stwierdzono wysoki poziom MAGI3 i niski poziom β‑kateniny; u osób, których choroba szybko postępowała, obserwowano odwrotny obraz. Niski poziom MAGI3 przewidywał krótsze całkowite przeżycie w tej grupie. U myszy z guzami o niskim MAGI3 sam everolimus lub sam lek hamujący szlak Wnt tylko umiarkowanie spowalniały wzrost. Jednak połączenie obu terapii dramatycznie zmniejszyło guzy bez zauważalnych skutków ubocznych, co sugeruje, że jednoczesne celowanie w oba szlaki może przełamać oporność wynikającą z utraty MAGI3.
Co to oznacza dla przyszłej opieki
Badanie ujawnia MAGI3 jako kluczową wewnętrzną blokadę, która utrzymuje przełącznik wzrostu Wnt/β‑katenina pod kontrolą w raku jasnokomórkowym nerki. Gdy MAGI3 zanika, β‑katenina unika degradacji, napędza przerzuty i powoduje mniejszą wrażliwość guzów na leki celujące mTOR. Pomiar MAGI3 i β‑kateniny w próbkach guza mógłby pomóc lekarzom zidentyfikować pacjentów bardziej lub mniej predysponowanych do korzyści z everolimusu. Co ważniejsze, praca sugeruje, że łączenie inhibitorów mTOR z lekami tłumiącymi sygnalizację Wnt/β‑kateniny może być skuteczną nową strategią dla pacjentów z agresywnym, opornym na leczenie nowotworem.
Cytowanie: Gu, S., Wang, H., Liu, H. et al. MAGI3 deficiency unleashes β-catenin conformational change to drive metastatic progression and mTOR inhibitor resistance in ccRCC. Cell Death Dis 17, 372 (2026). https://doi.org/10.1038/s41419-026-08563-x
Słowa kluczowe: rak jasnokomórkowy nerki, MAGI3, beta-katenina, oporność na inhibitory mTOR, szlak Wnt