Clear Sky Science · nl
MAGI3-tekort ontketent conformatieverandering van β-catenine die metastatische progressie en mTOR-remmerresistentie in ccRCC aandrijft
Waarom deze nierkankerstudie ertoe doet
Heldere cel-nierkanker behoort tot de dodelijkste urologische tumoren omdat ze vaak uitzaait en ophoudt te reageren op behandeling. Deze studie onthult een eerder verborgen "veiligheidsschakelaar" in niertumorcellen, een eiwit genaamd MAGI3, dat een krachtige groeidrivier in toom houdt. Wanneer deze schakelaar verloren gaat, worden tumoren invasiever en resistenter tegen een veelgebruikte geneesmiddelengroep, mTOR-remmers zoals Everolimus. Het werk verklaart niet alleen waarom sommige patiënten slechter af zijn, maar wijst ook op een praktische manier om therapie te verbeteren door bestaande middelen te combineren.
Een ontbrekende beschermer in niertumoren
De onderzoekers begonnen met het doorzoeken van grote openbare kankerdatabanken om genen te vinden die specifiek veranderd zijn wanneer heldercellige nierkanker gemetastaseerd raakt. Uit duizenden kandidaten stak MAGI3 er uit: de activiteit was lager in tumorweefsel dan in normaal nierweefsel, en nog lager in tumoren die al hadden uitgezaaid. Deze patronen werden bevestigd op eiwitniveau in patiëntenmonsters, waar MAGI3-kleuring het sterkst was in normaal nierweefsel, zwakker in primaire tumoren en het zwakst in metastatische afzettingen. Patiënten waarvan de tumoren weinig MAGI3 hadden, vertoonden doorgaans een gevorderder stadium, een hogere graad van ziekte en een significant kortere overleving, onafhankelijk van klassieke genetische veranderingen zoals VHL-mutaties.
Hoe MAGI3 een krachtige groeischakel in bedwang houdt
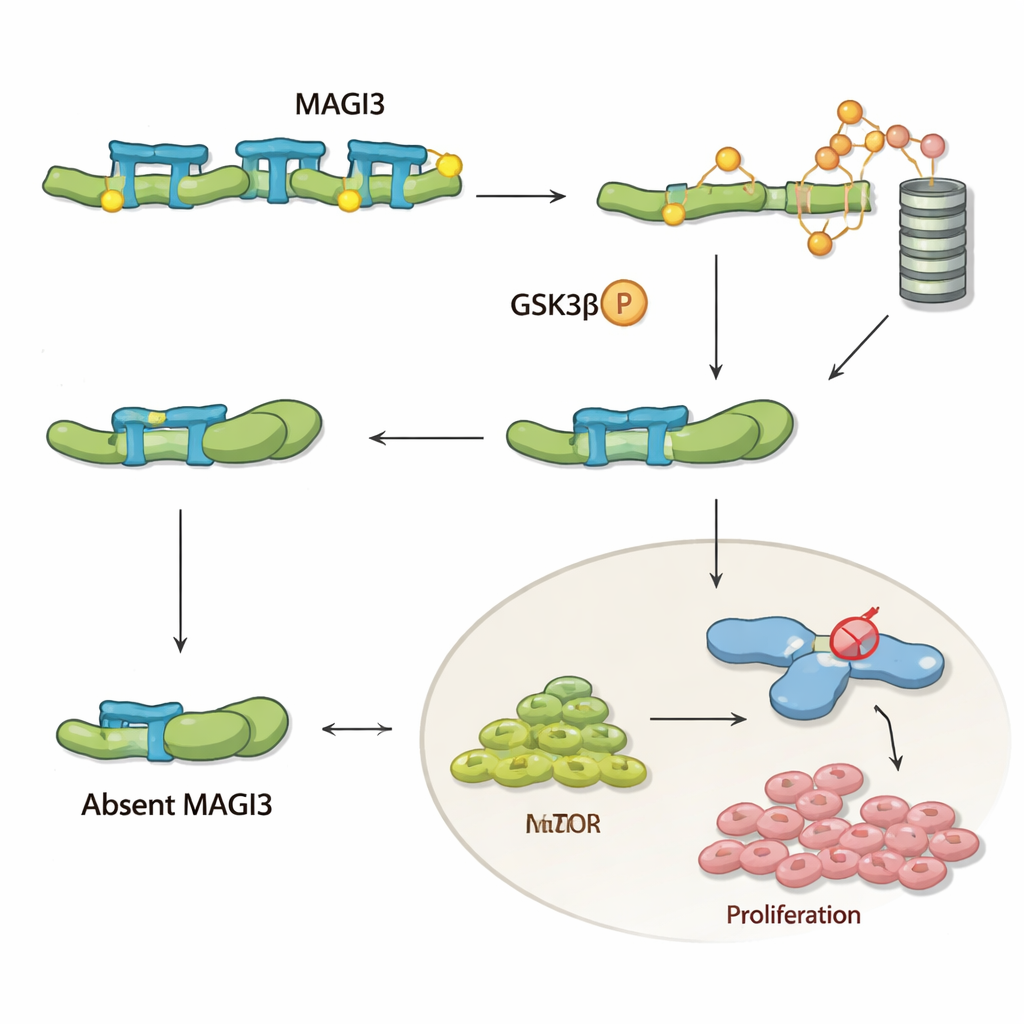
Om te begrijpen wat MAGI3 binnenin cellen doet, richtte het team zich op β‑catenine, een sleutelspeler in de Wnt-signaalweg die celgroei, overleving en migratie bevordert. In veel kankers hoopt β‑catenine zich op en drijft het de ziekte aan, maar bij heldercellige nierkanker is het zelden gemuteerd, wat suggereert dat de controlesystemen ervan eerder zijn verstoord. De auteurs laten zien dat MAGI3 fysiek bindt aan het staartuiteinde van β‑catenine en het eiwit in een meer “open” vorm dwingt. Dit maakt gevoelige plekken aan het tegenovergestelde uiteinde van β‑catenine toegankelijk, waardoor een ander enzym, GSK‑3β, het kan markeren voor afbraak door het cellulair afvalverwerkingssysteem. Wanneer MAGI3 aanwezig is, wordt β‑catenine voortdurend gemarkeerd, afgebroken en op veilige niveaus gehouden; bij afwezigheid van MAGI3 blijft β‑catenine gevouwen, ontsnapt het aan afbraak, hoopt het zich op in de cel en schakelt genen aan die tumorgroei en -uitzaaiing bevorderen.
Van celbeweging naar medicijnresistentie
In nierkankercellijnen verminderde het verhogen van MAGI3 migratie en invasie in laboratoriumtests, terwijl het verlagen van MAGI3 het tegengestelde effect had. Wanneer MAGI3-deficiente tumorcellen in muizen werden geïnjecteerd, vormden ze veel meer longmetastasen, wat het verlies van dit eiwit direct koppelt aan agressief gedrag. Het team onderzocht vervolgens hoe deze route zich verhoudt tot huidige behandelingen. Veel patiënten met gevorderde heldercellige nierkanker krijgen mTOR-remmers (vaak rapalogen genoemd), maar de responsen zijn beperkt en resistentie komt veel voor. Hier maakte het verlies van MAGI3 kankercellen veel minder gevoelig voor de mTOR-remmer Everolimus, waarbij de benodigde medicijnconcentratie om groei te vertragen meerdere malen toenam. Cruciaal was dat het blokkeren van Wnt/β‑catenine-signaaltransductie in deze MAGI3-deficiente cellen hun gevoeligheid voor Everolimus herstelde en hun invasieve vermogen sterk verminderde.
Bewijs uit patiënten en diermodellen
Om te testen of deze laboratoriumbevindingen toepasbaar zijn op echte patiënten, onderzochten de onderzoekers tumoren van 53 mensen met gemetastaseerde heldercellige nierkanker die met Everolimus waren behandeld. Degenen bij wie de ziekte werd gecontroleerd hadden hoge MAGI3- en lage β‑catenine-eiwitniveaus in hun tumoren, terwijl patiënten bij wie de kanker snel vorderde het omgekeerde patroon lieten zien. Lage MAGI3 voorspelde een kortere totale overleving in deze groep. Bij muizen met MAGI3-lage tumoren remde Everolimus alleen of een Wnt-pathwaymiddel alleen de groei slechts bescheiden. Echter, de combinatie van beide behandelingen verkleinde de tumoren dramatisch zonder merkbare bijwerkingen, wat suggereert dat dubbele targeting van deze routes de door MAGI3-verlies veroorzaakte resistentie kan overwinnen.
Wat dit betekent voor toekomstige zorg
Deze studie identificeert MAGI3 als een cruciale interne rem die de Wnt/β‑catenine-groeischakel in heldercellige nierkanker onder controle houdt. Wanneer MAGI3 verloren gaat, ontsnapt β‑catenine aan afbraak, wat metastasering aanjaagt en tumoren minder gevoelig maakt voor mTOR-gerichte medicijnen. Het meten van MAGI3 en β‑catenine in tumormonsters zou artsen daarom kunnen helpen patiënten te identificeren die meer of minder waarschijnlijk profiteren van Everolimus. Belangrijker nog suggereert het werk dat het combineren van mTOR-remmers met middelen die Wnt/β‑catenine-signaal dempen, een sterke nieuwe strategie kan bieden voor patiënten met agressieve, behandelresistente ziekte.
Bronvermelding: Gu, S., Wang, H., Liu, H. et al. MAGI3 deficiency unleashes β-catenin conformational change to drive metastatic progression and mTOR inhibitor resistance in ccRCC. Cell Death Dis 17, 372 (2026). https://doi.org/10.1038/s41419-026-08563-x
Trefwoorden: heldercellige niercelcarcinoom, MAGI3, beta-catenine, resistentie tegen mTOR-remmers, Wnt-signaaltransductie