Clear Sky Science · fr
La déficience en MAGI3 provoque un changement conformationnel de la β-caténine favorisant la progression métastatique et la résistance aux inhibiteurs de mTOR dans le CCRc
Pourquoi cette étude sur le cancer du rein est importante
Le carcinome rénal à cellules claires est l’un des cancers urologiques les plus mortels car il se propage souvent et cesse de répondre aux traitements. Cette étude met au jour un « interrupteur de sécurité » jusque-là caché à l’intérieur des cellules tumorales rénales, une protéine nommée MAGI3, qui maintient sous contrôle un puissant moteur de croissance. Lorsque cet interrupteur est perdu, les tumeurs deviennent plus invasives et résistantes à une classe de médicaments couramment utilisée, les inhibiteurs de mTOR tels que l’Evérolimus. Ces travaux expliquent non seulement pourquoi certains patients évoluent moins bien que d’autres, mais indiquent aussi une voie pratique pour améliorer la thérapie en combinant des médicaments existants.
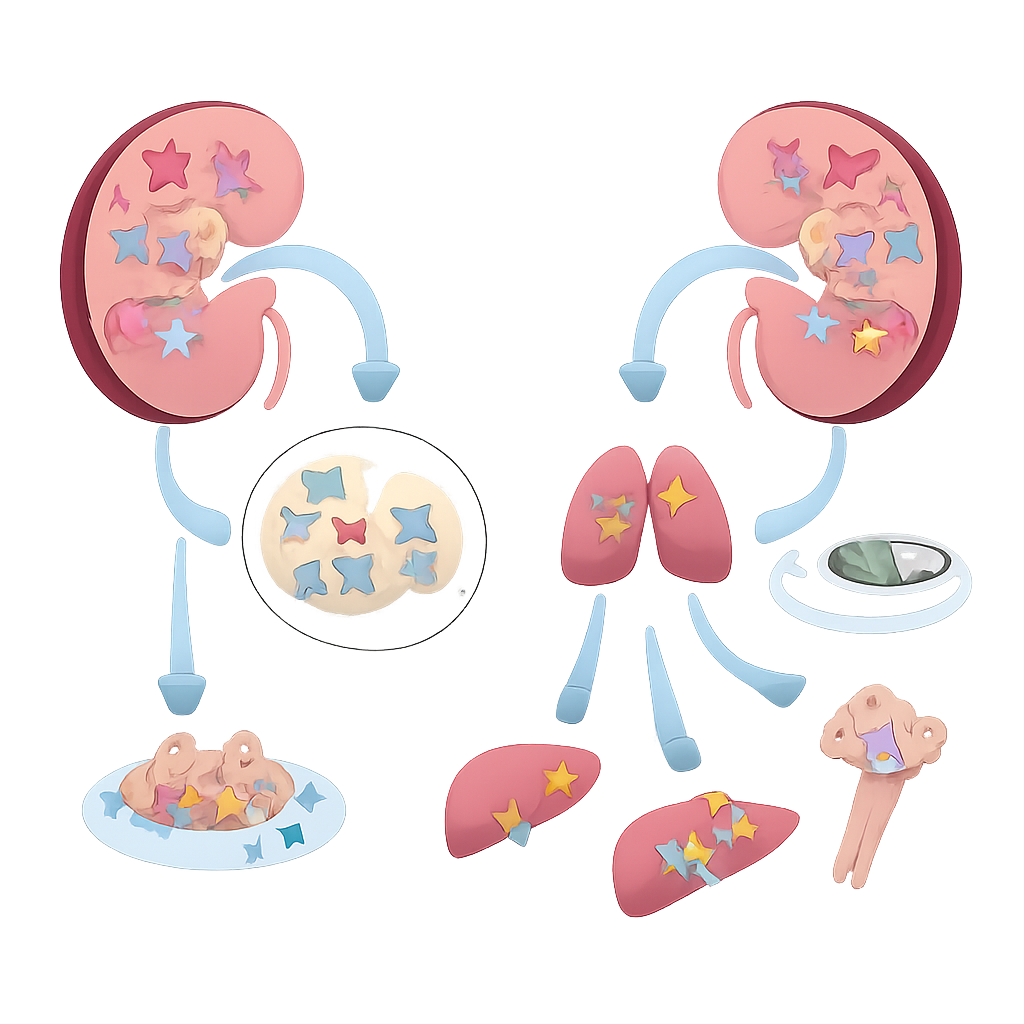
Un gardien manquant dans les tumeurs rénales
Les chercheurs ont commencé par analyser de larges jeux de données publiques sur le cancer afin de rechercher des gènes spécifiquement altérés lorsque le carcinome rénal à cellules claires devient métastatique. Parmi des milliers de candidats, MAGI3 s’est distingué : son activité était plus faible dans le tissu tumoral que dans le rein normal, et encore plus basse dans les tumeurs déjà disséminées. Ces tendances ont été confirmées au niveau protéique sur des échantillons de patients, où la coloration pour MAGI3 était la plus intense dans le rein normal, plus faible dans les tumeurs primitives et la plus faible dans les foyers métastatiques. Les patients dont les tumeurs présentaient une faible expression de MAGI3 avaient tendance à présenter des stades plus avancés, des tumeurs de grade plus élevé et une survie significativement plus courte, indépendamment des altérations génétiques classiques comme les mutations de VHL.
Comment MAGI3 bride un puissant interrupteur de croissance
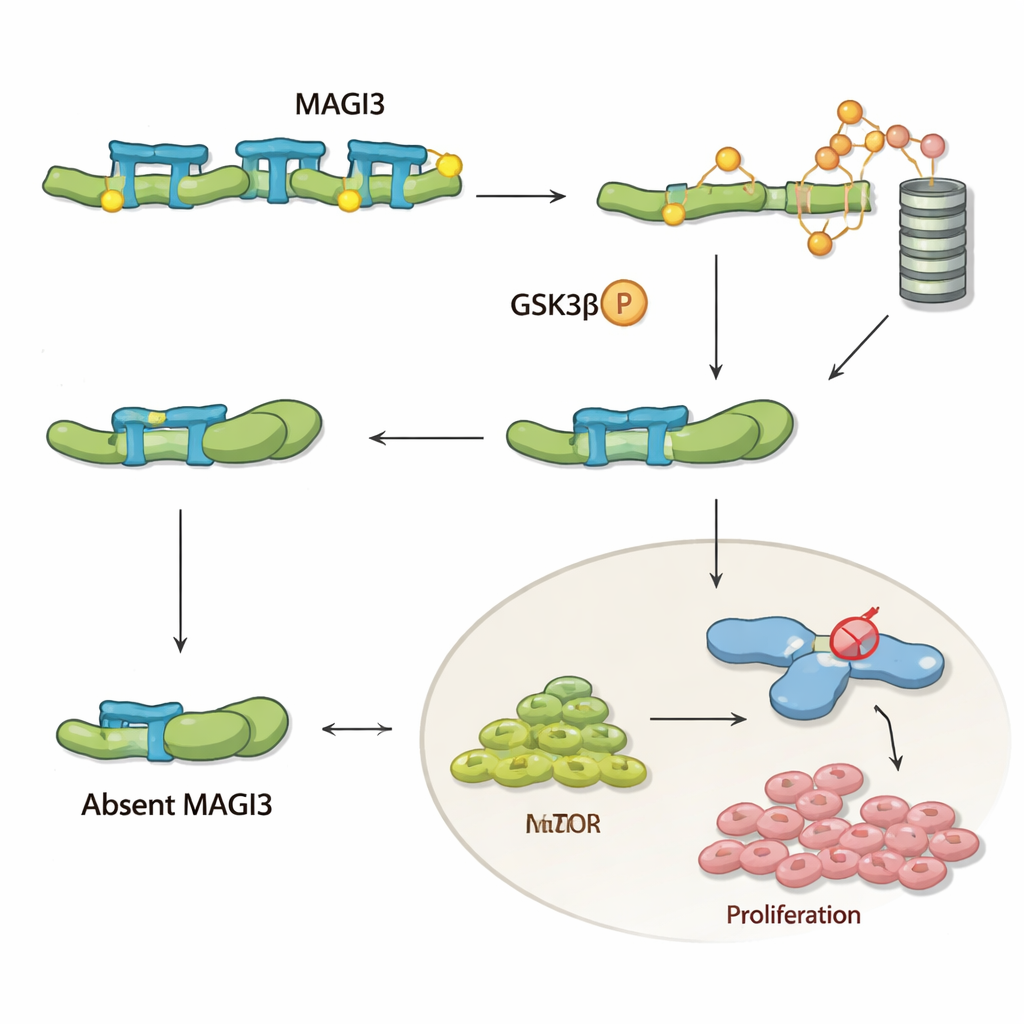
Pour comprendre ce que fait réellement MAGI3 dans les cellules, l’équipe s’est concentrée sur la β‑caténine, un acteur clé de la voie de signalisation Wnt qui favorise la croissance, la survie et la mobilisation cellulaire. Dans de nombreux cancers, la β‑caténine s’accumule et pilote la maladie, mais dans le carcinome rénal à cellules claires, elle est rarement mutée, ce qui suggère que ce sont ses systèmes de régulation qui sont altérés. Les auteurs montrent que MAGI3 se lie physiquement à l’extrémité terminale de la β‑caténine et contraint la protéine à adopter une conformation plus « ouverte ». Cela expose des sites sensibles à l’extrémité opposée de la β‑caténine, permettant à une autre enzyme, GSK‑3β, de la marquer pour destruction par le système d’élimination cellulaire. Lorsque MAGI3 est présent, la β‑caténine est continuellement marquée, démantelée et maintenue à des niveaux sûrs ; quand MAGI3 manque, la β‑caténine reste repliée, échappe à la destruction, s’accumule dans la cellule et active des gènes qui favorisent la croissance et la dissémination tumorales.
Du mouvement cellulaire à la résistance médicamenteuse
Dans des lignées cellulaires de cancer rénal, augmenter l’expression de MAGI3 réduisait la migration et l’invasion dans des essais en laboratoire, tandis que diminuer MAGI3 produisait l’effet inverse. Lorsque des cellules tumorales déficientes en MAGI3 ont été injectées chez des souris, elles ont formé beaucoup plus de métastases pulmonaires, reliant directement la perte de cette protéine à un comportement agressif. L’équipe a ensuite étudié comment cette voie interagit avec les traitements actuels. De nombreux patients atteints d’un carcinome rénal à cellules claires avancé reçoivent des inhibiteurs de mTOR (souvent appelés rapalogs), mais les réponses sont limitées et la résistance fréquente. Ici, l’absence de MAGI3 rendait les cellules cancéreuses nettement moins sensibles à l’Evérolimus, augmentant plusieurs fois la concentration de médicament nécessaire pour ralentir la croissance. De manière cruciale, bloquer la signalisation Wnt/β‑caténine dans ces cellules déficientes en MAGI3 a restauré leur sensibilité à l’Evérolimus et réduit fortement leur capacité d’invasion.
Preuves issues de patients et de modèles animaux
Pour vérifier si ces observations en laboratoire se traduisent chez les patients, les chercheurs ont examiné les tumeurs de 53 personnes atteintes de carcinome rénal à cellules claires métastatique traitées par Evérolimus. Ceux dont la maladie était contrôlée présentaient une forte expression de MAGI3 et une faible expression de β‑caténine dans leurs tumeurs, tandis que les patients dont le cancer progressait rapidement montraient le schéma inverse. Une faible expression de MAGI3 prédisait une survie globale plus courte dans ce groupe. Chez des souris porteuses de tumeurs à faible MAGI3, l’Evérolimus seul ou un médicament ciblant la voie Wnt seul ralentissait la croissance de manière seulement modeste. En revanche, la combinaison des deux traitements réduisait drastiquement la taille des tumeurs sans effets secondaires notables, suggérant que le ciblage conjoint de ces voies peut surmonter la résistance induite par la perte de MAGI3.
Ce que cela signifie pour les soins futurs
Cette étude révèle MAGI3 comme un frein interne crucial qui maintient l’interrupteur de croissance Wnt/β‑caténine sous contrôle dans le carcinome rénal à cellules claires. Quand MAGI3 est perdu, la β‑caténine échappe à la destruction, alimentant la métastase et rendant les tumeurs moins sensibles aux médicaments ciblant mTOR. Mesurer MAGI3 et la β‑caténine dans les échantillons tumoraux pourrait donc aider les médecins à identifier les patients plus ou moins susceptibles de bénéficier de l’Evérolimus. Plus important encore, ces travaux suggèrent que combiner des inhibiteurs de mTOR avec des médicaments qui atténuent la signalisation Wnt/β‑caténine pourrait offrir une nouvelle stratégie puissante pour les patients atteints de maladies agressives et résistantes aux traitements.
Citation: Gu, S., Wang, H., Liu, H. et al. MAGI3 deficiency unleashes β-catenin conformational change to drive metastatic progression and mTOR inhibitor resistance in ccRCC. Cell Death Dis 17, 372 (2026). https://doi.org/10.1038/s41419-026-08563-x
Mots-clés: carcinome rénal à cellules claires, MAGI3, beta-caténine, résistance aux inhibiteurs de mTOR, signalisation Wnt