Clear Sky Science · ar
نقص MAGI3 يطلق تغيرًا تَشكّليًا في β‑catenin يدفع التقدم النقِيلي ومقاومة مثبطات mTOR في سرطان الكلية ذو الخلايا الشفافة
لماذا تهم هذه الدراسة عن سرطان الكلية
سرطان الكلية ذو الخلايا الشفافة هو من أخطر سرطانات المسالك البولية لأنه غالبًا ما ينتشر ويتوقف عن الاستجابة للعلاج. تكشف هذه الدراسة عن "مفتاح أمان" خفي داخل خلايا الورم الكلوية، وهو بروتين يُدعى MAGI3، يحافظ على ضبط محرك نمو قوي. عند فقدان هذا المفتاح، تصبح الأورام أكثر اختراقًا ومقاومة لفئة أدوية مستخدمة شائعًا، مثبطات mTOR مثل الإفيروليموس. العمل لا يفسر فقط لماذا يسير الحال أسوأ لبعض المرضى، بل يشير أيضًا إلى طريقة عملية لتحسين العلاج من خلال الجمع بين أدوية متاحة.
حارس مفقود في أورام الكلية
بدأ الباحثون بتفحُّص مجموعات بيانات سرطانية عامة كبيرة للبحث عن جينات تتغير على نحو خاص عندما يصبح سرطان الكلية ذو الخلايا الشفافة نقيليًا. بين آلاف المرشحين، برز MAGI3: كان نشاطه أقل في نسيج الورم مقارنةً بالكلية الطبيعية، وأقل حتى في الأورام التي كانت قد انتشرت بالفعل. تَأكدت هذه الأنماط على مستوى البروتين في عينات المرضى، حيث كان تلوين MAGI3 أقوى في نسيج الكلية الطبيعي، وأضعف في الأورام الأولية، والأضعف في الترصيّات النقيليّة. ميّز المرضى الذين كانت أورامهم منخفضة MAGI3 بمرض أكثر تقدمًا، ودرجة أعلى، وبقاء أقصر بشكل ملحوظ، بغض النظر عن التغيرات الجينية الكلاسيكية مثل طفرات VHL.
كيف يكبح MAGI3 مفتاح نمو قوي
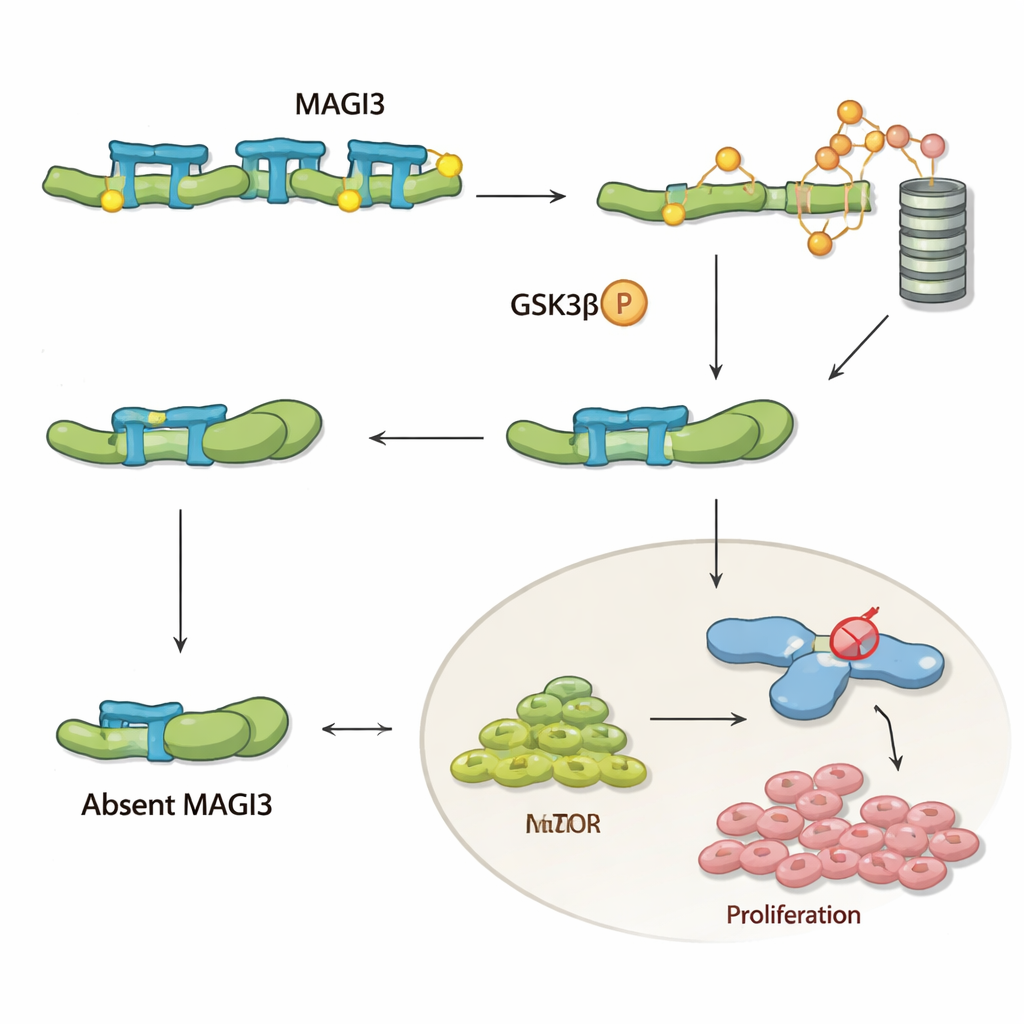
لفهم ما يفعله MAGI3 داخل الخلايا، ركز الفريق على β‑catenin، لاعب رئيسي في مسار إشارة Wnt الذي يعزز نمو الخلايا وبقائها وحركتها. في العديد من السرطانات، يتراكم β‑catenin ويقود المرض، لكن في سرطان الكلية ذو الخلايا الشفافة نادرًا ما يُطرأ عليه طفرات، ما يوحي بأن أنظمة ضبطه تتغير بدلًا من ذلك. تُظهر الدراسة أن MAGI3 يرتبط جسديًا بذيل β‑catenin ويجبر البروتين على اتخاذ شكل أكثر "انفتاحًا". هذا يعرض مواقع حساسة عند الطرف المقابل من β‑catenin، ما يسمح لإنزيم آخر، GSK‑3β، بوسمه لتدميره عبر آلية التخلص الخلوية. عندما يكون MAGI3 حاضرًا، يُوسم β‑catenin باستمرار، ويُفكك، ويُحافظ على مستوَيات آمنة؛ وعندما يختفي MAGI3، يبقى β‑catenin مطويًا، يفلت من الدمار، يتراكم داخل الخلية، ويُشغّل جينات تُساعد الأورام على النمو والانتشار.
من حركة الخلايا إلى مقاومة الدواء
في خطوط خلايا سرطان الكلية، أدت زيادة MAGI3 إلى تقليل الهجرة والاختراق في تجارب المختبر، بينما كان لانخفاض MAGI3 التأثير المعاكس. عندما حُقنت خلايا ورمية ناقصة MAGI3 في فئران، شكلت عددًا أكبر بكثير من الانبثاثات الرئوية، رابطًا فقدان هذا البروتين بسلوك عدواني. سپس سأل الفريق كيف يتقاطع هذا المسار مع العلاجات الحالية. يتلقى العديد من المرضى المصابين بسرطان الكلية ذو الخلايا الشفافة المتقدم مثبطات mTOR (المعروفة غالبًا بالـ rapalogs)، لكن الاستجابات محدودة والمقاومة شائعة. هنا، جعل فقدان MAGI3 الخلايا السرطانية أقل حساسية بكثير لمثبط mTOR الإفيروليموس، رافعًا تركيز الدواء المطلوب لإبطاء النمو بعدة أضعاف. والأهم من ذلك، أن حجب إشارة Wnt/β‑catenin في هذه الخلايا ناقصة MAGI3 استعاد حساسيتها للإفيروليموس وقصّر بشدة قدرتها على الاختراق.
دليل من المرضى والنماذج الحيوانية
لاختبار ما إذا كانت هذه النتائج المختبرية تنطبق على المرضى الحقيقيين، فحص الباحثون أورام 53 شخصًا مصابًا بسرطان الكلية ذو الخلايا الشفافة النقيلي والمعالجين بالإفيروليموس. أولئك الذين تمت السيطرة على مرضهم كان لديهم MAGI3 مرتفع وβ‑catenin منخفض في أورامهم، بينما أظهر المرضى الذين تقدّم سرطانهم بسرعة النمط المعاكس. تنبأ انخفاض MAGI3 بفترة بقاء كلية أقصر في هذه المجموعة. في الفئران الحاملة لأورام منخفضة MAGI3، كان الإفيروليموس وحده أو دواء مُعادل لمسار Wnt وحده يُبطئ النمو بشكل طفيف فقط. ومع ذلك، أدى الجمع بين العلاجين إلى انكماش الأورام بدرجة كبيرة دون التسبب في آثار جانبية واضحة، ما يوحي بأن الاستهداف المزدوج لهذه المسارات يمكن أن يتغلب على المقاومة الناتجة عن فقدان MAGI3.
ماذا يعني هذا للرعاية المستقبلية
تكشف هذه الدراسة أن MAGI3 يعمل كفرامل داخلية حاسمة تحافظ على ضبط مفتاح نمو Wnt/β‑catenin في سرطان الكلية ذو الخلايا الشفافة. عند فقدان MAGI3، يفلت β‑catenin من الدمار، مما يوقِد الانبثاث ويجعل الأورام أقل استجابة للأدوية المستهدفة لـ mTOR. لذلك قد يساعد قياس MAGI3 وβ‑catenin في عينات الورم الأطباء على تحديد المرضى الأكثر أو الأقل احتمالًا للاستفادة من الإفيروليموس. والأهم من ذلك، تشير النتائج إلى أن الجمع بين مثبطات mTOR والأدوية التي تخفف إشارة Wnt/β‑catenin قد يوفر استراتيجية جديدة قوية للمرضى ذوي الأورام العدوانية والمقاومة للعلاج.
الاستشهاد: Gu, S., Wang, H., Liu, H. et al. MAGI3 deficiency unleashes β-catenin conformational change to drive metastatic progression and mTOR inhibitor resistance in ccRCC. Cell Death Dis 17, 372 (2026). https://doi.org/10.1038/s41419-026-08563-x
الكلمات المفتاحية: سرطان الكلية ذو الخلايا الشفافة, MAGI3, بيتا‑كاتينين, مقاومة مثبطات mTOR, إشارة Wnt