Clear Sky Science · tr
SLIT3: Akt/GSK3β/β-katenin sinyal yoluyla odontojenik farklılaşmanın yeni bir düzenleyicisi
Bu diş öyküsü neden önemli
Birçok çocuk ve ergen, hâlâ gelişmekte olan bir dişin içindeki pulpayı öldüren travmalar veya derin çürükler yaşar. Bu olduğunda, kök büyümesi durabilir ve kısa, kırılgan bir diş geride kalabilir; bu da kolayca kırılmaya yol açar. Bu çalışma, SLIT3 adlı doğal bir proteini ve bunun genç dişlerin ucundaki özel kök hücrelerinin daha sağlam kök dentini inşa etmesine nasıl yardımcı olduğunu inceliyor; bu bulgular, hasarlı genç dişlerin kaybolmak yerine büyümeye devam etmesine yardımcı olabilecek gelecekteki tedavilere işaret ediyor.
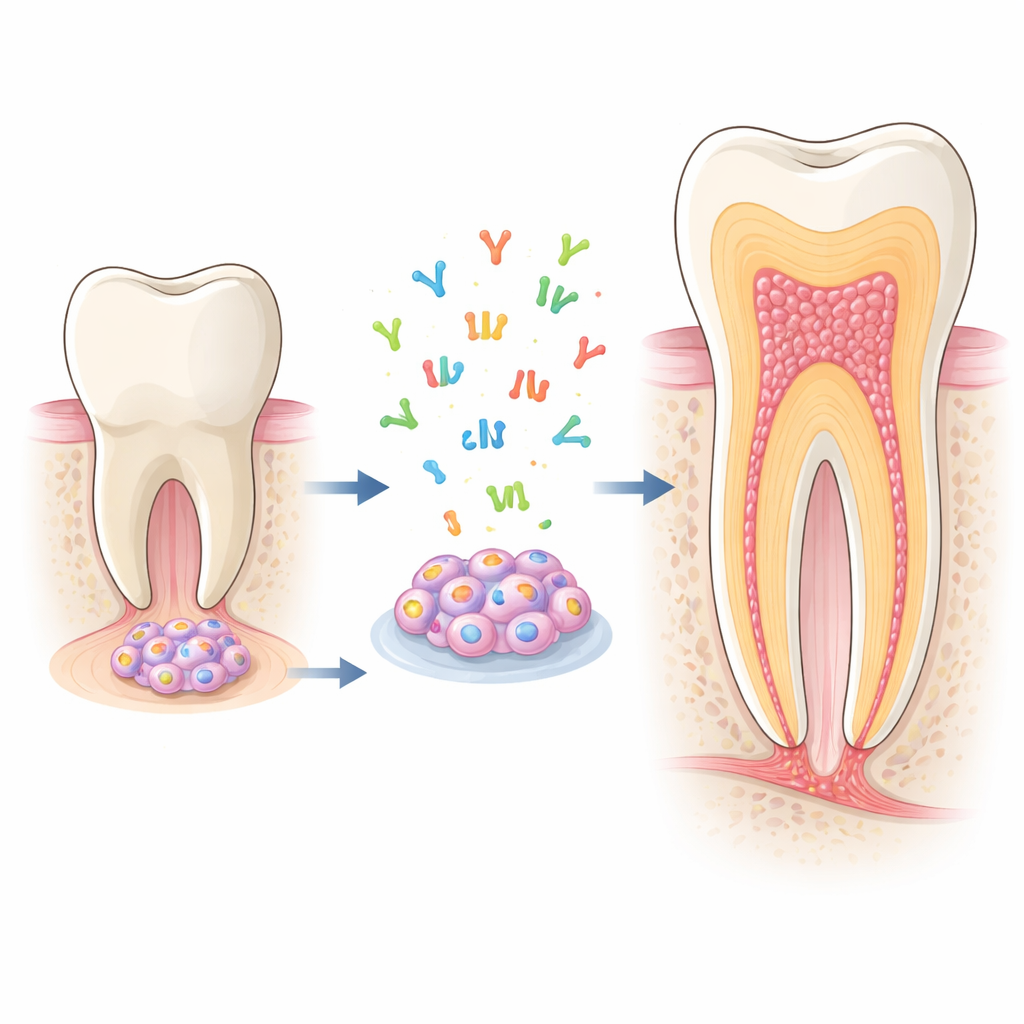
Genç dişlerin içindeki gizli yapıcılar
Olgunlaşmakta olan bir diş kökünün büyüme ucunda apikal papilla adı verilen yumuşak bir doku bulunur. Burada apikal papilladan kök hücreler (SCAP) yer alır; bu hücreler birkaç tür dişi destekleyici hücreye, özellikle dentini oluşturan odontoblastlara dönüşebilir—dentin, dişin çoğunu oluşturan sert dokudur. SCAP laboratuvarda iyi çoğalır ve kolaylıkla odontoblast-benzeri hücrelere dönüşebildiği için, köklerin nasıl geliştiğini ve hastalık ya da yaralanma sonrası nasıl kendilerini onarmaya teşvik edilebileceklerini incelemek için ideal bir modeldir.
Yeni bir işleve sahip bir yönlendirme proteini
SLIT3, beyin gelişimi sırasında sinir liflerinin yollarını bulmasına yardımcı olan bir yönlendirme işareti olarak daha çok bilinir ve ayrıca kemik yıkımını yeni kemik oluşumuyla bağlar. Kemik ve dentin birçok yapı kuralını paylaştığından, araştırmacılar SLIT3’ün dişlerde dentin oluşumunu da yönlendirip yönlendirmediğini sordular. Farklı evrelerdeki fare diş tomurcuklarından alınan tek hücre RNA sıralama verilerini yeniden analiz ederek, Slit3 geninin esas olarak dişin iç destek dokusunda (dental mezankim) aktif olduğunu, dış epitelyumda ise olmadığını buldular. Buna karşın SLIT3 proteini kendisi dentin oluşturan odontoblastlarda ve mine oluşturan ameloblastlarda güçlü biçimde görünüyordu; bu da proteinin salgılanıp yakın hücrelerde sert doku oluşumunu koordine etmek için etki ettiğine işaret ediyor.
Kök hücrelerin büyümesine ve sertleşmesine yardım etmek
SLIT3’ün rolünü doğrudan test etmek için ekip, olgunlaşmamış 20’lik dişlerden insan SCAP izole etti ve dentin oluşumunu teşvik eden koşullarda büyüttü. Bu hücreler olgunlaştıkça hem SLIT3 gen hem de protein düzeyleri düzenli olarak arttı. Araştırmacılar SLIT3’ü küçük enterferans RNA’ları ile yapay olarak düşürdüklerinde, SCAP daha yavaş çoğaldı ve daha zayıf mineralleşme gösterdi; iki ana dentin proteini olan DMP-1 ve DSPP düzeyleri azaldı. Buna karşılık, ekstra insan SLIT3 proteini eklemek SCAP’ın daha hızlı büyümesini, mineralleşmenin artmasını ve DMP-1 ile DSPP’nin yükselmesini sağladı. Daha fazla veya daha az SLIT3’e sahip SCAP’lar farelerde küçük seramik iskeletlere nakledildiğinde, yüksek-SLIT3 yapıların daha zengin dentin-benzeri doku ürettiği, düşük-SLIT3 yapıların ise daha zayıf doku ürettiği görüldü; bu da SLIT3’ün canlı sistemlerdeki önemini doğruladı.
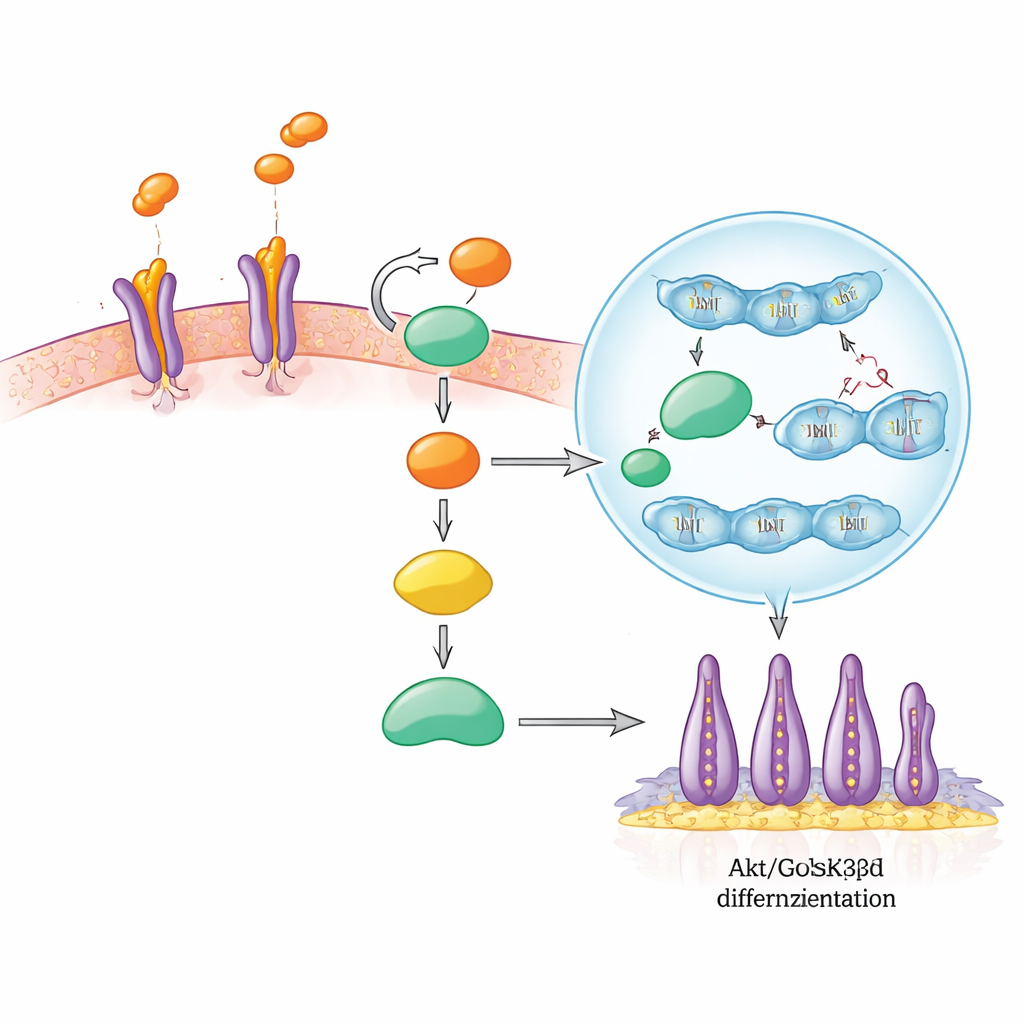
Hücrenin karar devre içindeki izleri
Araştırmacılar daha sonra SLIT3’ün SCAP içinde tetiklediği sinyal zincirini izlediler. SLIT3 ilk olarak hücre yüzeyindeki ROBO2 ve ROBO3 reseptörlerine bağlanır; bu, bir anahtarın kilidi çevirmesi gibidir. Bu, Akt adı verilen iyi bilinen bir büyüme ve hayatta kalma merkezini aktive eder; Akt daha sonra başka bir protein olan GSK3β’yi kapatır. Normalde aktif GSK3β, haberci β-katenini yok edilmek üzere işaretlemeye yardımcı olur. GSK3β kapandığında β-katenin birikir ve hücre çekirdeğine taşınır; burada diğer faktörlerle birlikte hücre bölünmesi ve farklılaşmayı yönlendiren genleri açar. Bu çalışmada, SLIT3 uyarımı hızla Akt ve GSK3β fosforilasyonunu artırdı, çekirdek β-katenini yükseltti ve büyümeyle ilişkili β-katenin hedef proteinlerinin düzeylerini yükseltti. ROBO2/ROBO3 bloke edildiğinde bu değişiklikler engellendi; bu da sinyalin geçmesi için bu reseptörlerin gerekli olduğunu gösterdi.
Yolun gerçekten önemli olduğunu kanıtlamak
Bu iç devrenin sadece yan etki olmadığını, dentin oluşumu için gerçekten gerekli olduğunu göstermek amacıyla ekip, Akt/GSK3β/β-katenin yolunu bloke etmek için Resibufogenin adlı bir kimyasal kullandı. Bu yol engellendiğinde, SLIT3 artık çekirdekte β-katenini artıramıyor ya da DMP-1 ve DSPP düzeylerini yükseltemiyordu ve odontojenik farklılaşmayı artırma yeteneği esasen kayboldu. Reseptör deneyleriyle birlikte, bu bulgular SLIT3’ün ROBO2/3 aracılığıyla Akt/GSK3β/β-katenin anahtarını açtığı ve bunun da SCAP’a çoğalmalarını ve dentin üreten hücrelere olgunlaşmalarını söylediği modelini güçlü biçimde destekliyor.
Gelecekteki diş onarımı için ne anlama geliyor
Bu çalışma, kök ucunda dentin oluşumunun yeni bir düzenleyicisi olarak SLIT3’ü konumlandırıyor ve diş köklerinin nasıl büyüdüğüne ve sertleştiğine dair haritamızı genişletiyor. Hasarlı, olgunlaşmamış dişleri olan hastalar için, bu SLIT3-odaklı yolu anlamak nihayetinde dişin kendi kök hücrelerini kök dentinini inşa etmeye devam etmeye teşvik eden biyolojik temelli tedavileri ilham verebilir. Herhangi bir klinik uygulama çok daha fazla araştırma gerektirecek olsa da, bu çalışma genç dişlerin nasıl geliştiğine ve onların kendi kendilerini nasıl iyileştirmelerine yardımcı olabileceğimize dair eksik bir anahtarı daha ekliyor.
Atıf: Jiang, L., Liu, L., Yang, F. et al. SLIT3: a novel regulator of odontogenic differentiation through Akt/GSK3β/β-catenin signaling pathway. Int J Oral Sci 18, 35 (2026). https://doi.org/10.1038/s41368-026-00426-7
Anahtar kelimeler: diş kökü rejenerasyonu, dentin oluşumu, diş kök hücreleri, SLIT3 sinyalizasyonu, Wnt beta-katenin yolu