Clear Sky Science · ar
SLIT3: منظم جديد للتمايز السني عبر مسار إشارات Akt/GSK3β/β-catenin
لماذا تهم قصة هذا السن
يتعرض العديد من الأطفال والمراهقين لإصابات أو تجاويف عميقة تقتل لب السن داخل سن لا يزال في طور النمو. عندما يحدث ذلك، قد يتوقف الجذر عن النمو، مما يترك سنًا قصيرة وهشة يمكن أن تنكسر بسهولة. تستكشف هذه الدراسة بروتينًا طبيعيًا يُدعى SLIT3 وكيف يساعد خلايا جذعية خاصة عند طرف الأسنان النامية على بناء عاج جذر أقوى، مما يشير إلى علاجات مستقبلية قد تساعد الأسنان الشابة المتضررة على الاستمرار في النمو بدلاً من فقدانها.
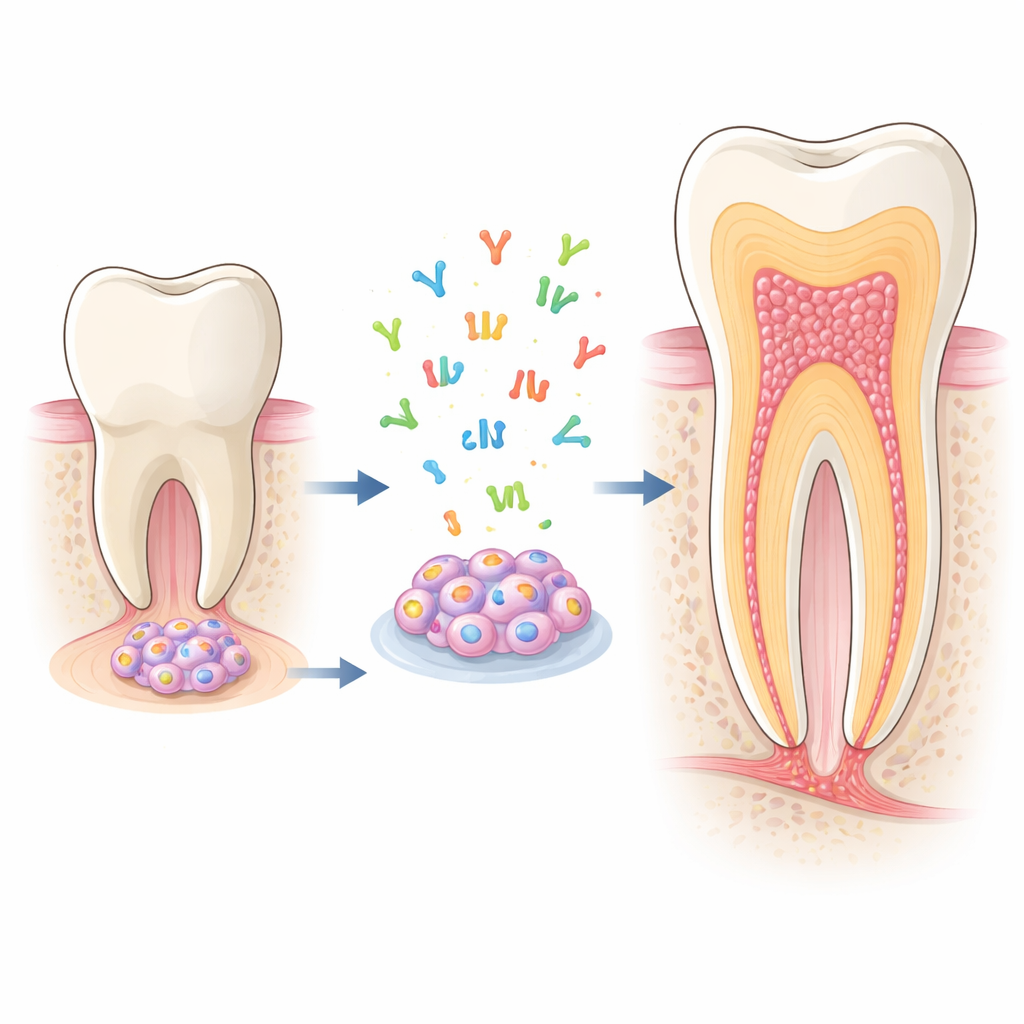
البنّاؤون الخفيون داخل الأسنان الشابة
في طرف جذر السن غير المكتمل يوجد نسيج رخوي يسمى الحُليمة القِمية. يحتوي هذا النسيج على خلايا جذعية من الحليمة القِمية (SCAP)، التي يمكن أن تتحول إلى عدة أنواع من الخلايا الداعمة للسن، وخصوصًا الخلايا السنية المفرزة للعاج (odontoblasts)—الخلايا التي تفرز العاج، وهو النسيج الصلب الذي يشكل معظم السن. وبما أن SCAP تنمو جيدًا في المختبر ويمكن أن تصبح بسهولة خلايا شبيهة بالأودونتوبلاست، فهي نموذج مثالي لدراسة كيفية تطور الجذور وكيف يمكننا حثها على إصلاح نفسها بعد المرض أو الإصابة.
بروتين إرشادي بوظيفة جديدة
يشتهر SLIT3 كمؤشر إرشادي يساعد ألياف الأعصاب على إيجاد مساراتها أثناء تطور الدماغ، كما يربط بين تكسّر العظم وتكوّن عظم جديد. وبما أن العظم والعاج يشتركان في العديد من قواعد البناء، تساءل الباحثون عما إذا كان SLIT3 قد يوجه أيضًا تكوّن العاج في الأسنان. من خلال إعادة تحليل بيانات تسلسل الرنا المفردة لخلايا جراثيم الأسنان في الفئران عبر مراحل مختلفة، وجدوا أن جين Slit3 نشط بشكل رئيسي في النسيج الداعم الداخلي للسن (المِزمَقة السنية)، وليس في الطبقة الظهارية الخارجية. ومع ذلك، ظهر بروتين SLIT3 نفسه بقوة على كل من الأودونتوبلاست المكوّنة للعاج والأميلايبوست المكوّنة للمينا، مما يوحي بأنه يُفرَز ثم يعمل على الخلايا المجاورة لتنسيق تكوّن النسيج الصلب.
مساعدة الخلايا الجذعية على النمو والتصلب
لاختبار دور SLIT3 مباشرة، عزّل الفريق خلايا SCAP بشرية من ضروس العقل غير الناضجة ونماها في ظروف تشجع تكوّن العاج. مع نضوج هذه الخلايا، ارتفعت مستويات جين وبروتين SLIT3 تدريجيًا. عندما خفّض الباحثون SLIT3 اصطناعيًا باستخدام رنا متداخل صغير، تكاثرت SCAP ببطء أكبر وشكلت ترسّبات معدنية أضعف، مع انخفاض مستويات بروتينين رئيسيين للعاج، DMP-1 وDSPP. على النقيض من ذلك، أضافت إضافة بروتين SLIT3 البشري خارجياً إلى تسريع نمو SCAP، وتعزيز التمعدن، وزيادة DMP-1 وDSPP. عندما نُقلت SCAP ذات مستويات أعلى أو أقل من SLIT3 في هياكل خزفية دقيقة داخل فئران، أنتجت التركيبات ذات SLIT3 العالي نسيجًا أشبه بالعاج أغنى، بينما أنتجت التركيبات منخفضة SLIT3 نسيجًا أفقر، مؤكدة أهمية SLIT3 في الأنظمة الحية.
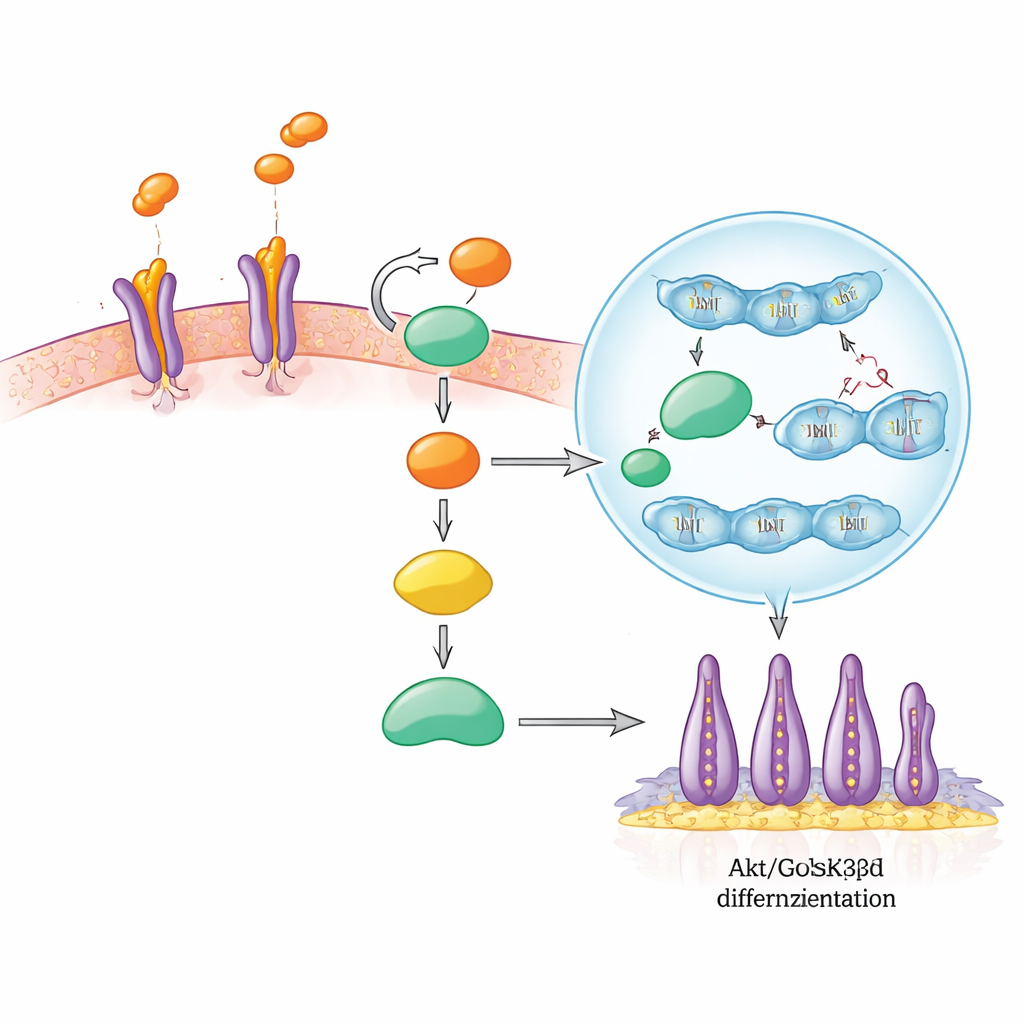
داخل دائرة القرار الخلوية
تابع الباحثون بعد ذلك سلسلة الإشارات التي يثيرها SLIT3 داخل SCAP. يرتبط SLIT3 أولًا بمستقبلات ROBO2 وROBO3 على سطح الخلية، تمامًا كما تدير المفتاح في قفل. هذا ينشط محورًا معروفًا للنمو والبقاء يسمى Akt، الذي يوقف بدوره بروتينًا آخر، GSK3β. عادةً، يساعد GSK3β النشط على تعليم رسالة β-catenin للتخلص منها. عندما يُطفأ GSK3β، يتراكم β-catenin وينتقل إلى نواة الخلية، حيث يتشارك مع عوامل أخرى لتشغيل جينات تدفع انقسام الخلايا وتخصصها. في هذه الدراسة، زادت تحفيزات SLIT3 بسرعة فسفرة Akt وGSK3β، وعزّزت وجود β-catenin النووي، ورفعت مستويات بروتينات مستهدفة لβ-catenin مرتبطة بالنمو. منعت حجب ROBO2/ROBO3 هذه التغيرات، مما يوضح أن هذه المستقبلات ضرورية لمرور الإشارة.
إثبات أن المسار مهم فعلًا
لإظهار أن هذه الدائرة الداخلية ليست مجرد أثر جانبي بل مطلوبة فعلاً لتكوين العاج، استخدم الفريق مركبًا كيميائيًا يُدعى Resibufogenin لحجب طريق Akt/GSK3β/β-catenin. عندما تم تثبيط هذا المسار، لم يعد بإمكان SLIT3 زيادة β-catenin في النواة أو رفع مستويات DMP-1 وDSPP، وفقدت قدرته على تعزيز التمايز العظمي السني أساسًا. مع تجارب المستقبلات، يدعم هذا بقوة نموذجًا يعمل فيه SLIT3 عبر ROBO2/3 لتشغيل مفتاح Akt/GSK3β/β-catenin، والذي بدوره يخبر SCAP بالتكاثر والنضوج إلى خلايا منتجة للعاج.
ماذا يعني هذا لإصلاح الأسنان في المستقبل
تضع هذه الدراسة SLIT3 كمنظم جديد لتكوين العاج عند طرف الجذر، مطوّلة خريطة فهمنا لكيفية نمو وتقسية جذور الأسنان. بالنسبة للمرضى ذوي الأسنان غير الناضجة المتضررة، قد يلهم فهم هذا المسار المرتكز على SLIT3 في نهاية المطاف علاجات حيوية تشجع خلايا السن الجذعية على مواصلة بناء عاج الجذر. وبينما ستتطلّب أي تطبيقات سريرية مزيدًا كبيرًا من البحث، تضيف هذه الدراسة قطعة أساسية مفقودة في لغز كيفية تطور الأسنان الشابة—وكيف قد نساعدها على الشفاء الذاتي.
الاستشهاد: Jiang, L., Liu, L., Yang, F. et al. SLIT3: a novel regulator of odontogenic differentiation through Akt/GSK3β/β-catenin signaling pathway. Int J Oral Sci 18, 35 (2026). https://doi.org/10.1038/s41368-026-00426-7
الكلمات المفتاحية: تجدد جذر السن, تكوّن العاج, خلايا جذعية سنية, إشارة SLIT3, مسار Wnt بيتا-كاتينين