Clear Sky Science · fr
SLIT3 : un nouveau régulateur de la différenciation odontogénique via la voie de signalisation Akt/GSK3β/β-caténine
Pourquoi cette histoire de dent est importante
De nombreux enfants et adolescents subissent des traumatismes ou des caries profondes qui détruisent la pulpe d’une dent encore en développement. Dans ces cas, la racine peut cesser de croître, laissant une dent courte et fragile, susceptible de se casser facilement. Cette étude explore une protéine naturelle appelée SLIT3 et la façon dont elle aide des cellules souches particulières situées à l’extrémité des dents jeunes à construire une dentine radiculaire plus résistante, ouvrant la voie à de futurs traitements qui pourraient permettre aux dents endommagées des jeunes de continuer à pousser plutôt que d’être perdues.
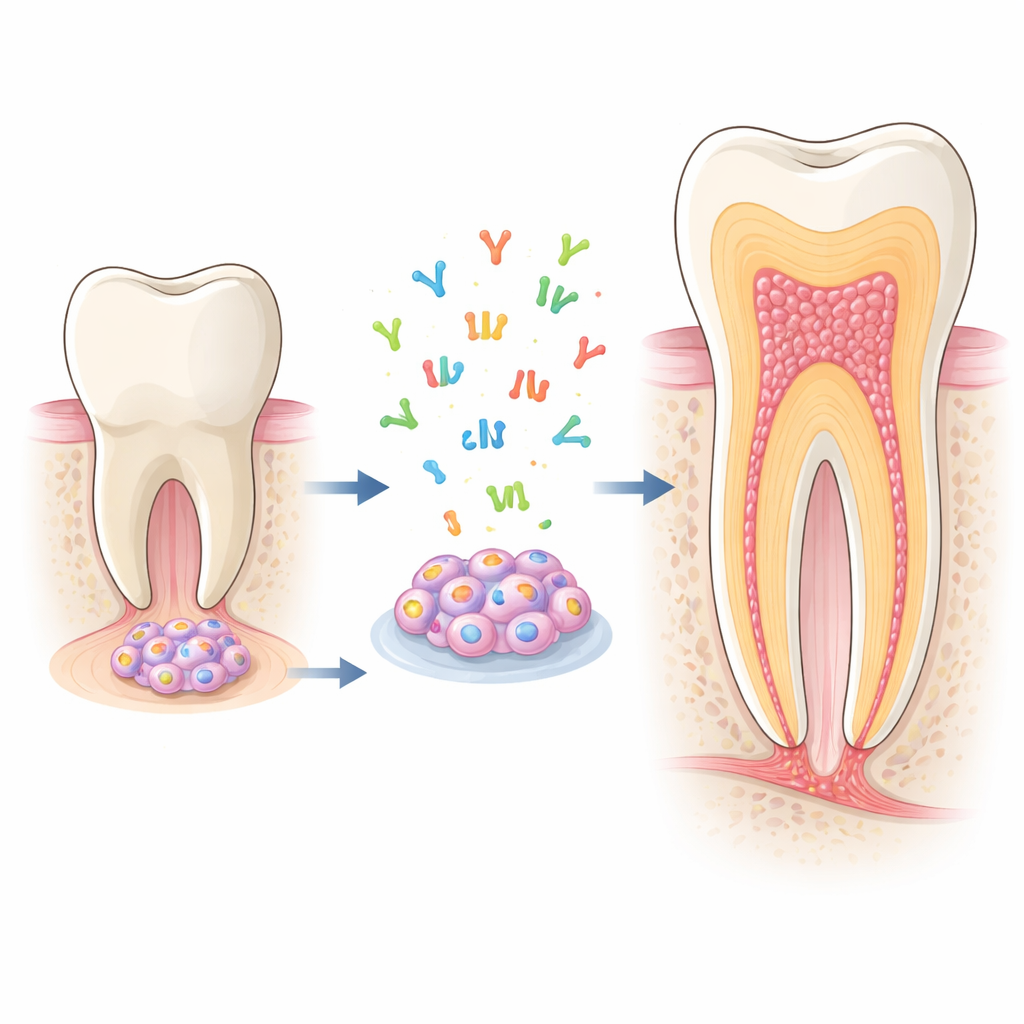
Des constructeurs cachés à l’intérieur des dents jeunes
À l’extrémité en croissance d’une racine dentaire immature se trouve un tissu mou appelé papille apicale. Il abrite des cellules souches de la papille apicale (SCAP), capables de se différencier en plusieurs types cellulaires de soutien dentaire, en particulier les odontoblastes — les cellules qui déposent la dentine, le tissu dur constituant la majeure partie de la dent. Parce que les SCAP se développent bien en culture et peuvent facilement devenir des cellules de type odontoblaste, elles constituent un modèle idéal pour étudier comment les racines se développent et comment on pourrait les inciter à se réparer après une maladie ou une blessure.
Une protéine guide avec un nouveau rôle
SLIT3 est surtout connue comme un signal guide aidant les fibres nerveuses à trouver leur chemin lors du développement cérébral, et elle relie également la résorption osseuse à la formation osseuse. Comme l’os et la dentine partagent de nombreuses règles de construction, les chercheurs se sont demandé si SLIT3 pouvait aussi guider la formation de la dentine dans les dents. En réanalysant des données de séquençage ARN unicellulaire de bourgeons dentaires de souris à différents stades, ils ont trouvé que le gène Slit3 est exprimé principalement dans le tissu de soutien interne de la dent (mésenchyme dentaire), et non dans l’épithélium externe. Pourtant, la protéine SLIT3 elle‑même était fortement détectée à la fois sur les odontoblastes formant la dentine et sur les améloblastes formant l’émail, ce qui suggère qu’elle est sécrétée puis agit sur les cellules voisines pour coordonner la formation des tissus durs.
Favoriser la croissance et la minéralisation des cellules souches
Pour tester directement le rôle de SLIT3, l’équipe a isolé des SCAP humaines à partir de dents de sagesse immatures et les a cultivées dans des conditions favorisant la formation de dentine. À mesure que ces cellules maturaient, les niveaux d’ARN et de protéine SLIT3 augmentaient régulièrement. Lorsque les chercheurs ont artificiellement réduit SLIT3 à l’aide de petits ARN interférents, les SCAP proliféraient plus lentement et formaient des dépôts minéraux plus faibles, avec des niveaux réduits de deux protéines clés de la dentine, DMP‑1 et DSPP. En revanche, l’ajout de protéine humaine SLIT3 supplémentaire a accéléré la croissance des SCAP, renforcé la minéralisation et augmenté DMP‑1 et DSPP. Lorsque des SCAP avec plus ou moins de SLIT3 ont été transplantées dans de petits échafaudages céramiques chez la souris, les constructions riches en SLIT3 ont produit un tissu proche de la dentine plus abondant, tandis que les constructions pauvres en SLIT3 ont donné un tissu de moindre qualité, confirmant l’importance de SLIT3 in vivo.
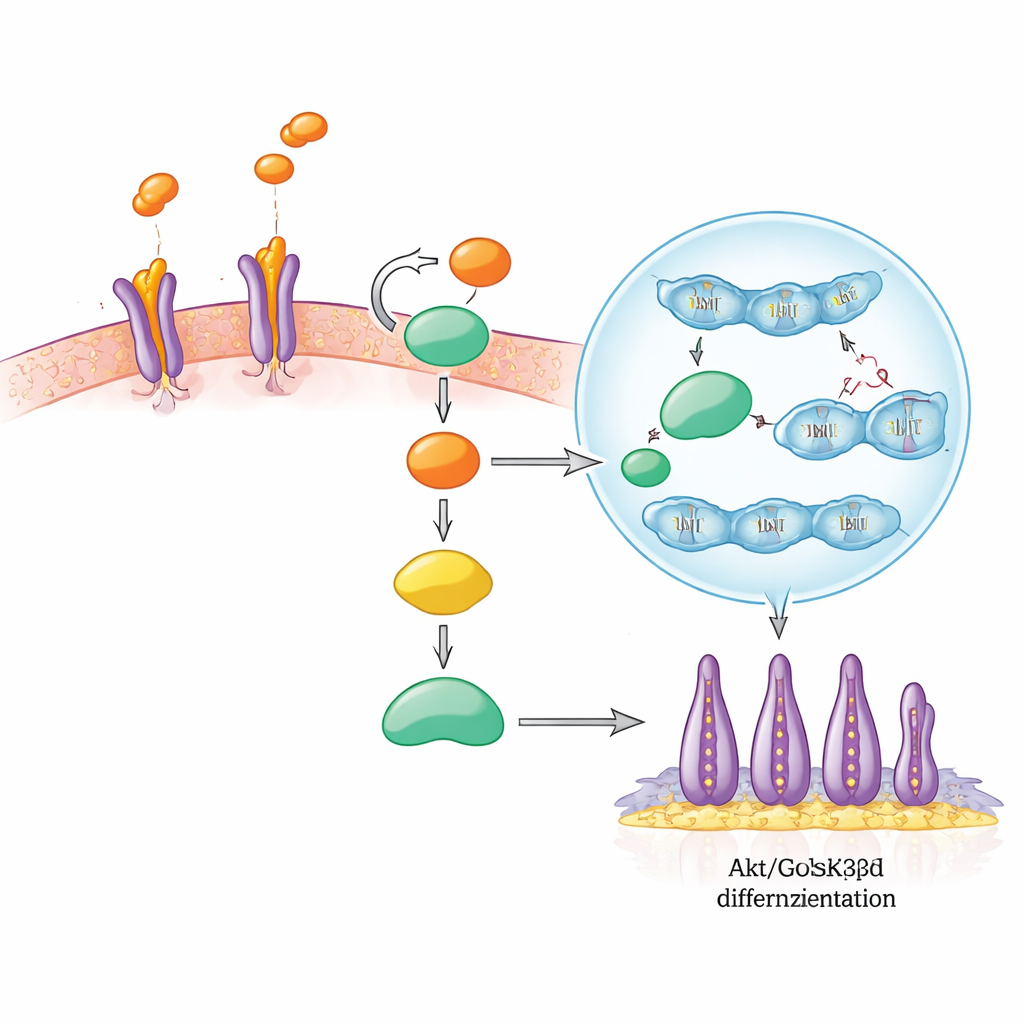
Dans le circuit de décision de la cellule
Les chercheurs ont ensuite suivi la chaîne de signaux déclenchée par SLIT3 à l’intérieur des SCAP. SLIT3 se lie d’abord aux récepteurs ROBO2 et ROBO3 à la surface cellulaire, un peu comme une clé tournant une serrure. Cela active un pôle bien connu de croissance et de survie appelé Akt, qui désactive ensuite une autre protéine, GSK3β. Normalement, la GSK3β active aide à marquer le messager β‑caténine pour sa destruction. Lorsque GSK3β est désactivée, β‑caténine s’accumule et migre dans le noyau cellulaire, où elle s’associe à d’autres facteurs pour activer des gènes qui stimulent la division et la spécialisation cellulaires. Dans cette étude, la stimulation par SLIT3 a rapidement augmenté la phosphorylation d’Akt et de GSK3β, renforcé la β‑caténine nucléaire et élevé les niveaux de protéines cibles de la β‑caténine liées à la croissance. Le blocage de ROBO2/ROBO3 a empêché ces changements, montrant que ces récepteurs sont essentiels au passage du signal.
Prouver que la voie importe vraiment
Pour montrer que ce circuit interne n’est pas un simple effet secondaire mais bien requis pour la formation de la dentine, l’équipe a utilisé une molécule appelée résibufogénine pour bloquer la voie Akt/GSK3β/β‑caténine. Lorsque cette voie a été inhibée, SLIT3 n’a plus pu augmenter la β‑caténine nucléaire ni élever les niveaux de DMP‑1 et DSPP, et sa capacité à améliorer la différenciation odontogénique a été essentiellement perdue. Avec les expériences sur les récepteurs, cela soutient fermement un modèle selon lequel SLIT3 agit via ROBO2/3 pour activer l’interrupteur Akt/GSK3β/β‑caténine, qui à son tour incite les SCAP à proliférer et à mûrir en cellules productrices de dentine.
Ce que cela signifie pour la réparation dentaire future
Ce travail positionne SLIT3 comme un nouveau régulateur de la formation de la dentine à la pointe de la racine, enrichissant notre cartographie des processus par lesquels les racines dentaires croissent et se durcissent. Pour les patients présentant des dents immatures endommagées, la compréhension de cette voie centrée sur SLIT3 pourrait éventuellement inspirer des traitements biologiques encourageant les propres cellules souches de la dent à continuer de construire la dentine radiculaire. Bien que toute application clinique nécessite beaucoup plus de recherches, cette étude ajoute une pièce manquante importante au puzzle du développement des dents jeunes — et de la manière dont nous pourrions les aider à se réparer elles‑mêmes.
Citation: Jiang, L., Liu, L., Yang, F. et al. SLIT3: a novel regulator of odontogenic differentiation through Akt/GSK3β/β-catenin signaling pathway. Int J Oral Sci 18, 35 (2026). https://doi.org/10.1038/s41368-026-00426-7
Mots-clés: régénération de la racine dentaire, formation de la dentine, cellules souches dentaires, signalisation SLIT3, voie Wnt β-caténine