Clear Sky Science · de
SLIT3: ein neuartiger Regulator der odontogenen Differenzierung über den Akt/GSK3β/β-Catenin-Signalweg
Warum diese Zahnstudie wichtig ist
Viele Kinder und Jugendliche erleiden Verletzungen oder tiefe Karies, die das Zahnmark in einem noch nicht fertig entwickelten Zahn abtötet. In solchen Fällen kann das Wurzelwachstum stoppen, sodass ein kurzer, brüchiger Zahn zurückbleibt, der leicht brechen kann. Diese Studie untersucht ein natürliches Protein namens SLIT3 und wie es spezielle Stammzellen an der Spitze junger Zähne dabei unterstützt, stärkeres Wurzeldentin zu bilden. Das weist auf mögliche künftige Behandlungen hin, die beschädigten jungen Zähnen helfen könnten, weiter zu wachsen, statt verloren zu gehen.
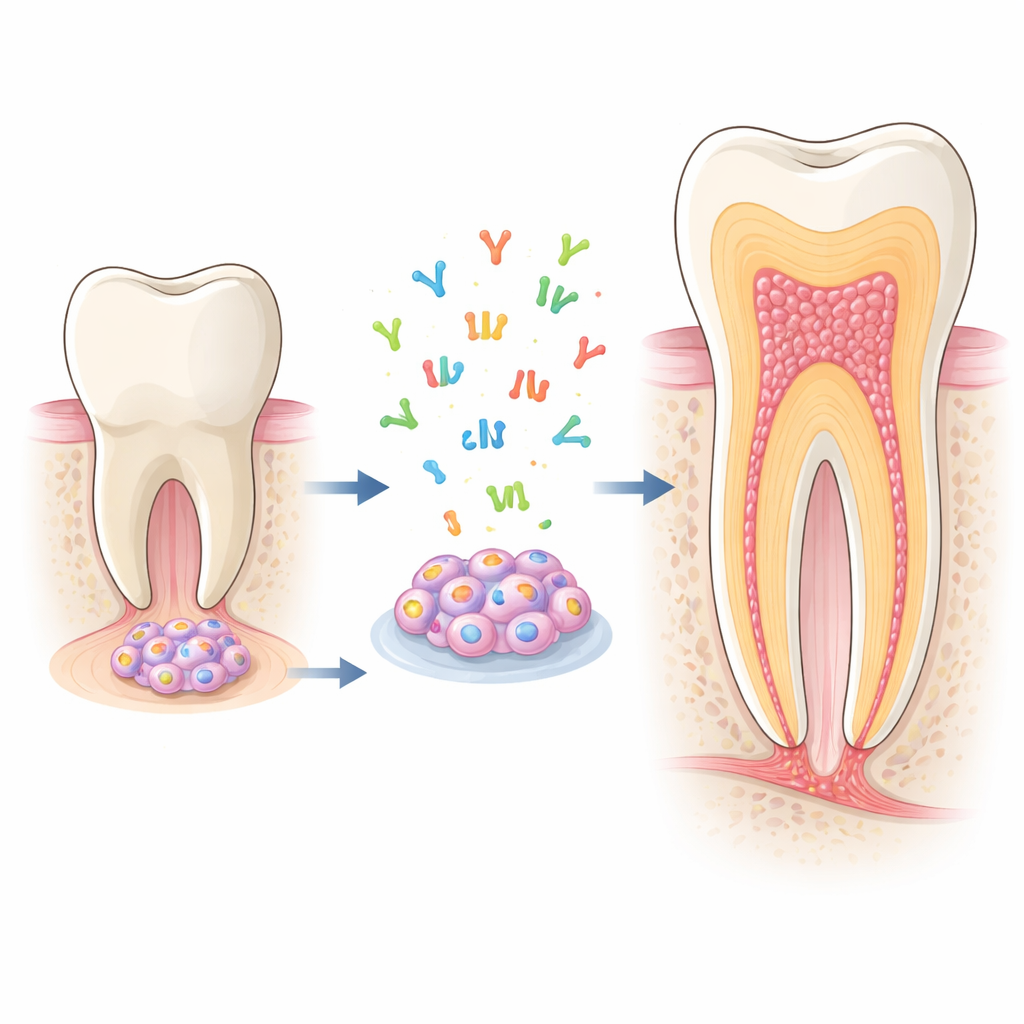
Verborgene Baumeister in jungen Zähnen
Am wachsenden Ende einer unreifen Zahnwurzel liegt ein weiches Gewebe, die apikale Papille. Sie beherbergt Stammzellen aus der apikalen Papille (SCAP), die sich in mehrere Typen zahnstützender Zellen verwandeln können, insbesondere in Odontoblasten – die Zellen, die Dentin aufbauen, das harte Gewebe, das den größten Teil des Zahns bildet. Da sich SCAP im Labor gut vermehren lassen und sich leicht in odontoblastenähnliche Zellen verwandeln, sind sie ein ideales Modell, um zu untersuchen, wie Wurzeln entstehen und wie man sie nach Krankheit oder Verletzung zur Selbstreparatur anregen könnte.
Ein Leitprotein mit neuer Aufgabe
SLIT3 ist hauptsächlich als Leitcues bekannt, das Nervenfasern während der Gehirnentwicklung auf ihren Weg bringt, und es verbindet auch Knochenabbau mit neuer Knochenbildung. Da Knochen und Dentin viele gemeinsame Bauregeln teilen, fragten die Forschenden, ob SLIT3 auch die Bildung von Dentin in Zähnen steuern könnte. Durch die Reanalyse von Einzelzell-RNA-Sequenzierungsdaten aus Maus-Zahnanlagen in verschiedenen Stadien fanden sie heraus, dass das Slit3-Gen vorwiegend im inneren Stützgewebe des Zahns (dentale Mesenchym) aktiv ist, nicht im äußeren Epithel. Das SLIT3-Protein selbst zeigte sich jedoch stark sowohl an dentinbildenden Odontoblasten als auch an schmelzbildenden Ameloblasten, was darauf hindeutet, dass es sekretorisch wirkt und benachbarte Zellen bei der Koordination der Hartgewebsbildung beeinflusst.
Stammzellen beim Wachsen und Verhärten helfen
Um die Rolle von SLIT3 direkt zu testen, isolierte das Team menschliche SCAP aus unreifen Weisheitszähnen und kultivierte sie unter Bedingungen, die die Dentinbildung fördern. Während diese Zellen reiften, stiegen sowohl SLIT3-mRNA- als auch Proteinspiegel stetig an. Wenn die Forschenden SLIT3 künstlich mit kleinen interferierenden RNAs verringerten, teilten sich die SCAP langsamer und bildeten schwächere Mineralablagerungen mit reduzierten Mengen zweier wichtiger Dentinproteine, DMP-1 und DSPP. Im Gegensatz dazu bewirkte die Zugabe von zusätzlichem humanem SLIT3-Protein, dass SCAP schneller wuchsen, die Mineralisierung zunahm und DMP-1 sowie DSPP angestiegen sind. Wurden SCAP mit erhöhtem oder reduziertem SLIT3 in winzige keramische Gerüste in Mäusen transplantiert, produzierten die hoch-SLIT3-Konstrukte reichhaltigeres dentinähnliches Gewebe, während die niedrig-SLIT3-Konstrukte ärmeres Gewebe bildeten – ein Befund, der die Bedeutung von SLIT3 in lebenden Systemen bestätigt.
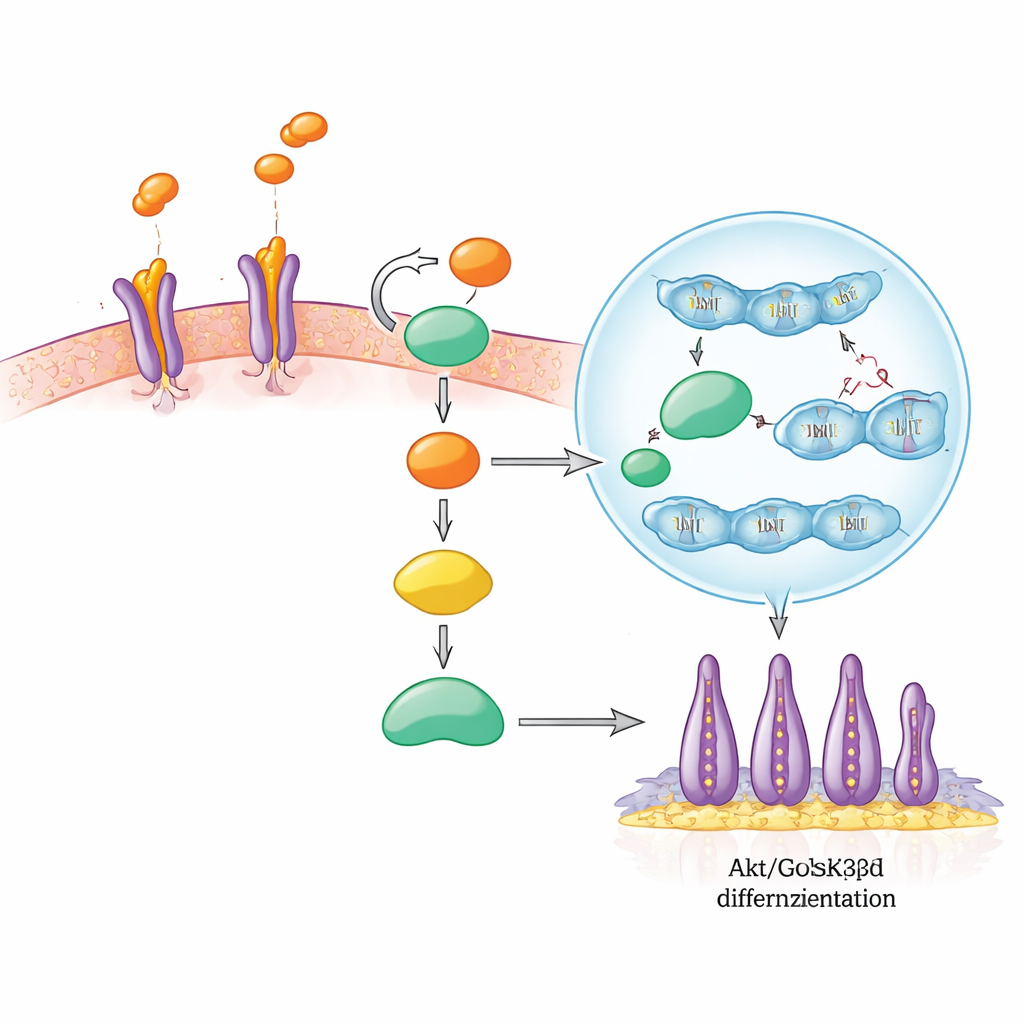
Im Entscheidungsnetzwerk der Zelle
Die Forschenden verfolgten anschließend die Signalkette, die SLIT3 innerhalb von SCAP auslöst. SLIT3 bindet zunächst an die Rezeptoren ROBO2 und ROBO3 an der Zelloberfläche, ähnlich wie ein Schlüssel, der ein Schloss dreht. Das aktiviert einen bekannten Wachstums- und Überlebensknoten namens Akt, der wiederum ein anderes Protein, GSK3β, ausschaltet. Normalerweise markiert aktives GSK3β den Botenstoff β-Catenin für den Abbau. Wenn GSK3β ausgeschaltet ist, akkumuliert β-Catenin und wandert in den Zellkern, wo es mit anderen Faktoren zusammen Gene aktiviert, die Zellteilung und Spezialisierung antreiben. In dieser Studie erhöhte SLIT3-Stimulation schnell die Phosphorylierung von Akt und GSK3β, verstärkte nukleäres β-Catenin und hob die Spiegel von β-Catenin-Zielproteinen, die mit Wachstum verbunden sind. Die Blockade von ROBO2/ROBO3 verhinderte diese Veränderungen, was zeigt, dass diese Rezeptoren für die Signalweiterleitung unerlässlich sind.
Nachweis, dass der Weg wirklich wichtig ist
Um zu zeigen, dass dieser interne Schaltkreis kein bloßer Nebeneffekt ist, sondern tatsächlich für die Dentinbildung erforderlich ist, verwendete das Team eine Substanz namens Resibufogenin, um die Akt/GSK3β/β-Catenin-Route zu blockieren. Wenn dieser Weg gehemmt war, konnte SLIT3 β-Catenin im Zellkern nicht mehr erhöhen oder DMP-1- und DSPP-Spiegel anheben, und seine Fähigkeit, die odontogene Differenzierung zu fördern, war im Wesentlichen verloren. Zusammen mit den Rezeptorexperimenten stützt dies ein Modell, in dem SLIT3 über ROBO2/3 die Akt/GSK3β/β-Catenin-Schaltung einschaltet, die wiederum SCAP anweist, sich zu vermehren und zu reifen zu dentinbildenden Zellen.
Was das für künftige Zahnreparaturen bedeutet
Die Arbeit positioniert SLIT3 als neuen Regulator der Dentinbildung an der Wurzelspitze und erweitert unsere Karte, wie Zahnwurzeln wachsen und verhärten. Für Patientinnen und Patienten mit beschädigten, unreifen Zähnen könnte das Verständnis dieses SLIT3-zentrierten Signalwegs schließlich zu biologisch basierten Therapien inspirieren, die die eigenen Stammzellen des Zahns anregen, weiterhin Wurzeldentin aufzubauen. Während jede klinische Anwendung noch deutlich mehr Forschung erfordert, fügt diese Studie ein wichtiges fehlendes Puzzleteil hinzu, wie sich junge Zähne entwickeln – und wie wir ihnen helfen könnten, sich selbst zu heilen.
Zitation: Jiang, L., Liu, L., Yang, F. et al. SLIT3: a novel regulator of odontogenic differentiation through Akt/GSK3β/β-catenin signaling pathway. Int J Oral Sci 18, 35 (2026). https://doi.org/10.1038/s41368-026-00426-7
Schlüsselwörter: Zahnwurzelregeneration, Dentinbildung, Zahnstammzellen, SLIT3-Signalgebung, Wnt-β-Catenin-Weg