Clear Sky Science · sv
SLIT3: en ny regulator av odontogen differentiering via Akt/GSK3β/β-katenin-signalvägen
Varför den här tandhistorien är viktig
Många barn och tonåringar drabbas av skador eller djupa karies som dödar pulpan i en ännu under utveckling stående tand. När det händer kan roten sluta växa, vilket lämnar en kort, skör tand som lätt kan gå av. Denna studie undersöker ett naturligt protein kallat SLIT3 och hur det hjälper speciella stamceller vid spetsen av unga tänder att bygga starkare rotdentin, vilket pekar mot framtida behandlingar som kan hjälpa skadade unga tänder att fortsätta växa istället för att gå förlorade.
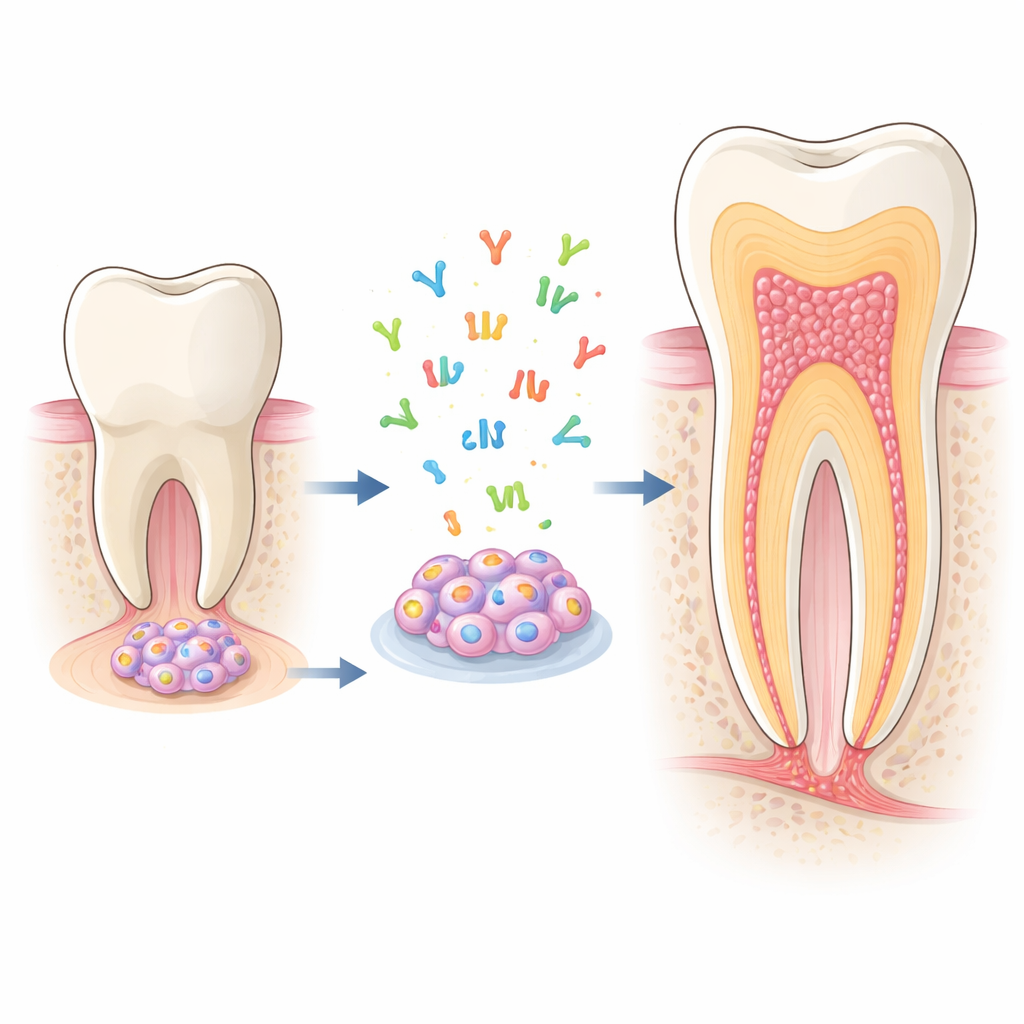
Gömda byggare inne i unga tänder
Vid den växande spetsen av en omogen tandrot finns en mjuk vävnad kallad apikal papilla. Den hyser stamceller från apikal papilla (SCAP), som kan differentiera till flera typer av tandstödjande celler, särskilt odontoblaster — cellerna som avsätter dentin, den hårda vävnaden som bildar större delen av tanden. Eftersom SCAP växer väl i laboratoriet och lätt kan bli odontoblastlika celler, är de en idealisk modell för att studera hur rötter utvecklas och hur vi kan få dem att reparera sig själva efter sjukdom eller skada.
Ett vägledande protein med ett nytt jobb
SLIT3 är mest känt som en vägledande signal som hjälper nervfibrer att hitta sina banor under hjärnans utveckling, och det kopplar också benresorption till ny benbildning. Eftersom ben och dentin delar många byggprinciper, undrade forskarna om SLIT3 också kunde styra bildningen av dentin i tänder. Genom att omanalyssera enkelcells-RNA-sekvenseringsdata från mus-tandanlag i olika stadier fann de att Slit3-genen är aktiv främst i tandens inre stödjevävnad (dental mesenkym), inte i det yttre epitelet. Ändå visade SLIT3-proteinet sig tydligt både på dentinbildande odontoblaster och emaljbildande ameloblaster, vilket antyder att det är utsöndrat och sedan verkar på närliggande celler för att samordna hårdvävnadsbildning.
Hjälper stamceller att växa och förhärda
För att testa SLIT3:s roll direkt isolerade teamet mänskliga SCAP från omogna visdomständer och odlade dem under förhållanden som främjar dentinbildning. När dessa celler mognade ökade både SLIT3-gen- och proteinivåerna stadigt. När forskarna konstgjort sänkte SLIT3 med små interfererande RNA, delade SCAP långsammare och bildade svagare mineralavlagringar, med minskade nivåer av två nyckelproteiner i dentin, DMP-1 och DSPP. Däremot gjorde tillsats av extra mänskligt SLIT3-protein att SCAP växte snabbare, ökade mineraliseringen och ökade DMP-1 och DSPP. När SCAP med högre eller lägre SLIT3 transplanterades i små keramiska ställverk i möss, producerade de hög-SLIT3-konstrukten rikare dentinlik vävnad, medan låga-SLIT3-konstrukten gav fattigare vävnad, vilket bekräftar SLIT3:s betydelse i levande system.
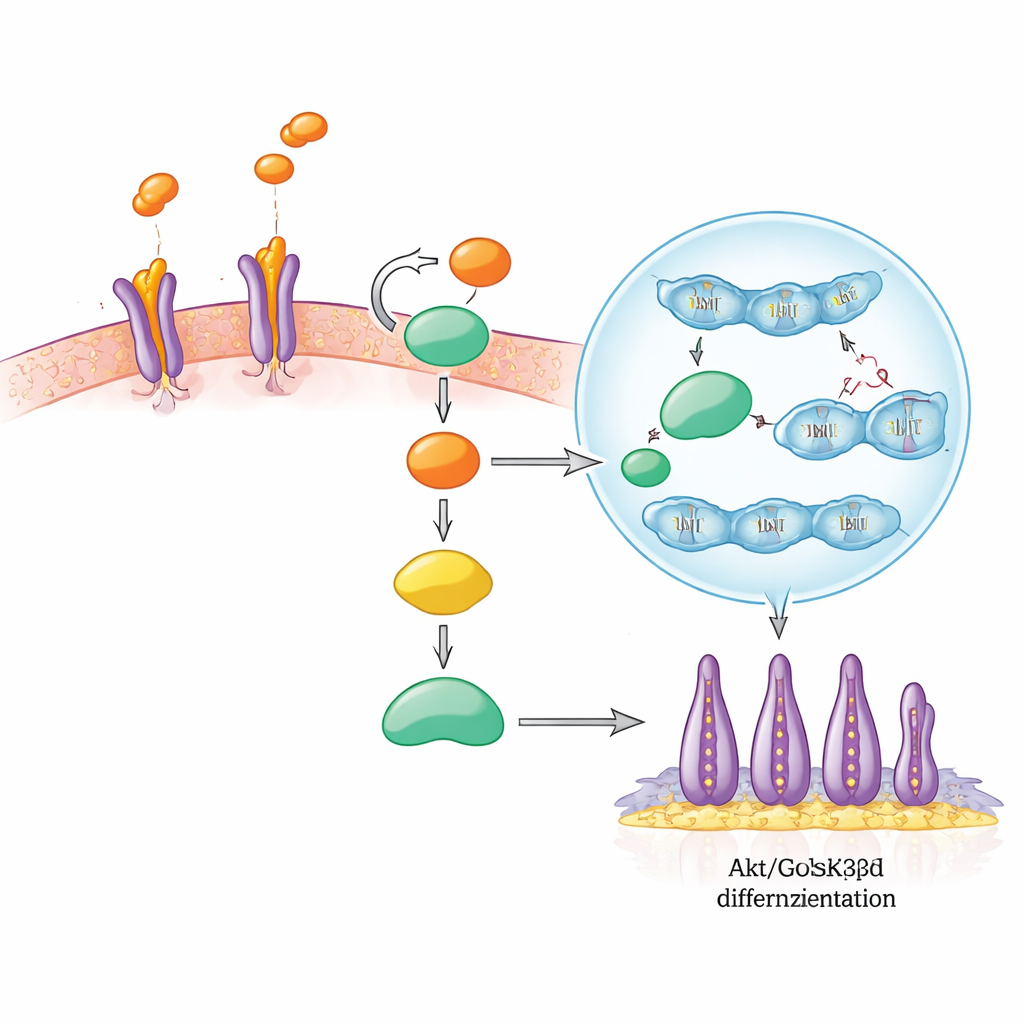
Inuti cellens beslutskrets
Forskarna följde sedan kedjan av signaler som SLIT3 utlöser inne i SCAP. SLIT3 binder först till ROBO2- och ROBO3-receptorer på cellytan, ungefär som en nyckel som vrider ett lås. Detta aktiverar en välkänd tillväxt- och överlevnadsnod kallad Akt, som sedan stänger av ett annat protein, GSK3β. Normalt hjälper aktivt GSK3β att märka budbäraren β-katenin för nedbrytning. När GSK3β stängs av ackumuleras β-katenin och transporteras in i cellkärnan, där det samarbetar med andra faktorer för att slå på gener som driver celldelning och specialisering. I denna studie ökade SLIT3-stimulering snabbt Akt- och GSK3β-fosforylering, stärkte nukleärt β-katenin och ökade nivåerna av β-katenin-målproteiner kopplade till tillväxt. Blockering av ROBO2/ROBO3 förhindrade dessa förändringar, vilket visar att dessa receptorer är nödvändiga för att signalen ska gå vidare.
Bevisa att vägen verkligen spelar roll
För att visa att denna interna krets inte bara är en bieffekt utan faktiskt krävs för dentinbildning, använde teamet en kemisk substans kallad Resibufogenin för att blockera Akt/GSK3β/β-katenin-vägen. När denna väg hämmdes kunde SLIT3 inte längre öka β-katenin i kärnan eller höja DMP-1- och DSPP-nivåerna, och dess förmåga att förbättra odontogen differentiering gick i princip förlorad. Tillsammans med receptorexperimenten stöder detta tydligt en modell där SLIT3 verkar via ROBO2/3 för att slå på Akt/GSK3β/β-katenin-omkopplaren, vilket i sin tur talar om för SCAP att dela sig och mogna till dentinproducerande celler.
Vad detta innebär för framtida tandreparation
Arbetet placerar SLIT3 som en ny regulator av dentinbildning vid rotspetsen och utökar vår karta över hur tandrötter växer och förhärdas. För patienter med skadade, omogna tänder kan förståelsen av denna SLIT3-centrerade väg så småningom inspirera biologiskt baserade behandlingar som uppmuntrar tandens egna stamceller att fortsätta bygga rotdentin. Medan klinisk tillämpning kommer att kräva betydligt mer forskning, lägger denna studie till en viktig pusselbit i förståelsen av hur unga tänder utvecklas — och hur vi kan hjälpa dem att läka sig själva.
Citering: Jiang, L., Liu, L., Yang, F. et al. SLIT3: a novel regulator of odontogenic differentiation through Akt/GSK3β/β-catenin signaling pathway. Int J Oral Sci 18, 35 (2026). https://doi.org/10.1038/s41368-026-00426-7
Nyckelord: tandrotsregenerering, bildning av dentin, dentala stamceller, SLIT3-signalering, Wnt beta-katenin-väg