Clear Sky Science · pl
SLIT3: nowy regulator różnicowania odontogennego poprzez szlak sygnalizacyjny Akt/GSK3β/β-katenina
Dlaczego ta opowieść o zębach ma znaczenie
Wiele dzieci i nastolatków doznało urazów lub głębokich ubytków, które niszczą miazgę w jeszcze rozwijającym się zębie. W takim wypadku korzeń może przestać rosnąć, pozostawiając krótki, kruchy ząb, podatny na złamania. Badanie to analizuje naturalne białko o nazwie SLIT3 i sposób, w jaki pomaga specjalnym komórkom macierzystym na szczycie młodych zębów budować mocniejszą zębinę korzeniową, wskazując drogę do przyszłych terapii, które mogłyby pomóc uszkodzonym młodym zębom kontynuować wzrost zamiast być utraconymi.
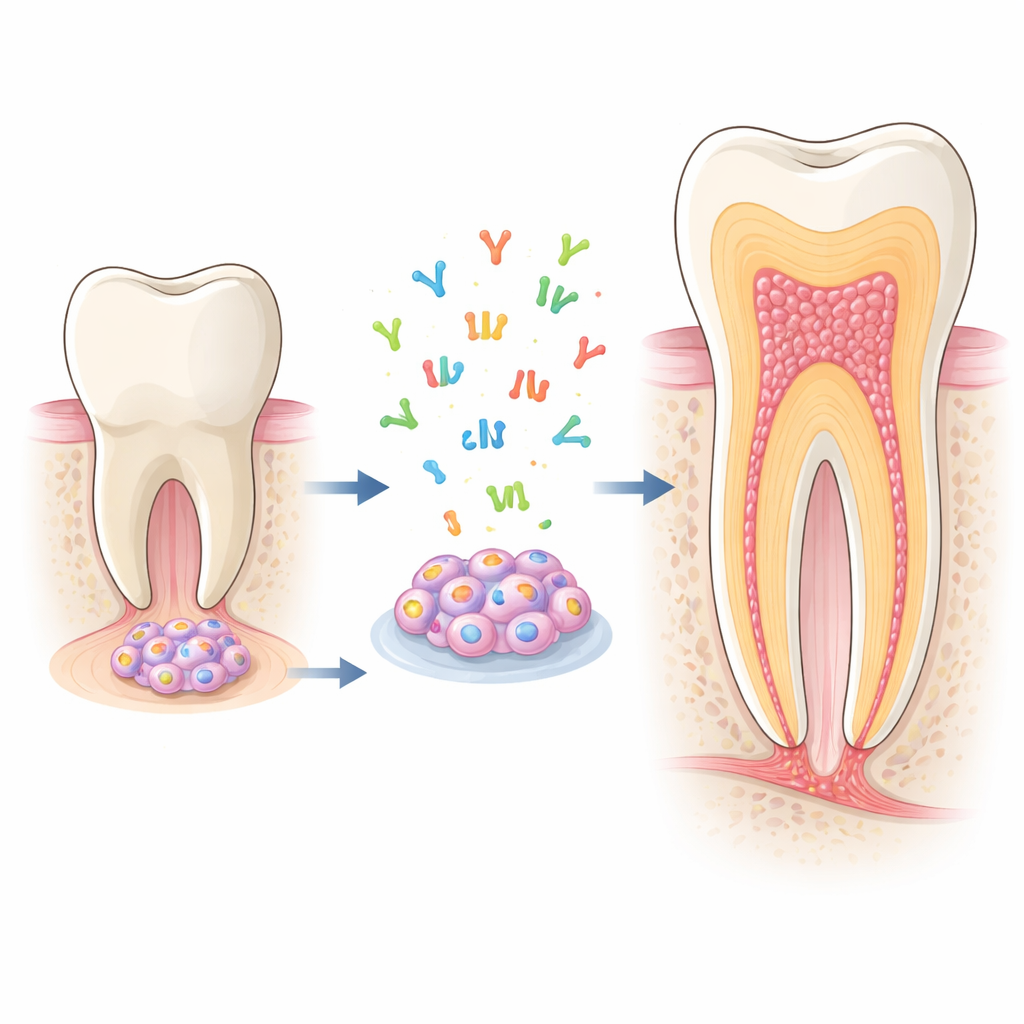
Ukryci budowniczowie wewnątrz młodych zębów
Na rosnącym końcu niedojrzałego korzenia zęba znajduje się miękka tkanka zwana brodawką szczytową (apical papilla). Mieszczą się w niej komórki macierzyste brodawki szczytowej (SCAP), które mogą przekształcać się w kilka typów komórek wspierających ząb, w szczególności w odontoblasty — komórki odkładające zębinę, twardą tkankę tworzącą większość zęba. Ponieważ SCAP dobrze rosną w laboratorium i łatwo przekształcają się w komórki podobne do odontoblastów, stanowią idealny model do badania, jak rozwijają się korzenie i jak można skłonić je do samonaprawy po chorobie lub urazie.
Białko przewodnie z nową rolą
SLIT3 jest najlepiej znane jako sygnał kierunkowy pomagający włóknom nerwowym znaleźć właściwe ścieżki podczas rozwoju mózgu, a także łączy resorpcję kości z jej tworzeniem. Ponieważ kość i zębina dzielą wiele zasad budowy, badacze zapytali, czy SLIT3 może także kierować tworzeniem zębiny w zębach. Ponowna analiza danych z pojedynczych komórek RNA-sekwencjonowania z zawiązków zębowych myszy na różnych etapach wykazała, że gen Slit3 jest aktywny głównie w wewnętrznej tkance podporowej zęba (mezenchyma zębowa), a nie w nabłonku zewnętrznym. Jednak sam białkowy produkt SLIT3 silnie pojawiał się zarówno na odontoblastach tworzących zębinę, jak i na ameloblastach tworzących szkliwo, co sugeruje, że jest wydzielany i działa na pobliskie komórki, koordynując tworzenie tkanek twardych.
Wspieranie wzrostu i utwardzania komórek macierzystych
Aby bezpośrednio sprawdzić rolę SLIT3, zespół wyizolował ludzkie SCAP z niedojrzałych zębów mądrości i hodował je w warunkach sprzyjających tworzeniu zębiny. W miarę dojrzewania tych komórek poziomy genu i białka SLIT3 systematycznie rosły. Gdy badacze sztucznie obniżyli poziom SLIT3 za pomocą małych interferujących RNA, SCAP mnożyły się wolniej i tworzyły słabsze depozyty mineralne, z obniżonymi poziomami dwóch kluczowych białek zębiny, DMP-1 i DSPP. Natomiast dodanie dodatkowego ludzkiego białka SLIT3 przyspieszało wzrost SCAP, zwiększało mineralizację oraz podnosiło poziomy DMP-1 i DSPP. Gdy SCAP o podwyższonym lub obniżonym SLIT3 przeszczepiano do małych ceramicznych rusztowań w myszach, konstrukty o wysokim poziomie SLIT3 wytwarzały bogatszą tkankę przypominającą zębinę, podczas gdy konstrukty o niskim SLIT3 dawały uboższą tkankę, potwierdzając znaczenie SLIT3 in vivo.
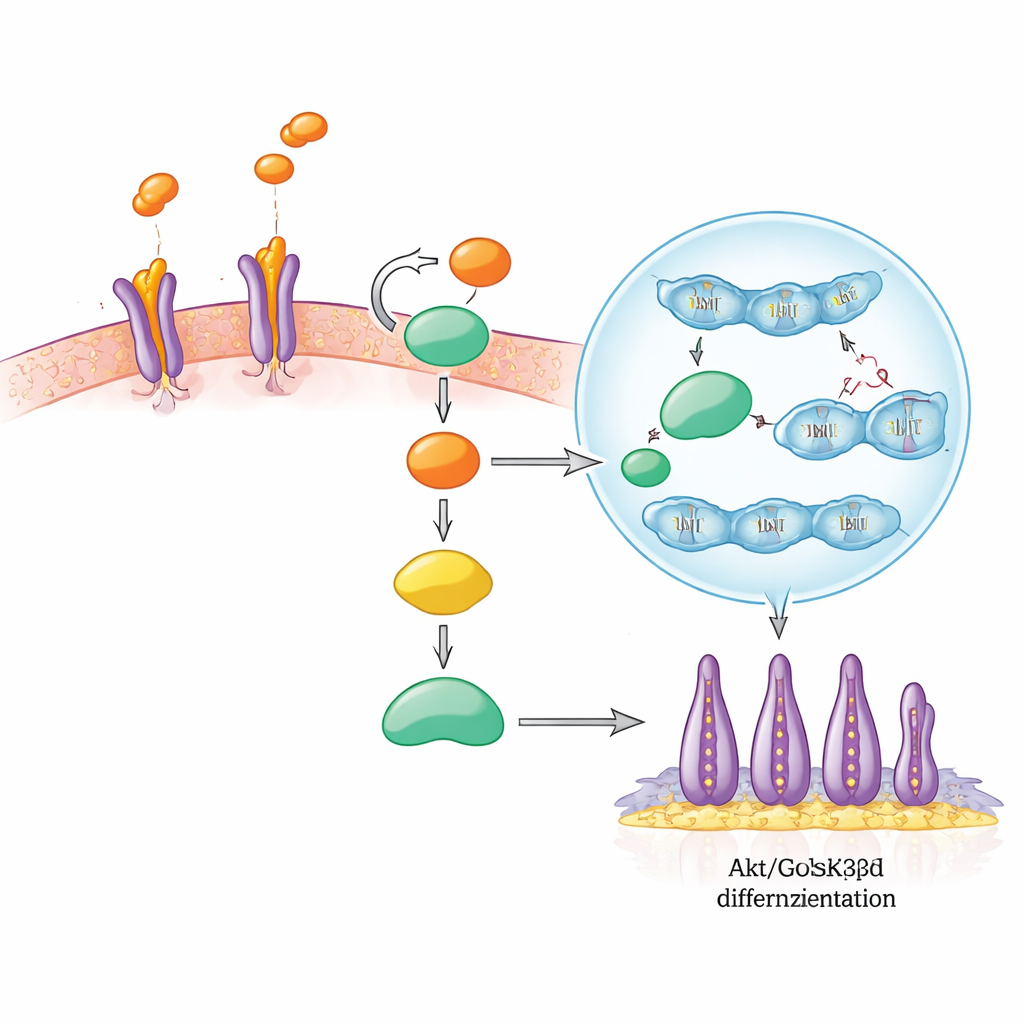
Wewnątrz komórkowego obwodu decyzyjnego
Badacze śledzili następnie łańcuch sygnałów wywoływanych przez SLIT3 w SCAP. SLIT3 najpierw wiąże się z receptorami ROBO2 i ROBO3 na powierzchni komórki, niczym klucz przekręcający zamek. To aktywuje dobrze znany węzeł wzrostu i przeżycia — Akt, który następnie wyłącza inne białko, GSK3β. Zwykle aktywne GSK3β pomaga oznaczać posłańca β-kateninę do degradacji. Gdy GSK3β zostaje wyłączone, β-katenina akumuluje się i przemieszcza do jądra komórkowego, gdzie współpracuje z innymi czynnikami, włączając geny pobudzające podział komórek i ich specjalizację. W tym badaniu stymulacja SLIT3 szybko zwiększała fosforylację Akt i GSK3β, zwiększała ilość β-kateniny w jądrze i podnosiła poziomy białek będących celami β-kateniny związanych z wzrostem. Zablokowanie ROBO2/ROBO3 zapobiegało tym zmianom, pokazując, że te receptory są niezbędne do przekazania sygnału.
Dowód, że szlak naprawdę ma znaczenie
Aby pokazać, że ten wewnętrzny obwód nie jest jedynie efektem ubocznym, ale faktycznie konieczny do tworzenia zębiny, zespół użył chemikalium o nazwie Resibufogenin do zablokowania szlaku Akt/GSK3β/β-katenina. Kiedy ten szlak został zahamowany, SLIT3 nie potrafiło już zwiększyć β-kateniny w jądrze ani podnieść poziomów DMP-1 i DSPP, a jego zdolność do wspierania różnicowania odontogennego zasadniczo zanikła. W połączeniu z eksperymentami receptorowymi stanowi to silne poparcie dla modelu, w którym SLIT3 działa poprzez ROBO2/3, aby włączyć przełącznik Akt/GSK3β/β-katenina, co z kolei nakazuje SCAP mnożyć się i dojrzewać w komórki produkujące zębinę.
Co to oznacza dla przyszłych napraw zębów
Praca ta wskazuje SLIT3 jako nowego regulatora tworzenia zębiny na szczycie korzenia, rozszerzając naszą mapę tego, jak korzenie zębów rosną i twardnieją. Dla pacjentów z uszkodzonymi, niedojrzałymi zębami, zrozumienie tego zorientowanego na SLIT3 szlaku może ostatecznie zainspirować biologicznie ukierunkowane terapie, które zachęcą własne komórki macierzyste zęba do dalszego budowania zębiny korzeniowej. Chociaż zastosowania kliniczne będą wymagać znacznie więcej badań, to badanie dodaje istotny brakujący element układanki dotyczącej tego, jak rozwijają się młode zęby — i jak możemy pomóc im się same naprawić.
Cytowanie: Jiang, L., Liu, L., Yang, F. et al. SLIT3: a novel regulator of odontogenic differentiation through Akt/GSK3β/β-catenin signaling pathway. Int J Oral Sci 18, 35 (2026). https://doi.org/10.1038/s41368-026-00426-7
Słowa kluczowe: regeneracja korzenia zęba, powstawanie zębiny, komórki macierzyste zęba, sygnalizacja SLIT3, szlak Wnt beta-katenina