Clear Sky Science · nl
SLIT3: een nieuwe regelaar van odontogene differentiatie via het Akt/GSK3β/β-catenine signaalpad
Waarom dit tandverhaal ertoe doet
Veel kinderen en tieners lopen verwondingen of diepe tandbederf op die de pulpa in een nog in ontwikkeling zijnde tand doden. Wanneer dat gebeurt, kan de wortel stoppen met groeien, waardoor een korte, kwetsbare tand overblijft die gemakkelijk kan breken. Deze studie onderzoekt een natuurlijk eiwit genaamd SLIT3 en hoe het speciale stamcellen aan de top van jonge tanden helpt om sterker worteldentine te vormen, wat wijst op toekomstige behandelingen die beschadigde jonge tanden kunnen helpen door te groeien in plaats van te verliezen.
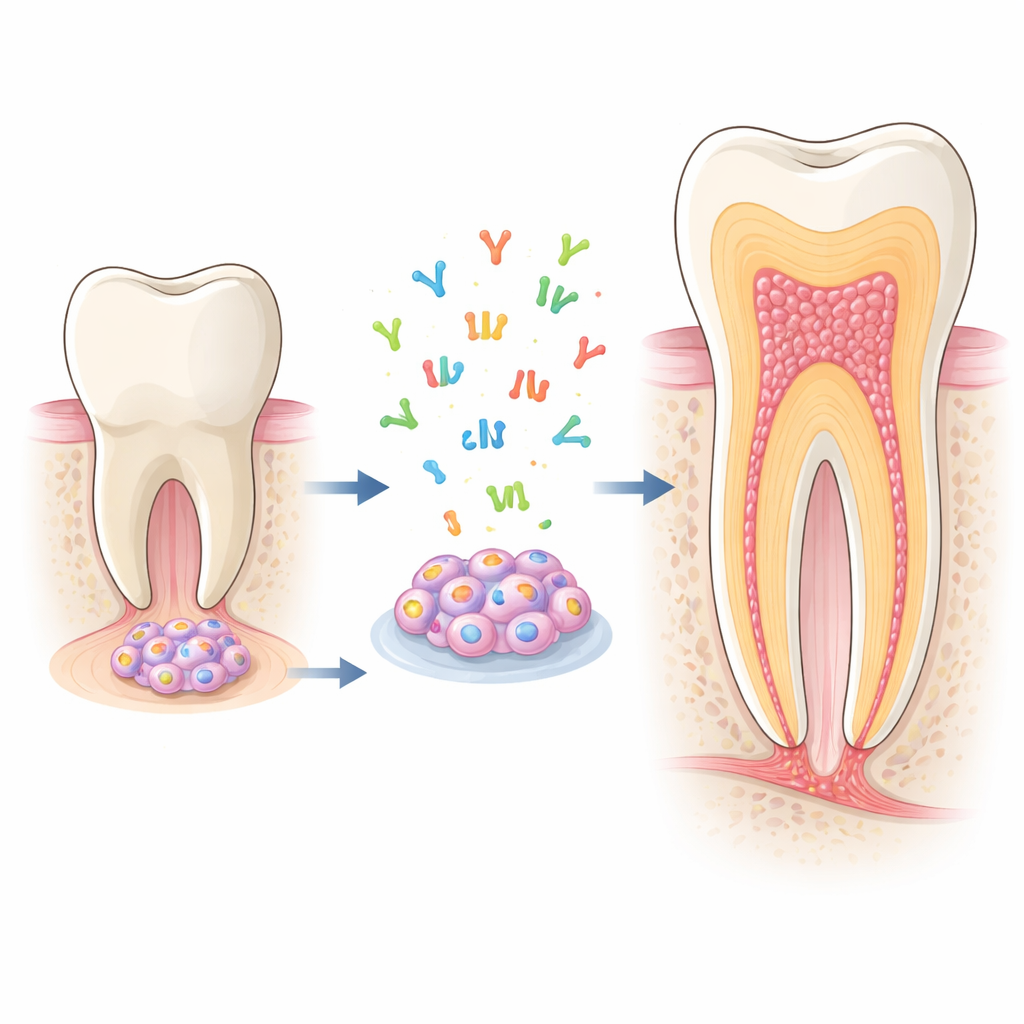
Verborgen bouwers in jonge tanden
Bij de groeiende top van een onrijpe tandwortel bevindt zich een zacht weefsel genaamd de apicale papil. Daarin huist het stamcelpopulatie van de apicale papil (SCAP), die kan differentiëren in meerdere typen tandondersteunende cellen, met name odontoblasten — de cellen die dentine aanleggen, het harde weefsel dat het grootste deel van de tand vormt. Omdat SCAP goed groeien in het laboratorium en gemakkelijk odontoblast-achtige cellen worden, vormen ze een ideaal model om te bestuderen hoe wortels zich ontwikkelen en hoe we ze mogelijk kunnen aanzetten zichzelf te herstellen na ziekte of letsel.
Een geleide-eiwit met een nieuwe taak
SLIT3 staat vooral bekend als een geleidingssignaal dat zenuwvezels helpt hun weg te vinden tijdens de ontwikkeling van de hersenen, en het koppelt ook botafbraak aan nieuwe botvorming. Omdat bot en dentine veel bouwprincipes delen, vroegen de onderzoekers zich af of SLIT3 ook de vorming van dentine in tanden zou kunnen sturen. Door single-cell RNA-sequencingdata van muizentandkiemcellen in verschillende stadia opnieuw te analyseren, vonden ze dat het Slit3-gen voornamelijk actief is in het binnenste ondersteunende weefsel van de tand (dentale mesenchym), niet in het buitenste epitheel. Toch verscheen het SLIT3-eiwit zelf sterk op zowel dentinevormende odontoblasten als glazuurvormende ameloblasten, wat suggereert dat het wordt uitgescheiden en vervolgens werkt op nabije cellen om de vorming van hard weefsel te coördineren.
Het helpen van stamcellen om te groeien en te verharden
Om de rol van SLIT3 direct te testen, isoleerde het team menselijke SCAP uit onrijpe verstandskiezen en kweekte ze onder omstandigheden die dentinevorming bevorderen. Naarmate deze cellen rijpten, namen zowel SLIT3-gen- als eiwitniveaus gestaag toe. Wanneer de onderzoekers SLIT3 kunstmatig verlaagden met kleine interfererende RNA-moleculen, deelden SCAP langzamer en vormden ze zwakkere mineraalafzettingen, met verminderde niveaus van twee belangrijke dentine-eiwitten, DMP-1 en DSPP. Daarentegen maakte toevoeging van extra humaan SLIT3-eiwit dat SCAP sneller groeiden, de mineralisatie toenam en DMP-1 en DSPP toenamen. Wanneer SCAP met meer of minder SLIT3 werden getransplanteerd in kleine keramische steigers in muizen, produceerden de constructies met veel SLIT3 rijker dentineachtig weefsel, terwijl de constructies met weinig SLIT3 armer weefsel produceerden, wat het belang van SLIT3 in levende systemen bevestigt.
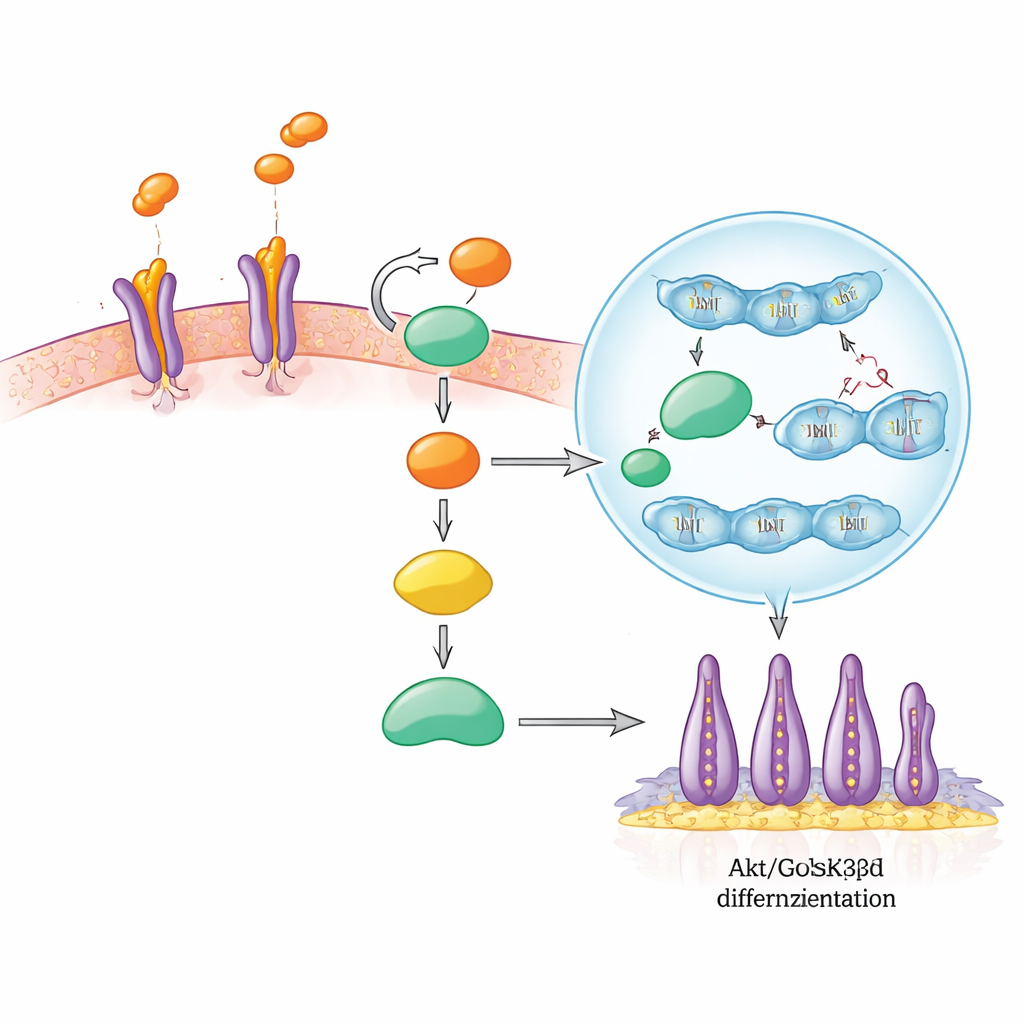
In het beslissingscircuit van de cel
De onderzoekers volgden vervolgens de keten van signalen die SLIT3 in SCAP activeert. SLIT3 bindt eerst aan ROBO2- en ROBO3-receptoren op het celoppervlak, vergelijkbaar met een sleutel die een slot omdraait. Dit activeert een bekend groeien overlevingscentrum genaamd Akt, dat vervolgens een ander eiwit, GSK3β, uitschakelt. Normaal helpt actieve GSK3β boodschapper β-catenine te markeren voor afbraak. Wanneer GSK3β wordt uitgeschakeld, stapelt β-catenine zich op en beweegt naar de celkern, waar het samenwerkt met andere factoren om genen aan te zetten die celvermenigvuldiging en specialisatie stimuleren. In deze studie verhoogde SLIT3-stimulatie snel de fosforylering van Akt en GSK3β, bevorderde kern-β-catenine en verhoogde niveaus van β-catenine-doeleiwitten die met groei zijn geassocieerd. Het blokkeren van ROBO2/ROBO3 verhinderde deze veranderingen, wat aantoont dat die receptoren essentieel zijn voor het doorgeven van het signaal.
Aantonen dat het pad echt belangrijk is
Om te laten zien dat dit interne circuit niet alleen een bijwerking is maar daadwerkelijk vereist voor dentinevorming, gebruikte het team een chemische stof genaamd Resibufogenine om het Akt/GSK3β/β-catenine-pad te blokkeren. Wanneer dit pad werd geremd, kon SLIT3 niet langer β-catenine in de kern verhogen of DMP-1 en DSPP verhogen, en verloor het zijn vermogen om odontogene differentiatie te verbeteren in wezen. Samen met de receptor-experimenten ondersteunt dit sterk een model waarin SLIT3 via ROBO2/3 werkt om de Akt/GSK3β/β-catenine-schakelaar om te zetten, die op zijn beurt SCAP vertelt zich te vermenigvuldigen en te rijpen tot dentine-producerende cellen.
Wat dit betekent voor toekomstige tandreparatie
Het werk plaatst SLIT3 als een nieuwe regelaar van dentinevorming aan de worteltip en breidt onze kaart uit van hoe tandwortels groeien en verhard worden. Voor patiënten met beschadigde, onrijpe tanden zou het begrip van dit op SLIT3 gerichte pad uiteindelijk kunnen inspireren tot biologische behandelingen die de eigen stamcellen van de tand aanmoedigen om door te gaan met het opbouwen van worteldentine. Hoewel elke klinische toepassing veel meer onderzoek zal vereisen, voegt deze studie een cruciaal ontbrekend stuk toe aan de puzzel van hoe jonge tanden zich ontwikkelen — en hoe we ze mogelijk kunnen helpen zichzelf te genezen.
Bronvermelding: Jiang, L., Liu, L., Yang, F. et al. SLIT3: a novel regulator of odontogenic differentiation through Akt/GSK3β/β-catenin signaling pathway. Int J Oral Sci 18, 35 (2026). https://doi.org/10.1038/s41368-026-00426-7
Trefwoorden: wortelregeneratie van tanden, dentinevorming, tandheelkundige stamcellen, SLIT3-signaal, Wnt beta-catenine pad