Clear Sky Science · sv
En maskininlärningsbaserad farmakokinetikprediktor (EGFR-PROPK) för EGFR-riktade PROTACs
Smartare läkemedelsdesign för svårbehandlade cancerformer
Många lovande nya cancerläkemedel misslyckas inte för att de inte träffar sitt mål, utan för att kroppen rensar bort dem för snabbt, lagrar dem på fel ställen eller inte kan absorbera dem väl. En ny klass mediciner kallade PROTACs kan förstöra sjukdomsframkallande proteiner som tidigare ansågs "ojobbabla", men deras beteende i kroppen är särskilt svårt att förutsäga. Den här studien presenterar ett maskininlärningsverktyg, EGFR-PROPK, utformat specifikt för att förutsäga hur en grupp PROTACs mot ett centralt cancerprotein rör sig i kroppen, med målet att hjälpa forskare välja bättre läkemedelskandidater tidigare och slösa färre år och resurser på återvändsgränder.
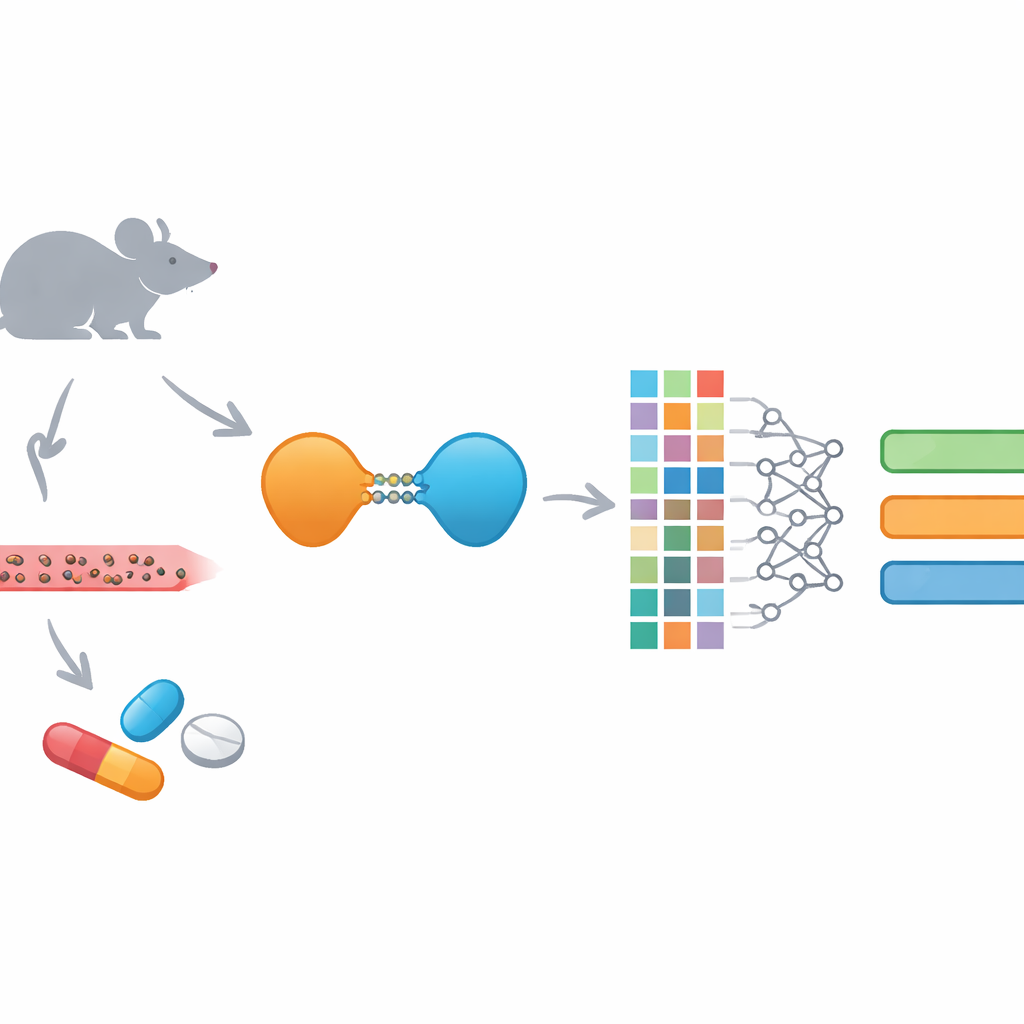
Nya proteinnedbrytande läkemedel och deras utmaningar
PROTACs är ovanliga läkemedel: istället för att bara blockera ett protein märker de det för nedbrytning av cellens egna sopmaskineri. Varje PROTAC förenar en bindande del för sjukdomsmålet med en annan del som rekryterar en cellulär "rives" och de är kopplade med en flexibel kedja. Denna design låter dem angripa proteiner som vanliga läkemedel inte lätt når och tillåter ofta tillfällig bindning snarare än ständig ockupation av en bindningssite. Men samma storlek och komplexitet gör PROTACs svåra att administrera och kontrollera i kroppen. De tenderar att vara stora, relativt fettlösliga och starkt bundna till blodproteiner, vilket komplicerar hur de absorberas, distribueras, bryts ner och utsöndras.
Varför vanliga tumregler för läkemedelsbeteende faller kort
Traditionella läkemedelsutvecklare använder enkla mått, såsom molekylvikt, fettbenägenhet (LogP) och tumregler för "drug-likeness", för att gissa hur en förening kan bete sig i kroppen. Forskarna började med att fråga om dessa välkända mått kunde förklara hur 100 PROTACs som riktar sig mot epidermal tillväxtfaktorreceptor (EGFR)—en viktig drivkraft i många cancerformer—äter sig i levande möss. De fokuserade på tre nyckelparametrar: clearance (hur snabbt kroppen avlägsnar läkemedlet), halveringstid (hur länge läkemedlet finns i cirkulation) och skenbar distributionsvolym (hur brett det sprider sig in i vävnader). När de jämförde dessa egenskaper med grundläggande deskriptorer var datapunkterna utspridda utan tydliga trender, vilket visar att enkla kemiska regler inte räcker för att förutsäga hur PROTACs beter sig.
Att träna en skräddarsydd prediktionsmotor
För att överbrygga denna lucka byggde teamet EGFR-PROPK, en maskininlärningsprediktor finjusterad specifikt för EGFR-riktade PROTACs. De genomförde först musstudier på 100 olika PROTACs och mätte deras clearance, halveringstid och distributionsvolym efter dosering. De beskrev sedan varje molekyl med flera rika "fingerprints" som kodar dess detaljerade struktur och beräknade 200 ytterligare kemiska egenskaper. Dessa numeriska beskrivningar matades in i en CatBoost-baserad modell, en modern algoritm som utmärker sig i att hitta mönster i tabulära data. Till skillnad från allmänna verktyg tränades EGFR-PROPK direkt på in vivo-resultat för PROTACs, vilket gjorde det möjligt att lära sig subtila samband mellan komplexa linkerformer, total storlek och hur länge läkemedlen stannar i blodet eller sprider sig i vävnader.
Överträffar generella modeller och avslöjar dolda nyanser
Forskarna jämförde EGFR-PROPK med välanvända prediktionsplattformar som till största delen är byggda för traditionella småmolekylära läkemedel. När dessa generiska modeller användes "som de är" på PROTACs var deras förutsägelser dåliga: uppskattade värden för halveringstid, clearance och vävnadsdistribution avvek ofta kraftigt från verkliga mätningar. Även efter att en konkurrentmodell finjusterats med PROTAC-data låg den fortfarande efter. I kontrast uppnådde EGFR-PROPK avsevärt bättre överensstämmelse mellan förutsagda och experimentella värden, särskilt för halveringstid och clearance, med måttliga vinster för distribution. Modellen hanterade också verkliga fallstudier: två PROTACs med mycket liknande strukturer men mycket olika beteende särskiljdes mer exakt av EGFR-PROPK än av generella verktyg, vilket understryker vikten av PROTAC-specifika träningsdata.
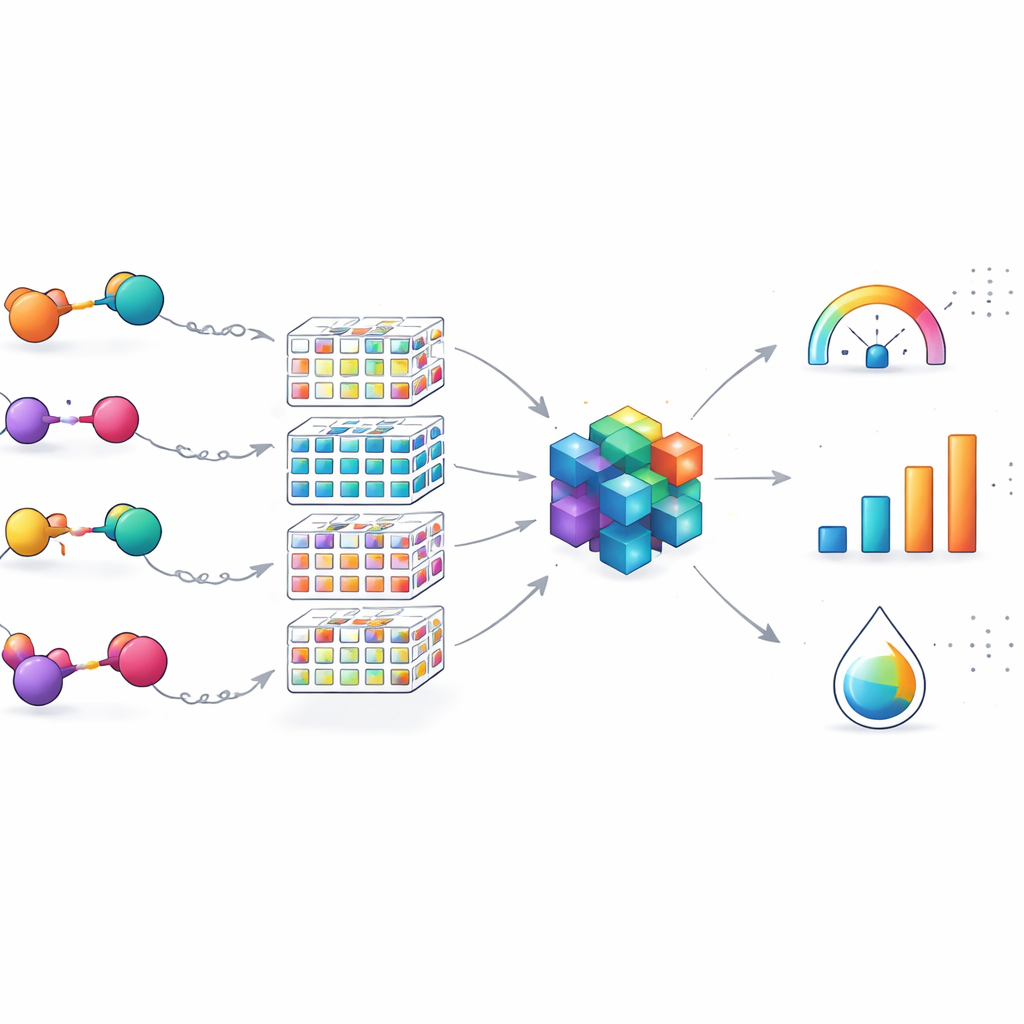
Kartläggning av det kemiska landskapet och dess begränsningar
Utöver prestationssiffror kontrollerade teamet om deras 100 PROTACs täckte ett brett spektrum av designer eller bara ett snävt hörn av det kemiska rummet. Genom att reducera molekylerna till deras kärnskaffolder och visualisera dem bland tusentals patenterade PROTACs visade de att deras uppsättning spänner över många distinkta strukturella typer, särskilt i de flexibla linkrarna. Detta betyder att modellen är väl lämpad för att förfina EGFR-riktade PROTACs som delar nyckelbyggstenar men varierar i hur delarna är kopplade. Samtidigt betonar författarna att verktyget är en domänspecialist: dess noggrannhet kan sjunka för PROTACs byggda kring helt andra mål eller degraderingsvägar, vilket pekar på behovet av framtida expansion och transferinlärning över dataset.
Vad detta betyder för framtida läkemedel
För lekman är huvudbudskapet att ett läkemedels "rörsystem" i kroppen—hur det absorberas, vart det tar vägen och hur länge det stannar—kan göra eller förstöra en lovande cancerterapi, och de vanliga genvägarna för små piller fungerar inte väl för nästa generations degraderare som PROTACs. Genom att skapa EGFR-PROPK visar forskarna att noggrant insamlade djurdata, kombinerat med avancerade mönsterigenkänningsmetoder, kan ge en mycket skarpare tidig bild av hur dessa komplexa molekyler kommer att bete sig. Denna typ av skräddarsydd prediktion bör hjälpa kemister att designa PROTACs som inte bara förstör rätt proteiner utan också når dem i rätt mängder, och så bana väg för effektivare och säkrare behandlingar mot resistenta cancerformer.
Citering: Zhang, R., Li, F., Liu, Y. et al. A machine learning-based pharmacokinetics predictor (EGFR-PROPK) for EGFR-targeting PROTACs. Commun Chem 9, 134 (2026). https://doi.org/10.1038/s42004-026-01938-3
Nyckelord: PROTAC farmakokinetik, EGFR-riktade degraderare, maskininlärning i läkemedelsdesign, ADMET-prediktion, målinriktad proteinnedbrytning