Clear Sky Science · es
Un predictor de farmacocinética basado en aprendizaje automático (EGFR-PROPK) para PROTACs dirigidos a EGFR
Diseño de fármacos más inteligente para cánceres difíciles de tratar
Muchos fármacos anticancerígenos prometedores fracasan no porque fallen en su diana, sino porque el organismo los elimina demasiado rápido, se acumulan en sitios no deseados o no se absorben bien. Una nueva clase de medicamentos llamada PROTACs puede destruir proteínas causantes de enfermedad que antes se consideraban “no drugables”, pero su comportamiento dentro del cuerpo es especialmente difícil de predecir. Este estudio presenta una herramienta de aprendizaje automático, EGFR-PROPK, diseñada específicamente para anticipar cómo un conjunto de PROTACs dirigidos contra una proteína clave del cáncer se distribuye y se elimina en el organismo, con el objetivo de ayudar a los científicos a seleccionar mejores candidatos farmacológicos desde etapas tempranas y ahorrar años y recursos en callejones sin salida.
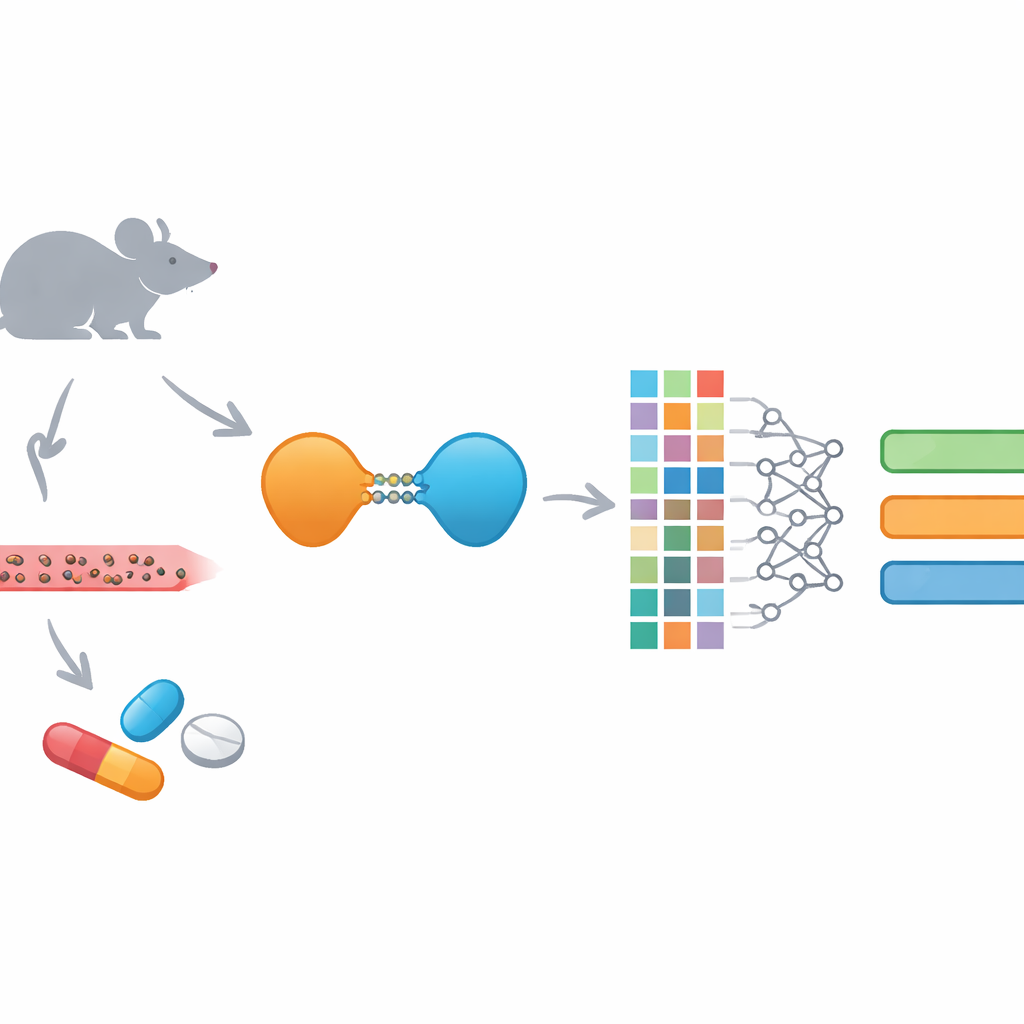
Nuevos fármacos que destruyen proteínas y sus retos
Los PROTACs son fármacos poco convencionales: en lugar de limitarse a bloquear una proteína, la marcan para su destrucción por la propia maquinaria celular de eliminación. Cada PROTAC une una pieza que se acopla a la diana patológica con otra que recluta a un “triturador” celular, conectadas por una cadena flexible. Este diseño les permite atacar proteínas a las que los fármacos normales no llegan con facilidad y con frecuencia permite una unión temporal en lugar de una ocupación constante del sitio proteico. Sin embargo, ese mismo tamaño y complejidad hacen que los PROTACs sean difíciles de administrar y controlar en el organismo. Tienden a ser grandes, relativamente hidrofóbicos y a unirse fuertemente a proteínas sanguíneas, factores que complican su absorción, distribución, metabolización y eliminación.
Por qué las reglas habituales del comportamiento de fármacos se quedan cortas
Los desarrolladores tradicionales de fármacos usan números simples, como el peso molecular, la afinidad por la grasa (LogP) y reglas empíricas de “drug-likeness”, para estimar cómo podría comportarse un compuesto en el cuerpo. Los investigadores se preguntaron si estas medidas familiares podrían explicar el comportamiento en ratón de 100 PROTACs dirigidos al receptor del factor de crecimiento epidérmico (EGFR), un impulsor importante en muchos cánceres. Se centraron en tres propiedades clave: aclaramiento (qué tan rápido el organismo elimina el fármaco), vida media (cuánto tiempo permanece el fármaco en circulación) y volumen aparente de distribución (qué tan ampliamente se extiende hacia los tejidos). Al comparar estas propiedades con descriptores básicos, los puntos de datos estaban dispersos sin tendencias claras, lo que demuestra que las reglas químicas simples no bastan para predecir el comportamiento de los PROTACs.
Entrenando un motor de predicción a medida
Para superar esta laguna, el equipo construyó EGFR-PROPK, un predictor de aprendizaje automático ajustado específicamente a PROTACs dirigidos a EGFR. Primero realizaron estudios en ratón con 100 PROTACs diferentes, midiendo su aclaramiento, vida media y volumen de distribución tras la administración. Luego describieron cada molécula usando varios “fingerprints” ricos que codifican su estructura detallada y calcularon 200 características químicas adicionales. Estas descripciones numéricas se introdujeron en un modelo basado en CatBoost, un algoritmo moderno que sobresale encontrando patrones en datos tabulares. A diferencia de las herramientas de propósito general, EGFR-PROPK se entrenó directamente con resultados in vivo de PROTACs, lo que le permitió aprender relaciones sutiles entre formas complejas de los enlaces, el tamaño global y cuánto tiempo los fármacos permanecen en sangre o se distribuyen en tejidos.
Rendimiento superior a modelos generales y revelación de matices ocultos
Los investigadores compararon EGFR-PROPK con plataformas de predicción ampliamente usadas, desarrolladas principalmente para fármacos de pequeña molécula tradicionales. Cuando esos modelos genéricos se aplicaron “tal cual” a PROTACs, sus predicciones fueron pobres: los valores estimados de vida media, aclaramiento y distribución tisular a menudo se desviaron notablemente de las mediciones reales. Incluso después de afinar un modelo competidor con datos de PROTACs, éste siguió quedándose atrás. En contraste, EGFR-PROPK alcanzó una concordancia sustancialmente mayor entre valores predichos y experimentales, especialmente para vida media y aclaramiento, con mejoras moderadas en distribución. El modelo también manejó casos reales: dos PROTACs con estructuras muy similares pero comportamientos muy diferentes fueron distinguidos con mayor precisión por EGFR-PROPK que por las herramientas generales, subrayando la importancia de contar con datos de entrenamiento específicos para PROTACs.
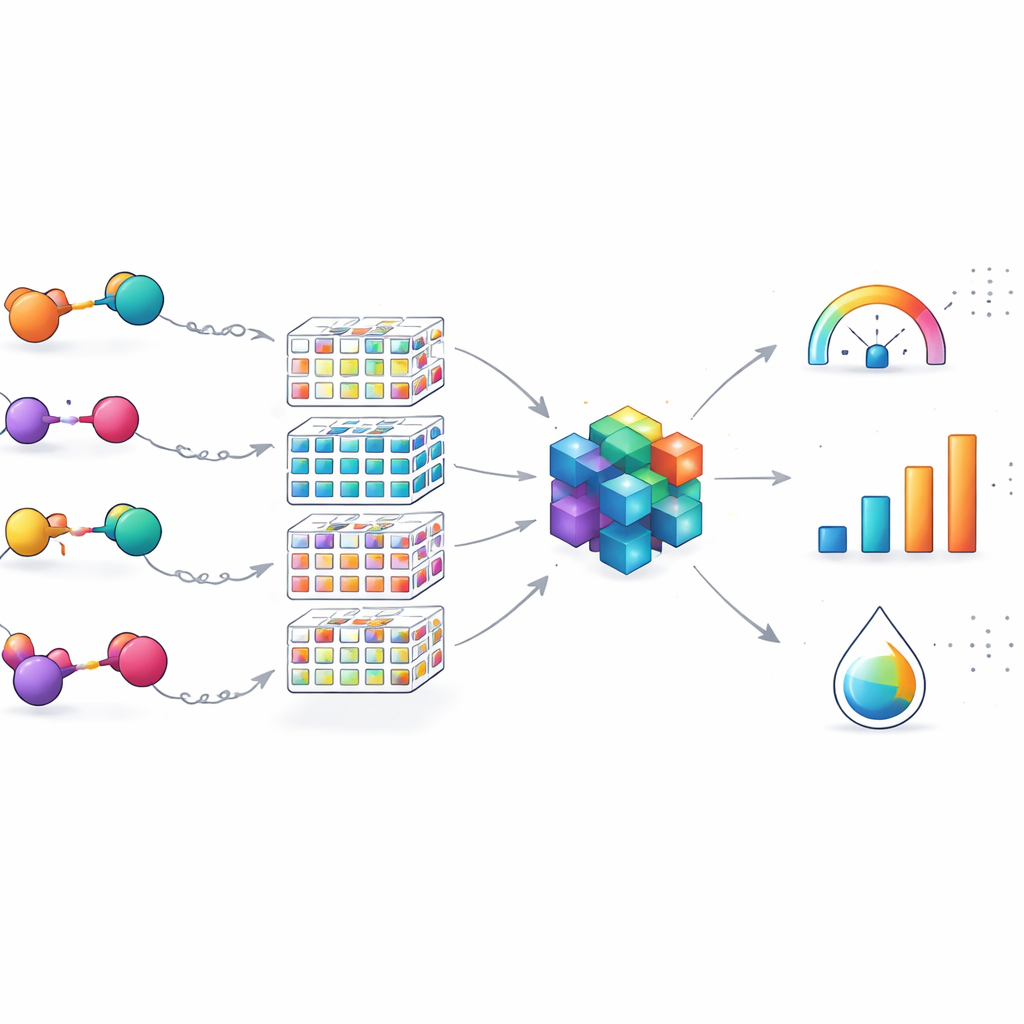
Trazando el paisaje químico y sus límites
Más allá de las cifras de rendimiento, el equipo comprobó si sus 100 PROTACs cubrían una amplia gama de diseños o sólo un rincón estrecho del espacio químico. Al reducir las moléculas a sus andamiajes principales y visualizarlas entre miles de PROTACs patentados, mostraron que su conjunto abarca muchos tipos estructurales distintos, especialmente en los enlaces flexibles. Esto significa que el modelo es adecuado para refinar PROTACs dirigidos a EGFR que comparten bloques de construcción clave pero varían en la forma en que sus partes se conectan. Al mismo tiempo, los autores enfatizan que la herramienta es especialista de dominio: su precisión puede disminuir para PROTACs construidos alrededor de dianas o vías de degradación completamente diferentes, lo que apunta a la necesidad de una futura expansión y aprendizaje por transferencia entre conjuntos de datos.
Qué implica esto para los medicamentos del futuro
Para el público no especializado, la conclusión principal es que la “plomería” de un fármaco en el cuerpo—cómo se absorbe, a dónde va y cuánto tiempo permanece—puede determinar el éxito o fracaso de una terapia anticancerígena prometedora, y los atajos habituales para comprimidos pequeños no funcionan bien para degradadores de nueva generación como los PROTACs. Al crear EGFR-PROPK, los investigadores muestran que datos animales cuidadosamente recogidos, combinados con métodos avanzados de reconocimiento de patrones, pueden ofrecer una visión temprana mucho más nítida de cómo se comportarán estas moléculas complejas. Este tipo de predicción a medida debería ayudar a los químicos a diseñar PROTACs que no solo destruyan las proteínas correctas, sino que también las alcancen en las concentraciones adecuadas, allanando el camino hacia tratamientos más eficaces y seguros contra cánceres resistentes.
Cita: Zhang, R., Li, F., Liu, Y. et al. A machine learning-based pharmacokinetics predictor (EGFR-PROPK) for EGFR-targeting PROTACs. Commun Chem 9, 134 (2026). https://doi.org/10.1038/s42004-026-01938-3
Palabras clave: Farmacocinética de PROTACs, Degradadores dirigidos a EGFR, aprendizaje automático en diseño de fármacos, predicción ADMET, degradación proteica dirigida