Clear Sky Science · ar
مُتنبئ حركية دوائية قائم على التعلم الآلي (EGFR-PROPK) لبروتاكات المستهدفة لمستقبلات EGFR
تصميم أذكى للأدوية لأنواع السرطان صعبة العلاج
يفشل العديد من الأدوية الجديدة الواعدة للسرطان ليس لأنّها تفشل في استهداف الهدف، بل لأنّ الجسم يطردها بسرعة كبيرة أو يخزنها في أماكن خاطئة أو لا يستطيع امتصاصها جيدًا. فئة جديدة من الأدوية تُدعى بروتاكات قادرة على تدمير بروتينات مسببة للمرض كانت تُعتبر سابقًا «غير قابلة للعلاج»، لكن سلوكها داخل الجسم يصعب التنبؤ به. تقدم هذه الدراسة أداة تعلم آلي، EGFR-PROPK، مصممة خصيصًا للتنبؤ بكيفية تحرك مجموعة من البروتاكات المضادة لبروتين سرطاني رئيسي داخل الجسم، بهدف مساعدة الباحثين على اختيار مرشحين أفضل مبكرًا وتوفير سنوات وموارد ضائعة على مسارات مسدودة.
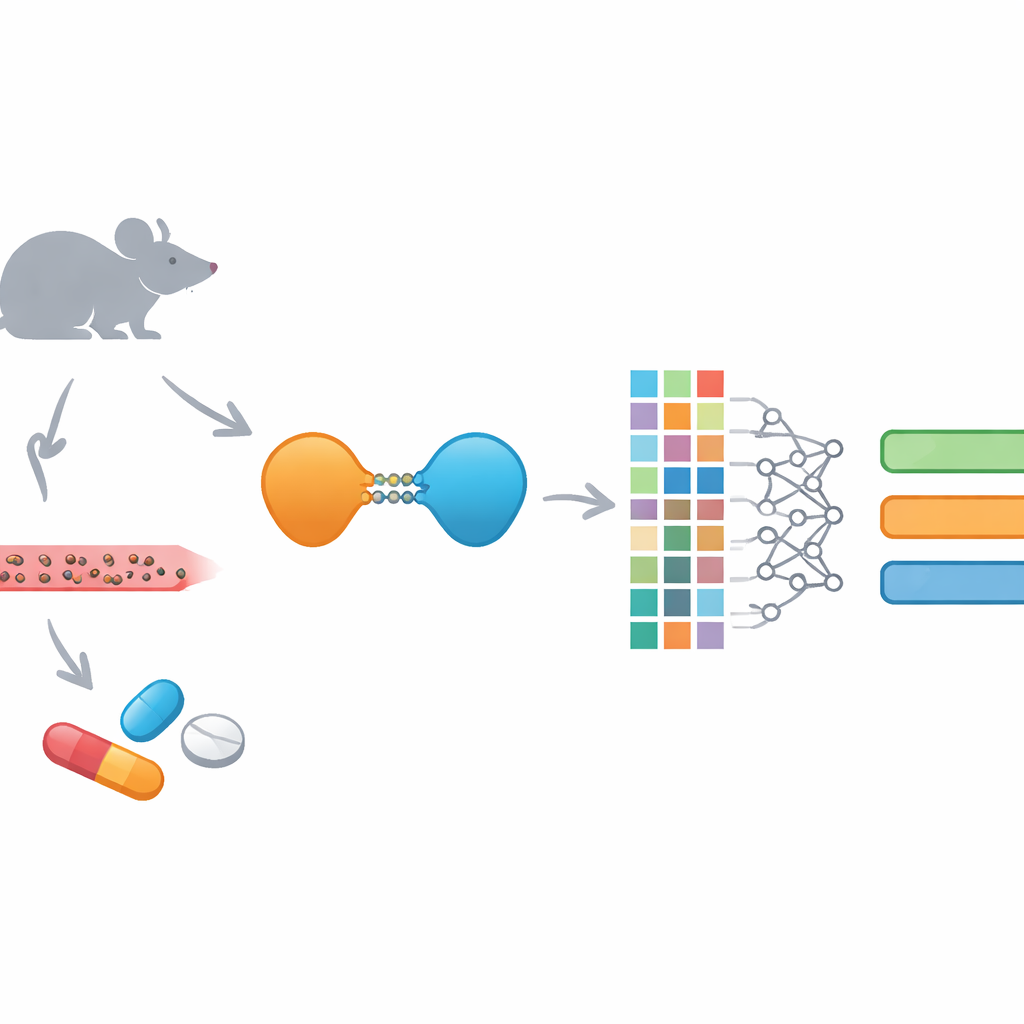
أدوية جديدة مدمرة للبروتينات وتحدياتها
البروتاكات أدوية غير عادية: بدلاً من مجرد حجب بروتين، تُعلِّم الخلية على تدميره عبر تجنيد آليات التخلص الخلوية. كل بروتاك يربط جزءًا يلتصق بالهدف المرضي بجزء آخر يجذب «المِهشِّم» الخلوي، مرتبطًا بسلسلة مرنة. يسمح هذا التصميم باستهداف بروتينات لا تستطيع الأدوية التقليدية الوصول إليها بسهولة وغالبًا يمكنه الارتباط مؤقتًا بدل الانشغال الدائم بموقع البروتين. ومع ذلك، فإن الحجم والتعقيد نفسه يجعلان توصيل البروتاكات والتحكم فيها داخل الجسم أمرًا صعبًا. فهي عادة ما تكون كبيرة، دهنية نسبيًا، وترتبط بقوة ببروتينات الدم، وكل ذلك يعقد امتصاصها وتوزيعها وتفكيكها وإزالتها.
لماذا القواعد التقليدية لسلوك الدواء لا تكفي
يستخدم مطورو الأدوية التقليديون مقاييس بسيطة، مثل الوزن الجزيئي، ومحبة الدهون (LogP)، وقواعد عامة لـ«شبيهة الدواء»، للتنبؤ بكيفية سلوك مركب ما في الجسم. بدأ الباحثون بسؤال ما إذا كانت هذه المقاييس المألوفة يمكنها تفسير سلوك 100 بروتاك تستهدف مستقبل عامل نمو البشرة (EGFR) — وهو مدفوع رئيسي في كثير من السرطانات — في فئران حية. ركزوا على ثلاث خصائص رئيسية: الإزالة (السرعة التي يطرد بها الجسم الدواء)، ونصف العمر (مدة بقاء الدواء في الدورة الدموية)، والحجم الظاهر للتوزيع (مدى انتشاره في الأنسجة). عندما قارنوا هذه الخصائص بمؤشرات بسيطة، تشتتّت نقاط البيانات بلا اتجاهات واضحة تقريبًا، مما أظهر أن القواعد الكيميائية البسيطة لا تكفي للتنبؤ بسلوك البروتاكات.
تدريب محرك تنبؤ مُفصّل
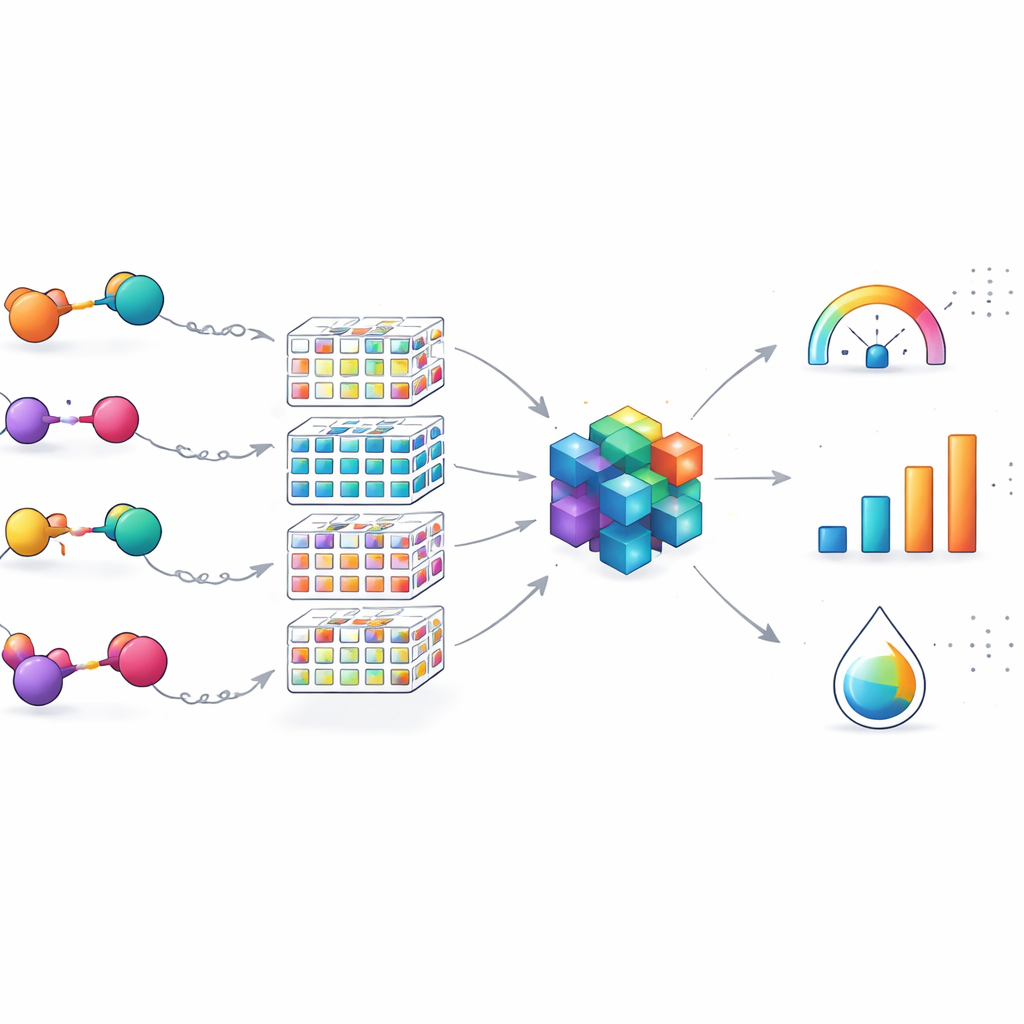
لتجاوز هذه الفجوة، بنى الفريق EGFR-PROPK، متنبئًا بالتعلم الآلي مخصّصًا لبروتاكات الموجّهة إلى EGFR. أجروا أولًا تجارب على الفئران لـ100 بروتاك مختلف، قاسوا فيها الإزالة ونصف العمر وحجم التوزيع بعد الجرعة. ثم وصفوا كل جزيء عبر عدة «بصمات» غنية تُشفِّر تركيبه التفصيلي وحسبوا 200 ميزة كيميائية إضافية. أدخلت هذه الأوصاف العددية إلى نموذج قائم على CatBoost، خوارزمية حديثة متفوقة في اكتشاف الأنماط في البيانات الجدولية. خلافًا للأدوات العامة، تم تدريب EGFR-PROPK مباشرة على نتائج حية للبروتاكات، مما أتاح له تعلم علاقات دقيقة بين أشكال الوصلات المعقّدة، والحجم الكلي، ومدة بقاء الأدوية في الدم أو انتشارها في الأنسجة.
تفوق على النماذج العامة وكشف فروق دقيقة مخفية
قارن الباحثون EGFR-PROPK بمنصات تنبؤ شائعة صممت في الأساس للأدوية الصغيرة التقليدية. عندما طُبِّقت تلك النماذج العامة «كما هي» على البروتاكات، كانت تنبؤاتها ضعيفة: القيم المقدرة لنصف العمر والإزالة وتوزيع الأنسجة انحرفت كثيرًا عن القياسات الحقيقية. حتى بعد تعديل نموذج منافس واحد ببيانات البروتاكات، ظل متخلفًا. بالمقابل، حقق EGFR-PROPK توافقًا أقوى بكثير بين القيم المتنبأ بها والتجريبية، خاصة لنصف العمر والإزالة، مع مكاسب معتدلة للتوزيع. كما تعامل النموذج مع دراسات حالة من العالم الحقيقي: بروتاكان لهما تراكيب متشابهة جدًا لكن سلوكهما مختلف جدًا تم تمييزهما بدقة أعلى بواسطة EGFR-PROPK مقارنة بالأدوات العامة، مما يؤكد أهمية بيانات تدريب خاصة بالبروتاكات.
رسم خريطة المناظر الكيميائية وحدودها
بعيدًا عن أرقام الأداء، تحقق الفريق فيما إذا كانت مجموعتهم المكونة من 100 بروتاك تغطي نطاقًا واسعًا من التصاميم أو مجرد زاوية ضيقة من الفضاء الكيميائي. عبر تبسيط الجزيئات إلى هياكلها الأساسية وتصويرها ضمن آلاف البروتاكات المسجلة ببراءات اختراع، أظهروا أن مجموعتهم تمتد إلى العديد من الأنواع التركيبية المختلفة، خصوصًا في الوصلات المرنة. هذا يعني أن النموذج مناسب لتحسين بروتاكات موجهة إلى EGFR تشترك في لبنات بناء رئيسية لكنها تختلف في كيفية ربط أجزائها. وفي الوقت نفسه، يؤكد المؤلفون أن الأداة متخصصة في نطاق معين: دقتها قد تنخفض بالنسبة لبروتاكات بُنيت حول أهداف مختلفة تمامًا أو مسارات تحلل بديلة، مما يشير إلى الحاجة إلى توسيع وتعليم نقلي مستقبلي عبر مجموعات بيانات أخرى.
ماذا يعني هذا للأدوية المستقبلية
لغير المتخصصين، الخلاصة الرئيسية أن «سباكة» الدواء داخل الجسم — كيفية امتصاصه وإلى أين يذهب وكم يستمر — يمكن أن تصنع الفارق في نجاح علاج سرطاني واعد، والقواعد المختصرة المعتادة للأقراص الصغيرة لا تعمل جيدًا مع الجيل التالي من المُحللات مثل البروتاكات. عبر إنشاء EGFR-PROPK، يظهر الباحثون أن بيانات حيوانية مُجمّعة بعناية، مدموجة بأساليب متقدمة لاكتشاف الأنماط، يمكن أن تعطي نظرة مبكرة أكثر وضوحًا على كيفية تصرّف هذه الجزيئات المعقّدة. ينبغي أن تساعد هذه التنبؤات المخصّصة الكيميائيين على تصميم بروتاكات لا تدمّر فقط البروتينات الصحيحة، بل تصل إليها بالمستويات المناسبة، ممهِّدة الطريق لعلاجات أكثر فعالية وأمانًا ضد السرطانات المقاومة.
الاستشهاد: Zhang, R., Li, F., Liu, Y. et al. A machine learning-based pharmacokinetics predictor (EGFR-PROPK) for EGFR-targeting PROTACs. Commun Chem 9, 134 (2026). https://doi.org/10.1038/s42004-026-01938-3
الكلمات المفتاحية: حركية دوائية لبروتاكات, مُحللات مستهدفة لمستقبل EGFR, التعلم الآلي في تصميم الأدوية, تنبؤ ADMET, التحلل المستهدف للبروتينات