Clear Sky Science · pt
Um preditor farmacocinético baseado em aprendizado de máquina (EGFR-PROPK) para PROTACs que miram EGFR
Design de fármacos mais inteligente para cânceres difíceis de tratar
Muitos medicamentos promissores contra o câncer fracassam não porque não atinjam seu alvo, mas porque o corpo os elimina rápido demais, os armazena em locais indesejados ou não os absorve bem. Uma nova classe de fármacos chamada PROTACs pode destruir proteínas causadoras de doença que antes eram consideradas “indrugáveis”, mas seu comportamento no organismo é particularmente difícil de prever. Este estudo apresenta uma ferramenta de aprendizado de máquina, EGFR-PROPK, projetada especificamente para prever como um grupo de PROTACs contra uma proteína cancerígena chave se desloca pelo corpo, com o objetivo de ajudar cientistas a escolher candidatos a fármaco melhores mais cedo e desperdiçar menos anos e recursos em becos sem saída.
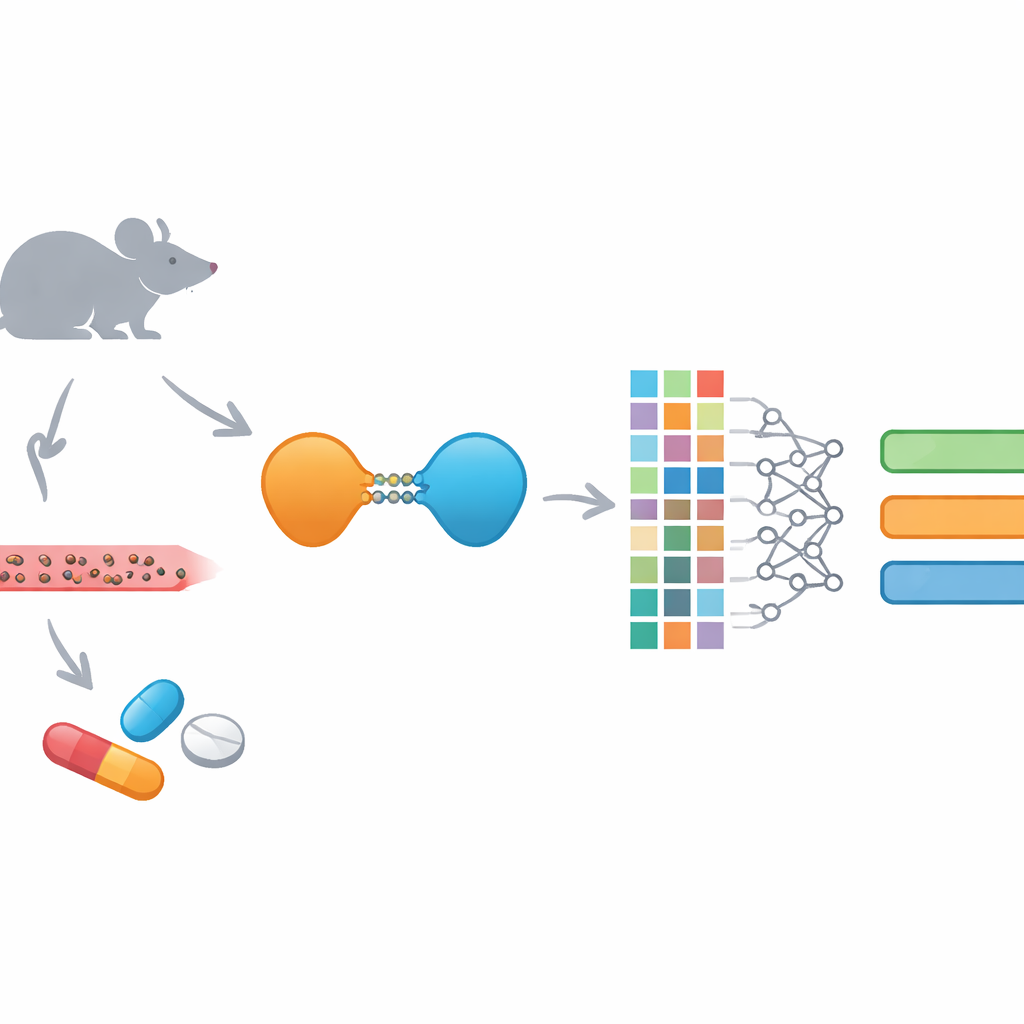
Novos fármacos que destroem proteínas e seus desafios
PROTACs são fármacos incomuns: em vez de apenas bloquear uma proteína, eles a marcam para destruição pela própria maquinaria de eliminação da célula. Cada PROTAC liga uma peça que se une ao alvo da doença a outra que recruta um “digeridor” celular, conectadas por uma cadeia flexível. Esse desenho permite que ataquem proteínas que fármacos convencionais não alcançam facilmente e frequentemente possibilita ligação temporária em vez de ocupação constante do sítio proteico. Contudo, esse mesmo tamanho e complexidade tornam os PROTACs difíceis de administrar e controlar no organismo. Eles tendem a ser grandes, relativamente lipofílicos e fortemente ligados a proteínas sanguíneas, fatores que complicam sua absorção, distribuição, metabolização e eliminação.
Por que as regras usuais de comportamento de fármacos falham
Desenvolvedores tradicionais de fármacos usam números simples, como peso molecular, afinidade por gordura (LogP) e medidas empíricas de “características de fármaco”, para estimar como um composto se comportará no corpo. Os pesquisadores perguntaram-se se essas medidas familiares poderiam explicar como 100 PROTACs que visam o receptor do fator de crescimento epidérmico (EGFR) — um condutor importante em muitos cânceres — se comportam em camundongos vivos. Eles focalizaram três propriedades chave: depuração (quão rápido o corpo remove o fármaco), meia-vida (quanto tempo o fármaco permanece na circulação) e volume aparente de distribuição (quão amplamente se espalha pelos tecidos). Ao comparar essas propriedades com descritores básicos, os pontos de dados estavam dispersos sem tendências claras, mostrando que regras químicas simples não são suficientes para prever o comportamento de PROTACs.
Treinando um motor de previsão sob medida
Para superar essa lacuna, a equipe construiu o EGFR-PROPK, um preditor de aprendizado de máquina afinado especificamente para PROTACs direcionados ao EGFR. Primeiro, realizaram estudos em camundongos com 100 PROTACs diferentes, medindo sua depuração, meia-vida e volume de distribuição após administração. Em seguida, descreveram cada molécula usando vários “impressões digitais” ricas que codificam sua estrutura detalhada e calcularam 200 características químicas adicionais. Essas descrições numéricas foram fornecidas a um modelo baseado em CatBoost, um algoritmo moderno que se destaca em encontrar padrões em dados tabulares. Diferente de ferramentas de uso geral, o EGFR-PROPK foi treinado diretamente com resultados in vivo para PROTACs, permitindo que aprendesse relações sutis entre formas complexas de linkers, tamanho geral e quanto tempo os fármacos permanecem no sangue ou se distribuem nos tecidos.
Superando modelos gerais e revelando nuances ocultas
Os pesquisadores compararam o EGFR-PROPK com plataformas de previsão amplamente usadas, desenvolvidas principalmente para fármacos tradicionais de pequena molécula. Quando esses modelos genéricos foram aplicados “como estão” aos PROTACs, suas previsões foram ruins: valores estimados para meia-vida, depuração e distribuição tecidual frequentemente divergiram fortemente das medições reais. Mesmo após um modelo concorrente ser ajustado com dados de PROTACs, ainda ficou atrás. Em contraste, o EGFR-PROPK alcançou concordância substancialmente melhor entre valores previstos e experimentais, especialmente para meia-vida e depuração, com ganhos moderados na distribuição. O modelo também lidou com estudos de caso do mundo real: dois PROTACs com estruturas muito semelhantes, mas comportamentos muito diferentes, foram distinguidos com mais precisão pelo EGFR-PROPK do que por ferramentas gerais, ressaltando a importância de dados de treinamento específicos para PROTACs.
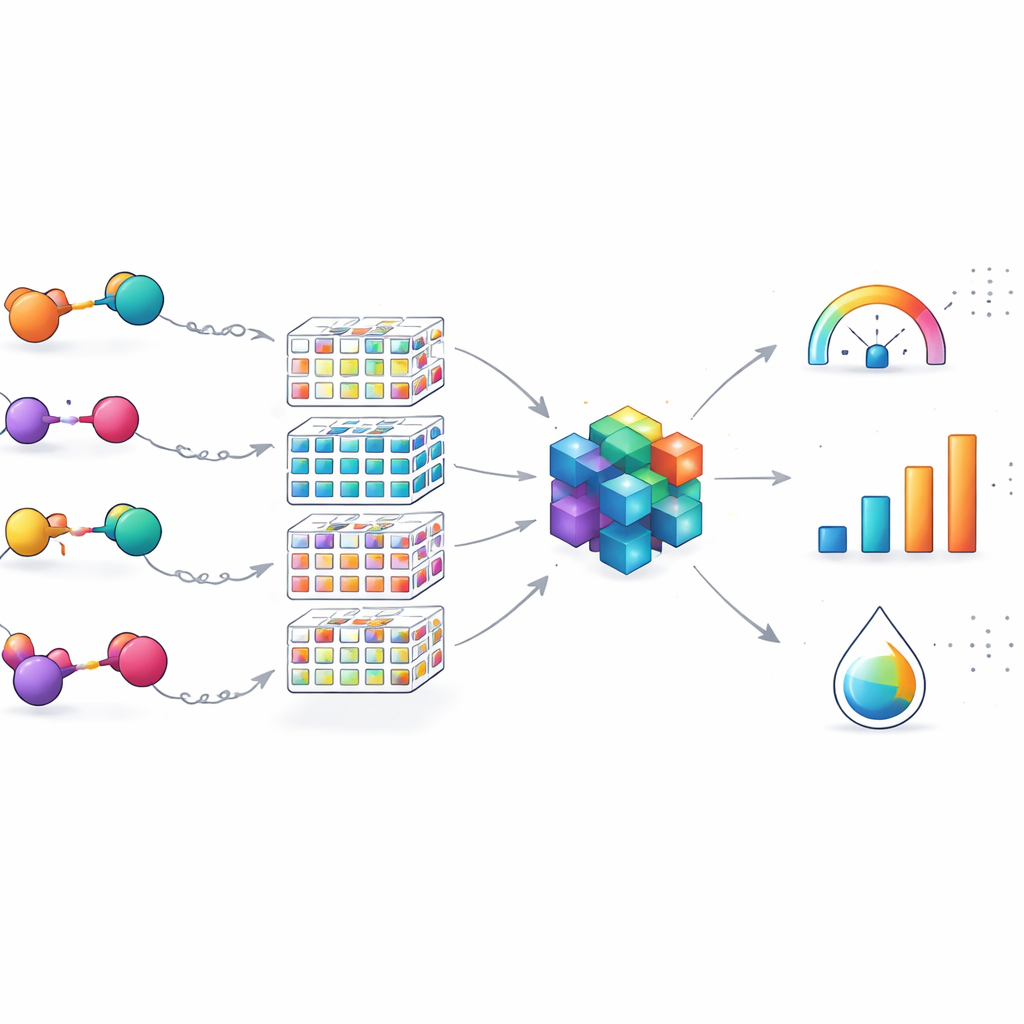
Mapeando a paisagem química e seus limites
Além dos números de desempenho, a equipe verificou se seus 100 PROTACs cobriam uma ampla gama de designs ou apenas um canto estreito do espaço químico. Ao reduzir as moléculas aos seus andaimes centrais e visualizá-las entre milhares de PROTACs patenteados, mostraram que o conjunto abrange muitos tipos estruturais distintos, especialmente nos linkers flexíveis. Isso significa que o modelo é bem adequado para refinar PROTACs direcionados ao EGFR que compartilham blocos construtivos chave, mas variam na forma como suas partes estão conectadas. Ao mesmo tempo, os autores enfatizam que a ferramenta é uma especialista de domínio: sua precisão pode cair para PROTACs construídos em torno de alvos ou vias de degradação inteiramente diferentes, apontando para a necessidade de expansão futura e de aprendizagem por transferência entre conjuntos de dados.
O que isso significa para medicamentos futuros
Para não especialistas, a principal conclusão é que a “plumbing” de um fármaco no organismo — como ele é absorvido, para onde vai e quanto tempo permanece — pode fazer ou destruir uma terapia contra o câncer promissora, e os atalhos usuais para comprimidos pequenos não funcionam bem para degradadores de nova geração como os PROTACs. Ao criar o EGFR-PROPK, os pesquisadores mostram que dados animais cuidadosamente coletados, combinados com métodos avançados de reconhecimento de padrões, podem fornecer um retrato inicial muito mais preciso de como essas moléculas complexas se comportarão. Esse tipo de previsão sob medida deve ajudar químicos a projetar PROTACs que não apenas destruam as proteínas certas, mas também as alcancem nos níveis corretos, abrindo caminho para tratamentos mais eficazes e seguros contra cânceres resistentes.
Citação: Zhang, R., Li, F., Liu, Y. et al. A machine learning-based pharmacokinetics predictor (EGFR-PROPK) for EGFR-targeting PROTACs. Commun Chem 9, 134 (2026). https://doi.org/10.1038/s42004-026-01938-3
Palavras-chave: farmacocinética de PROTACs, degradadores direcionados a EGFR, aprendizado de máquina no design de fármacos, previsão ADMET, degradação proteica direcionada