Clear Sky Science · pl
Predyktor farmakokinetyczny oparty na uczeniu maszynowym (EGFR-PROPK) dla PROTAC-ów ukierunkowanych na EGFR
Inteligentniejsze projektowanie leków na trudne do leczenia nowotwory
Wiele obiecujących nowych leków przeciwnowotworowych zawodzi nie dlatego, że nie trafiają w cel, lecz dlatego, że organizm zbyt szybko je usuwa, gromadzi w nieodpowiednich miejscach lub nie wchłania ich skutecznie. Nowa klasa leków zwana PROTAC-ami potrafi zniszczyć białka wywołujące chorobę, które dawniej uważano za „nieleczalne”, ale ich zachowanie w organizmie jest szczególnie trudne do przewidzenia. W tym badaniu przedstawiono narzędzie oparte na uczeniu maszynowym, EGFR-PROPK, zaprojektowane specjalnie do prognozowania, jak grupa PROTAC-ów przeciwko kluczowemu białku nowotworowemu przemieszcza się po organizmie, z celem pomocy naukowcom w wcześniejszym wybieraniu lepszych kandydatów na leki i zmniejszaniu marnotrawstwa lat oraz zasobów na ślepe uliczki.
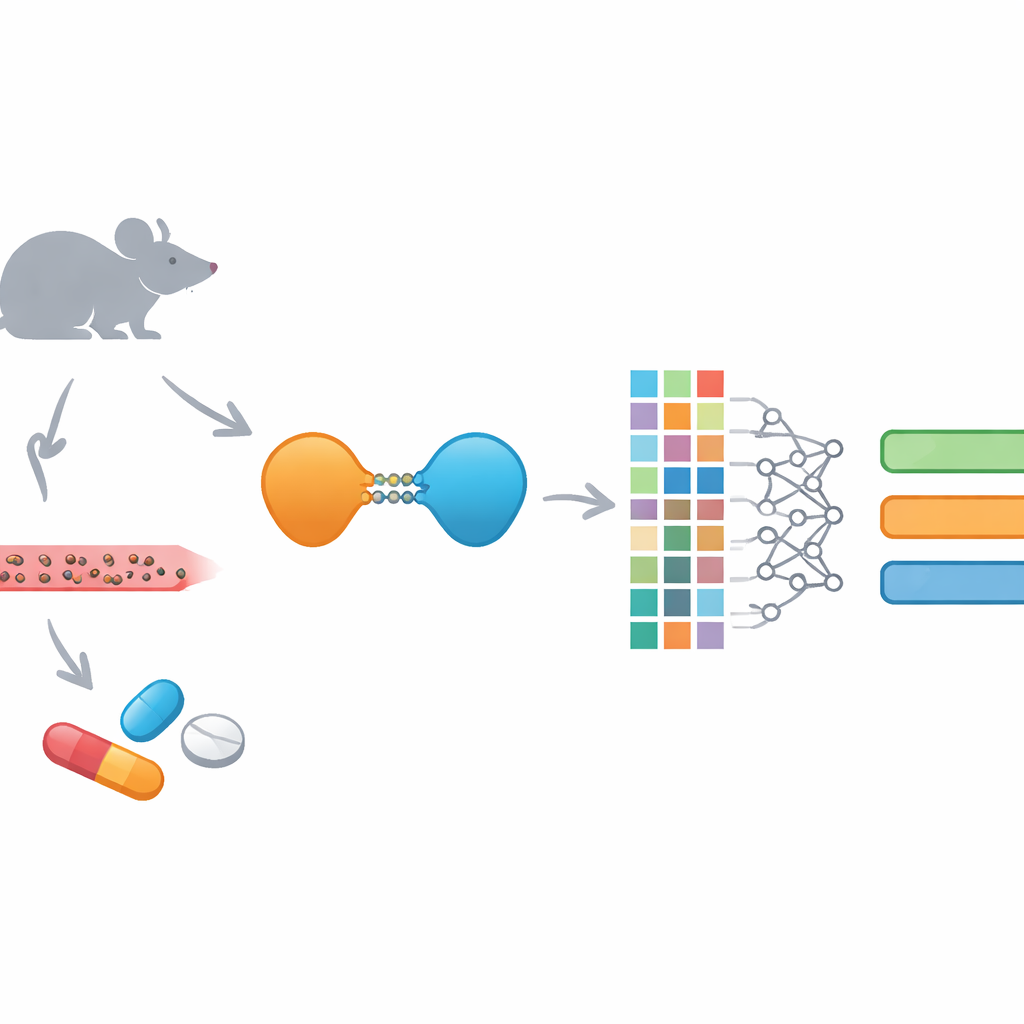
Nowe leki niszczące białka i ich wyzwania
PROTAC-y to nietypowe leki: zamiast jedynie blokować białko, oznaczają je do zniszczenia przez komórkowe mechanizmy usuwania. Każdy PROTAC łączy fragment wiążący cel chorobowy z fragmentem rekrutującym komórkowy „niszczyciel”, połączone elastycznym łącznikiem. Taka konstrukcja pozwala im atakować białka, do których zwykłe leki mają utrudniony dostęp, i często umożliwia wiązanie tymczasowe zamiast stałego zajmowania miejsca na białku. Jednak ta sama wielkość i złożoność utrudniają dostarczanie i kontrolę PROTAC-ów w organizmie. Mają tendencję do bycia dużymi, stosunkowo lipofilowymi i silnie wiążącymi białka krwi, co komplikuje ich wchłanianie, dystrybucję, rozkład i usuwanie.
Dlaczego zwykłe reguły dotyczące zachowania leków zawodzą
Tradycyjni twórcy leków używają prostych wskaźników, takich jak masa cząsteczkowa, lipofilowość (LogP) i reguły „drug-likeness”, aby przewidzieć, jak związek może zachować się w organizmie. Badacze zaczęli od pytania, czy te znane miary wytłumaczą zachowanie 100 PROTAC-ów ukierunkowanych na receptor naskórkowego czynnika wzrostu (EGFR) — kluczowy czynnik w wielu nowotworach — u żywych myszy. Skupili się na trzech właściwościach: klirensie (jak szybko organizm usuwa lek), okresie półtrwania (jak długo lek krąży we krwi) oraz pozornym wole dystrybucji (jak szeroko rozprzestrzenia się w tkankach). Porównanie tych właściwości z podstawowymi deskryptorami wykazało rozproszone punkty danych bez wyraźnych trendów, co pokazuje, że proste reguły chemiczne nie wystarczają do przewidzenia zachowania PROTAC-ów.
Szkolenie specjalistycznego silnika predykcyjnego
Aby przezwyciężyć tę lukę, zespół zbudował EGFR-PROPK, predyktor uczenia maszynowego dostrojony specjalnie do PROTAC-ów ukierunkowanych na EGFR. Najpierw przeprowadzili badania na myszach z 100 różnymi PROTAC-ami, mierząc ich klirens, półtrwanie i objętość dystrybucji po podaniu. Następnie opisali każdą cząsteczkę za pomocą kilku bogatych „odcisków palców” kodujących szczegółową strukturę oraz obliczyli 200 dodatkowych cech chemicznych. Te numeryczne opisy wprowadzono do modelu opartego na CatBoost — nowoczesnego algorytmu świetnie radzącego sobie z wyszukiwaniem wzorców w danych tabelarycznych. W przeciwieństwie do narzędzi ogólnego przeznaczenia, EGFR-PROPK był trenowany bezpośrednio na wynikach in vivo dla PROTAC-ów, co pozwoliło mu uchwycić subtelne zależności między złożonymi kształtami łączników, ogólną wielkością a tym, jak długo leki pozostają we krwi lub rozchodzą się do tkanek.
Przewyższając modele ogólne i ujawniając ukryte niuanse
Badacze porównali EGFR-PROPK z powszechnie używanymi platformami predykcyjnymi stworzonymi głównie dla tradycyjnych leków małocząsteczkowych. Gdy te ogólne modele zastosowano „tak jak są” do PROTAC-ów, ich prognozy były słabe: szacowane wartości półtrwania, klirensu i dystrybucji tkanek często znacznie odbiegały od rzeczywistych pomiarów. Nawet po dostrojeniu jednego z konkurencyjnych modeli danymi PROTAC-ów wciąż nie dorównywał on wydajności. W przeciwieństwie do tego EGFR-PROPK osiągnął znacznie lepszą zgodność między wartościami przewidywanymi a eksperymentalnymi, szczególnie dla okresu półtrwania i klirensu, z umiarkowaną poprawą dla dystrybucji. Model poradził sobie także z rzeczywistymi przypadkami: dwa PROTAC-i o bardzo podobnych strukturach, lecz odmiennym zachowaniu, zostały dokładniej rozróżnione przez EGFR-PROPK niż przez ogólne narzędzia, podkreślając wagę danych treningowych specyficznych dla PROTAC-ów.
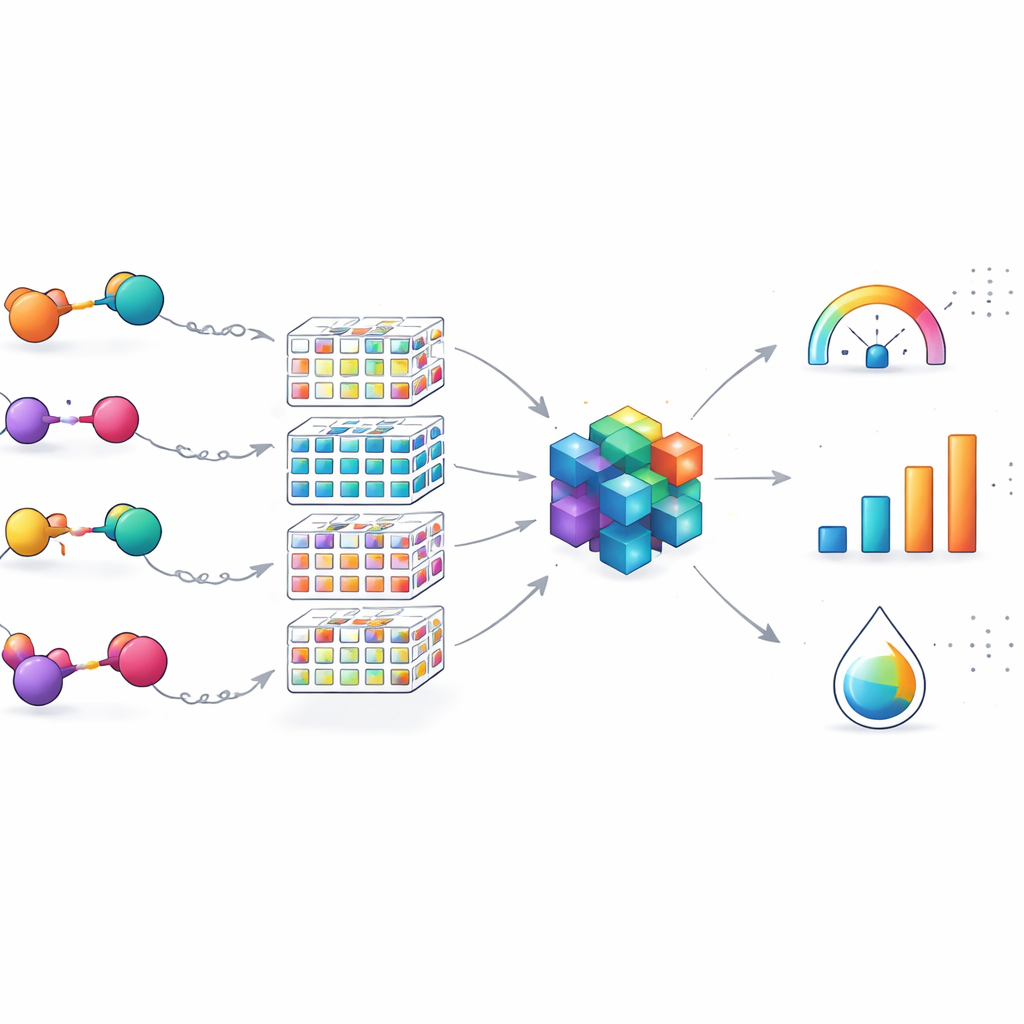
Mapowanie krajobrazu chemicznego i jego ograniczeń
Ponad liczby opisujące wydajność, zespół sprawdził, czy ich 100 PROTAC-ów obejmuje szeroki zakres projektów, czy tylko wąski wycinek przestrzeni chemicznej. Poprzez sprowadzenie cząsteczek do rdzeniowych szkieletów i wizualizację ich wśród tysięcy opatentowanych PROTAC-ów, pokazali, że ich zestaw obejmuje wiele odmiennych typów strukturalnych, szczególnie w elastycznych łącznikach. Oznacza to, że model dobrze nadaje się do udoskonalania PROTAC-ów skierowanych na EGFR, które dzielą kluczowe elementy budulcowe, ale różnią się sposobem łączenia części. Jednocześnie autorzy podkreślają, że narzędzie jest specjalistą dziedzinowym: jego dokładność może spadać dla PROTAC-ów zbudowanych wokół zupełnie innych celów lub szlaków degradacji, co wskazuje na potrzebę rozszerzenia i transferu uczenia między zestawami danych w przyszłości.
Co to oznacza dla przyszłych leków
Dla osób niebędących ekspertami główne przesłanie jest takie, że „instalacja” leku w organizmie — jak jest wchłaniany, dokąd trafia i jak długo tam zostaje — może przesądzić o sukcesie obiecującej terapii przeciwnowotworowej, a zwykłe skróty stosowane dla małych tabletek nie sprawdzają się dobrze przy nowej generacji degraderów takich jak PROTAC-y. Tworząc EGFR-PROPK, badacze pokazali, że starannie zebrane dane zwierzęce, połączone z zaawansowanymi metodami rozpoznawania wzorców, mogą dać znacznie lepszy, wczesny obraz tego, jak te złożone cząsteczki będą się zachowywać. Tego rodzaju specjalistyczna predykcja powinna pomóc chemikom projektować PROTAC-y, które nie tylko niszczą właściwe białka, ale także docierają do nich we właściwych stężeniach, torując drogę do skuteczniejszych i bezpieczniejszych terapii przeciwko opornym nowotworom.
Cytowanie: Zhang, R., Li, F., Liu, Y. et al. A machine learning-based pharmacokinetics predictor (EGFR-PROPK) for EGFR-targeting PROTACs. Commun Chem 9, 134 (2026). https://doi.org/10.1038/s42004-026-01938-3
Słowa kluczowe: farmakokinetyka PROTAC, degradery ukierunkowane na EGFR, uczenie maszynowe w projektowaniu leków, predykcja ADMET, ukierunkowana degradacja białek