Clear Sky Science · sv
Mekanistiska insikter i strukturen och funktionen hos RecA:s C-terminala svans
Hur bakterier hanterar DNA‑stress
Bakterier utsätts ständigt för faktorer som skadar deras DNA, från antibiotika till strålning. Ändå överlever de ofta och blir ibland svårare att utrota. Denna studie granskar noggrant ett centralt bakteriellt protein kallat RecA, som hjälper till att reparera brutet DNA och att starta ett nödläge kallat SOS‑responsen. Författarna fokuserar på en liten, flexibel svans i ena änden av RecA som länge undgått strukturella studier, och visar hur denna lilla del fungerar som en inbyggd broms och strömbrytare för DNA‑reparation och överlevnad vid antibiotikapåverkan.
En molekylär första blick på en dold svans
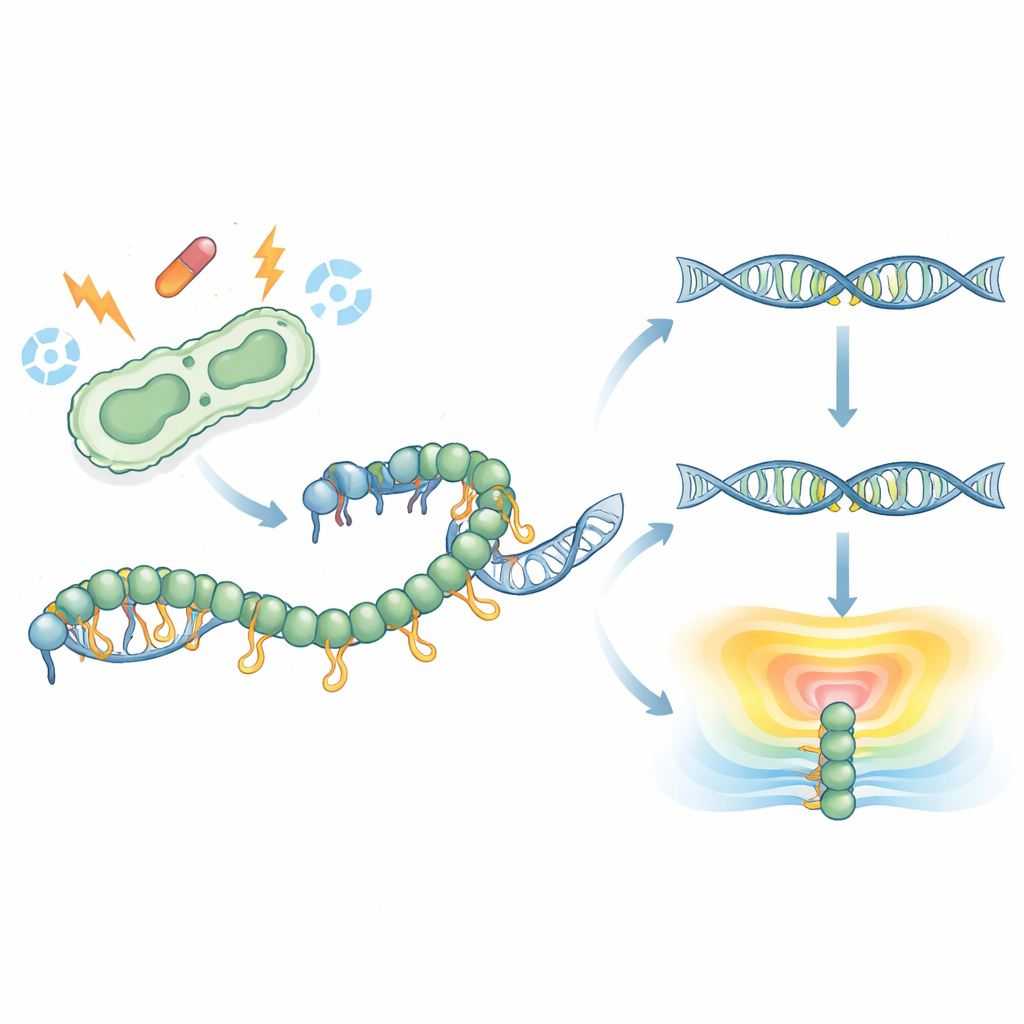
RecA lindar sig runt enkelsträngat DNA för att bilda ett filament som driver DNA‑reparation och aktiverar SOS‑responsen. Tidigare strukturer hade aldrig fångat RecA:s rörliga C‑terminala svans, vilket lämnade dess roll mystisk. Här löste forskarna en högupplöst kristallstruktur av fullängds RecA från patogenen Klebsiella pneumoniae bundet till en ATP‑lik molekyl. Till sin förvåning veckade sig en del av svansen till en kort, ordnad remsa och nådde över för att kontakta motorregionen i en RecA‑molekyl i ett intilliggande filament. Denna interaktion förenar negativa laddningar på svansen med positiva laddningar i kärnan och avslöjar ett tidigare osett sätt på vilket RecA‑molekyler kan röra vid varandra och sammansättas till högre ordnade strukturer.
En inbyggd broms på DNA‑bindning och reparation
Eftersom svansen sitter nära RecA:s DNA‑bindande regioner testade teamet hur den påverkar kontakten med DNA. Med gel‑shift‑tester visade de att RecA‑varianter som saknade svansen, eller bar laddningsändrande förändringar i svansen, grep både enkelsträngat och dubbelsträngat DNA hårdare än det normala proteinet. Elektronmikroskopi bekräftade att dessa förändrade proteiner byggde längre RecA‑filament på korta DNA‑stycken än vad fullängdsproteinet gjorde. I direkta strandbytesexperiment, som efterliknar hjärtat av homolog rekombination, utförde svanslösa eller svansmutanta RecA DNA‑utbyte mer effektivt. Tillsammans visar dessa resultat att svansen normalt fungerar som ett autoinhibitoriskt element: den gör det svårare för RecA att binda DNA, att förlänga sig längs det och att genomföra genetiskt strandbyte, vilket hjälper till att förhindra okontrollerad rekombination på intakta kromosomer.
Finjustering av bakteriens SOS‑larm
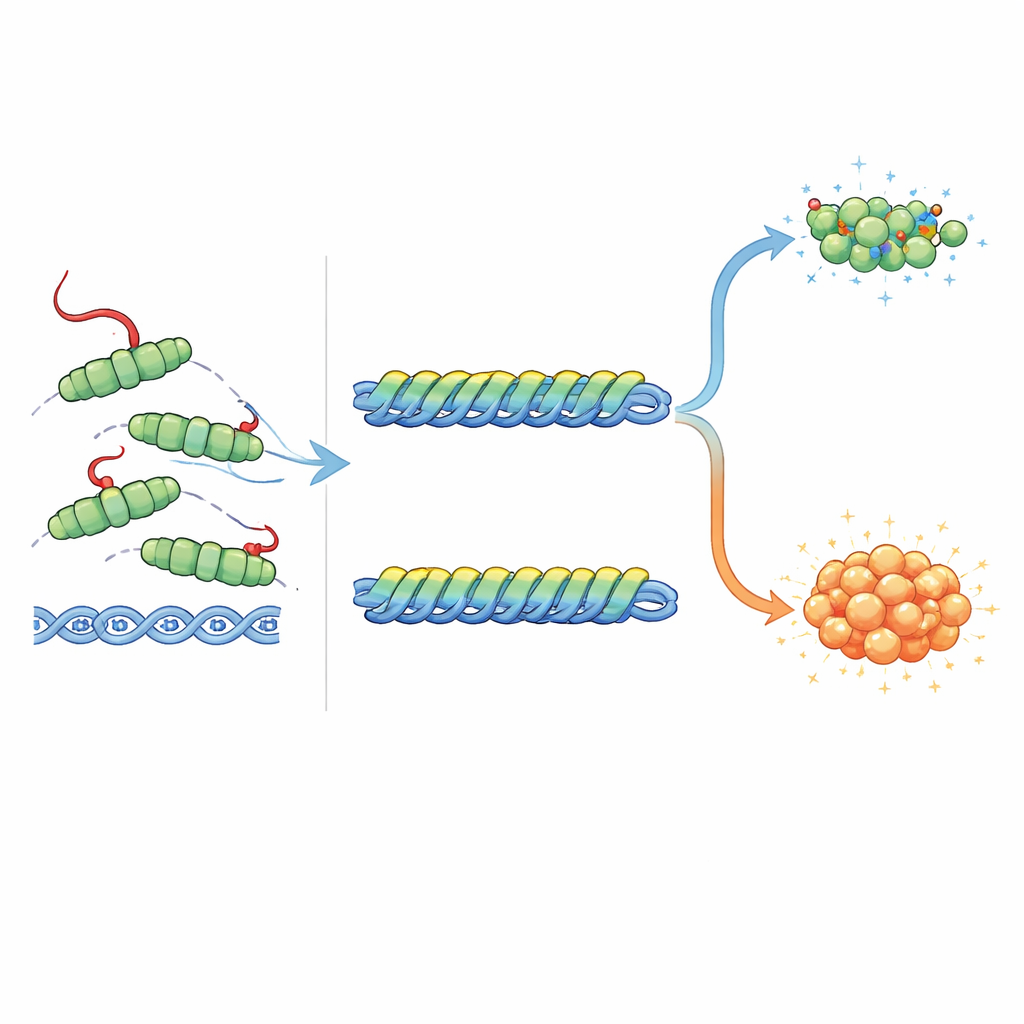
RecA:s uppgift är inte bara att reparera DNA utan också att utlösa SOS‑responsen genom att hjälpa två andra proteiner, LexA och UmuD, att klyva sig själva. LexA håller normalt SOS‑gener tysta; när det klipps, slås dessa gener på. Klyvning av UmuD ger en partner till en särskild felbenägen DNA‑polymeras som kan kopiera förbi skador men också introducerar mutationer. Författarna fann att RecA‑svansen har motsatta effekter på dessa två självklippningar. FullängdsRecA, med sin intakta svans, var bäst på att främja LexA‑klyvning, medan svanslösa eller starkt förändrade varianter var sämre. Därmed var samma svanslösa och mutanta former bättre på att stimulera UmuD‑klyvning än det normala proteinet. Strukturella jämförelser föreslår varför: svansen kan sitta bekvämt nära bundet LexA och till och med bilda gynnsamma laddningsinteraktioner, men den skulle kollidera både fysiskt och elektrostatik med bundet UmuD′. Med andra ord hjälper svansen till att slå på SOS‑larmet samtidigt som den dämpar den mest mutationsdrivna delen av responsen.
Påverkan på antibiotikasvar i levande celler
För att pröva hur detta spelar ut inuti bakterier konstruerade forskarna Escherichia coli‑stammar där en fluorescerande rapportör lyser när en tidig SOS‑gen kallad recN aktiveras. De behandlade sedan dessa stammar med två DNA‑skadande läkemedel: mitomycin C och det vida använda antibiotikumet ciprofloxacin. Celler med normal RecA visade stark SOS‑aktivering. Celler som saknade svansen gav däremot mycket svagare fluorescenssignaler, i överensstämmelse med minskad LexA‑klyvning och en dämpad SOS‑respons. Mutanta svansar som stärkte DNA‑bindning och filamentbildning drev däremot ofta en ännu starkare SOS‑respons. Dessa in‑cell‑resultat stämmer med de biokemiska fynden och understryker svansens roll i att balansera reparation, överlevnad och mutation under antibiotikabelastning.
Varför denna lilla svans är viktig
Detta arbete avslöjar RecA:s C‑terminala svans som en subtil men kraftfull regulator av bakteriellt genomunderhåll. Genom att kontakta proteinets kärna och fösa DNA och partnerproteiner antingen närmare eller längre bort bromsar svansen filamenttillväxt och DNA‑strandbyte, hjälper till att säkerställa att SOS‑responsen utlöses på lämpligt sätt via LexA, och dämpar överdriven mutagen reparation via UmuD. För allmänheten är detta viktigt eftersom RecA och SOS‑systemet påverkar hur snabbt bakterier utvecklar resistens mot antibiotika. Att förstå denna lilla svanss strukturella och funktionella knep kan i framtiden vägleda designen av läkemedel som tippar balansen mot reparation utan okontrollerade mutationer, vilket gör befintliga antibiotika effektivare längre.
Citering: Su, L., Li, X., Wang, F. et al. Mechanistic insights into the structure and function of the RecA C-terminal tail. Commun Biol 9, 526 (2026). https://doi.org/10.1038/s42003-026-09788-4
Nyckelord: RecA-protein, SOS-respons, DNA-reparation, antibiotikaresistens, bakteriell genomstabilitet