Clear Sky Science · it
Approfondimenti meccanicistici sulla struttura e funzione della coda C-terminale di RecA
Come i batteri gestiscono lo stress del DNA
I batteri sono costantemente esposti a agenti che danneggiano il DNA, dagli antibiotici alle radiazioni. Eppure spesso sopravvivono e diventano persino più difficili da eliminare. Questo studio esamina da vicino una proteina batterica chiave chiamata RecA, che aiuta a riparare il DNA rotto e ad attivare un programma di emergenza noto come risposta SOS. Gli autori si concentrano su una piccola coda flessibile a un'estremità di RecA che a lungo era sfuggita agli studi strutturali, e mostrano come questo frammento agisca come un freno e un interruttore integrati per la riparazione del DNA e la sopravvivenza agli antibiotici.
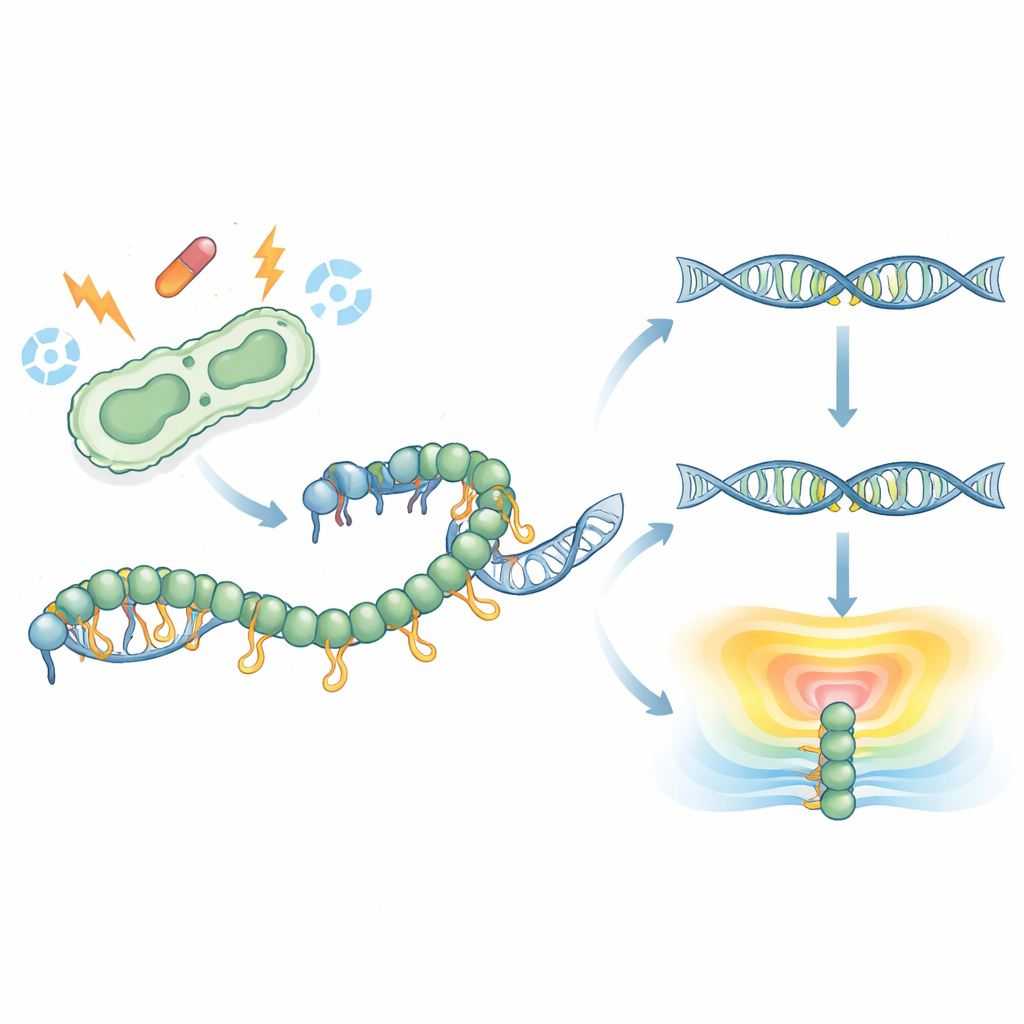
Una prima occhiata molecolare a una coda nascosta
RecA si avvolge attorno a filamenti singoli di DNA per formare un filamento che guida la riparazione del DNA e attiva la risposta SOS. Strutture precedenti non avevano mai catturato la coda C-terminale floscia di RecA, lasciandone misterioso il ruolo. Qui, i ricercatori hanno risolto una struttura cristallina ad alta risoluzione di RecA a lunghezza intera del patogeno Klebsiella pneumoniae legato a una molecola simile all'ATP. Con loro sorpresa, parte della coda si è ripiegata in una corta striscia ordinata e si è estesa per contattare la regione motrice centrale di una molecola di RecA in un filamento adiacente. Questa interazione unisce cariche negative sulla coda a cariche positive sul nucleo, rivelando un modo finora non osservato in cui le molecole di RecA possono toccarsi e assemblarsi in strutture di ordine superiore.
Un freno integrato sul legame al DNA e sulla riparazione
Poiché la coda si trova vicino alle regioni di legame al DNA di RecA, il team ha testato come essa influenzi il contatto con il DNA. Utilizzando saggi di spostamento su gel, hanno mostrato che versioni di RecA prive della coda, o portatrici di modifiche che alterano la carica nella coda, si legavano sia al DNA a singolo filamento sia a doppio filamento più saldamente della proteina normale. La microscopia elettronica ha confermato che queste proteine alterate costruivano filamenti di RecA più lunghi su pezzi corti di DNA rispetto alla proteina a lunghezza intera. In esperimenti diretti di scambio di filamenti, che imitano il cuore della ricombinazione omologa, RecA privo di coda o con mutazioni nella coda eseguiva lo scambio di DNA in modo più efficiente. Nel complesso, questi risultati mostrano che la coda agisce normalmente come un elemento autoinibitorio: rende più difficile per RecA legare il DNA, estendersi lungo di esso e svolgere lo scambio di filamenti genetici, contribuendo a prevenire ricombinazioni incontrollate sui cromosomi intatti.
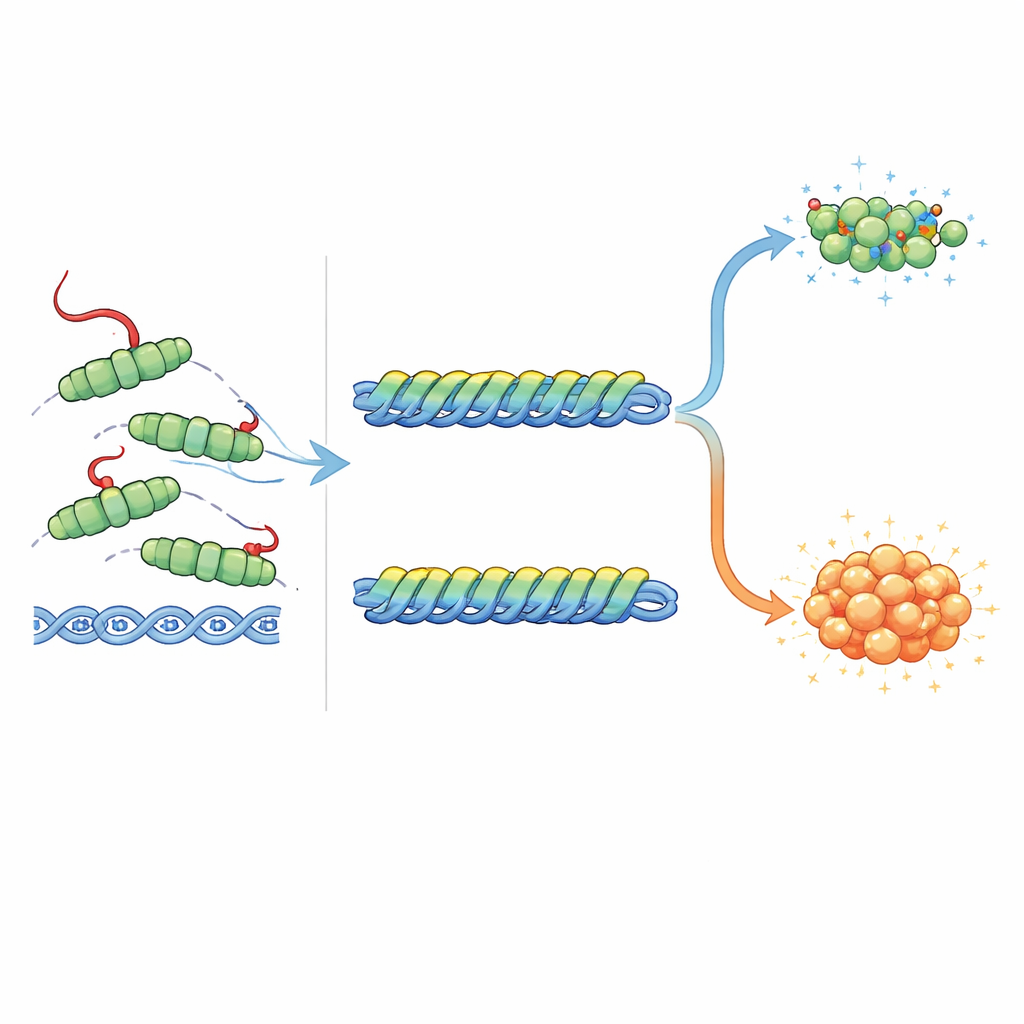
Affinare l'allarme SOS batterico
Il compito di RecA non è solo riparare il DNA ma anche attivare la risposta SOS aiutando altre due proteine, LexA e UmuD, a tagliarsi. LexA normalmente mantiene silenti i geni SOS; quando viene clivata, quei geni si attivano. Il clivaggio di UmuD produce un partner per una DNA polimerasi speciale e incline all'errore che può copiare oltre il danno ma introduce anche mutazioni. Gli autori hanno scoperto che la coda di RecA ha effetti opposti su questi due autoclivaggi. RecA a lunghezza intera, con la coda intatta, era il migliore nel promuovere il clivaggio di LexA, mentre le versioni senza coda o fortemente alterate erano meno efficaci. Al contrario, le stesse forme senza coda e mutate erano più efficaci nello stimolare il clivaggio di UmuD rispetto alla proteina normale. Confronti strutturali suggeriscono il perché: la coda può sedersi comodamente vicino a LexA legata e persino formare interazioni di carica favorevoli, ma si scontrerebbe fisicamente ed elettrostaticamente con UmuD′ legato. In altre parole, la coda aiuta ad attivare l'allarme SOS limitando al contempo il braccio più mutageno della risposta.
Impatto sulla risposta antibiotica nelle cellule viventi
Per verificare come ciò si traduca all'interno dei batteri, i ricercatori hanno ingegnerizzato ceppi di Escherichia coli in cui un reporter fluorescente si illumina quando un gene SOS precoce chiamato recN viene attivato. Hanno quindi trattato questi ceppi con due farmaci che danneggiano il DNA: mitomicina C e il comune antibiotico ciprofloxacina. Le cellule con RecA normale hanno mostrato una forte attivazione SOS. Le cellule prive della coda, tuttavia, hanno prodotto segnali fluorescenti molto più deboli, coerenti con una ridotta clivaggio di LexA e una risposta SOS attenuata. Le code mutate che rafforzavano il legame al DNA e la formazione di filamenti, al contrario, spesso hanno indotto una risposta SOS ancora più intensa. Questi risultati in cellule corrispondono alle osservazioni biochimiche e sottolineano il ruolo della coda nell'equilibrare riparazione, sopravvivenza e mutazione sotto stress da antibiotici.
Perché questa piccola coda è importante
Questo lavoro rivela la coda C-terminale di RecA come un regolatore sottile ma potente della manutenzione del genoma batterico. Contattando il nucleo della proteina e avvicinando o allontanando il DNA e le proteine partner, la coda rallenta la crescita del filamento e lo scambio di filamenti del DNA, aiuta a garantire che la risposta SOS sia attivata appropriatamente tramite LexA e attenua una riparazione eccessivamente mutagena attraverso UmuD. Per il pubblico più ampio, questo è importante perché RecA e il sistema SOS influenzano la velocità con cui i batteri evolvono la resistenza agli antibiotici. Comprendere i trucchi strutturali e funzionali di questa piccola coda potrebbe, in futuro, guidare la progettazione di farmaci che spostino l'equilibrio verso la riparazione senza mutazioni incontrollate, rendendo gli antibiotici esistenti più efficaci più a lungo.
Citazione: Su, L., Li, X., Wang, F. et al. Mechanistic insights into the structure and function of the RecA C-terminal tail. Commun Biol 9, 526 (2026). https://doi.org/10.1038/s42003-026-09788-4
Parole chiave: Proteina RecA, risposta SOS, riparazione del DNA, resistenza agli antibiotici, stabilità del genoma batterico