Clear Sky Science · pl
Mechanistyczne wglądy w strukturę i funkcję ogonka C-końcowego białka RecA
Jak bakterie radzą sobie ze stresem DNA
Bakterie są nieustannie narażone na czynniki uszkadzające ich DNA, od antybiotyków po promieniowanie. Mimo to często przetrwają, a czasem stają się trudniejsze do zwalczenia. W tym badaniu analizowano szczegółowo kluczowe białko bakteryjne RecA, które pomaga naprawiać przerwane DNA i uruchamiać alarmowy program zwany odpowiedzią SOS. Autorzy koncentrują się na małym, elastycznym ogonku na jednym końcu RecA, który długo umykał badaniom strukturalnym, i pokazują, jak ten drobny fragment działa jako wewnętrzny hamulec i przełącznik dla naprawy DNA i przeżywalności w obecności antybiotyków.
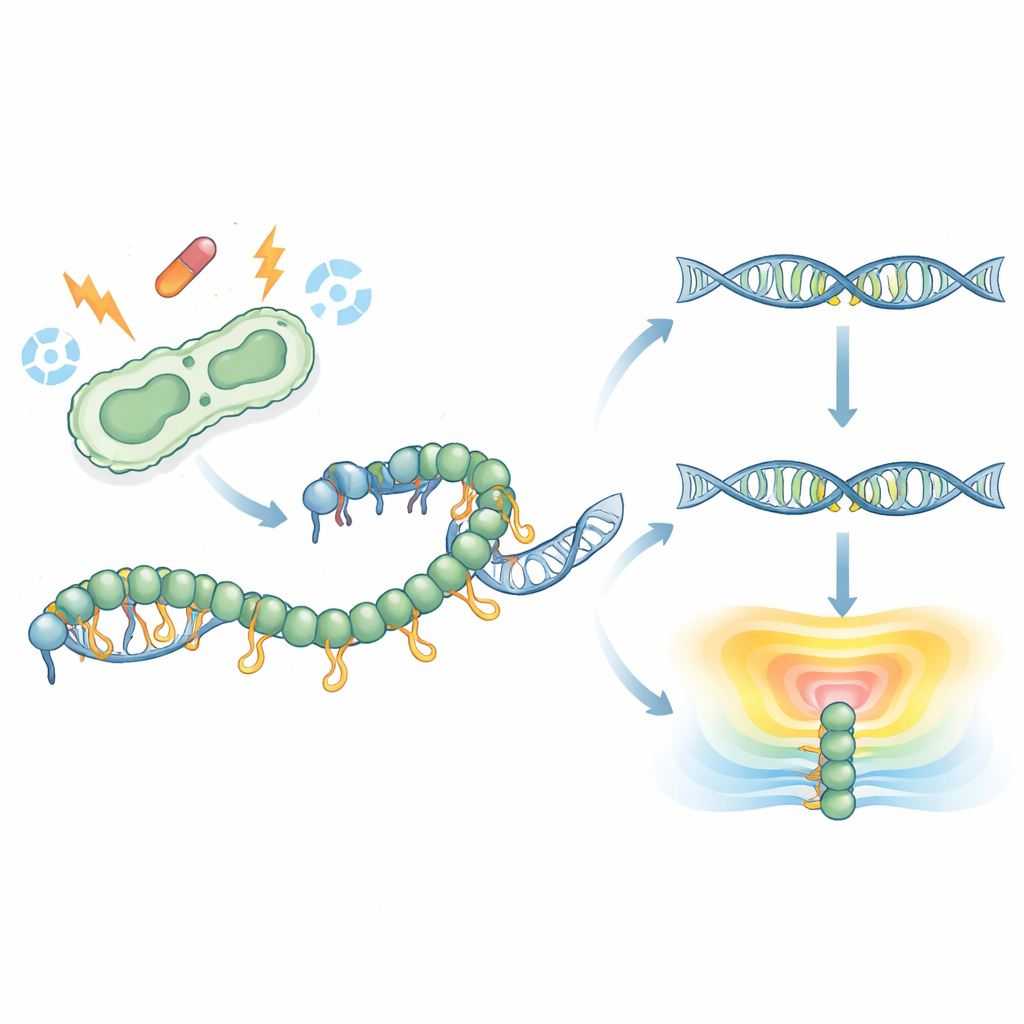
Molekularne pierwsze spojrzenie na ukryty ogonek
RecA owija się wokół jednoniciowego DNA, tworząc filament, który napędza naprawę DNA i aktywuje odpowiedź SOS. Wcześniejsze struktury nigdy nie uchwyciły wiotkiego ogonka C‑końcowego RecA, dlatego jego rola była tajemnicą. Tutaj badacze rozwiąazali strukturę krystaliczną pełnej długości RecA pochodzącego od patogenu Klebsiella pneumoniae, związanej z cząsteczką podobną do ATP, o wysokiej rozdzielczości. Ku ich zaskoczeniu część ogonka złożyła się w krótki, uporządkowany pas i dosięgała do centralnej części napędowej cząsteczki RecA w sąsiednim filamentie. Ta interakcja łączy ujemne ładunki na ogonku z dodatnimi ładunkami rdzenia, ujawniając wcześniej nieznany sposób, w jaki cząsteczki RecA mogą się stykać i tworzyć struktury wyższych rzędów.
Wbudowany hamulec wiązania i naprawy DNA
Ponieważ ogonek leży blisko regionów wiążących DNA w RecA, zespół przebadał, jak wpływa na kontakt z DNA. Za pomocą testów przesunięcia w żelu wykazali, że wersje RecA pozbawione ogonka lub niosące zmiany zmieniające ładunek w ogonku wiązały zarówno DNA jednoniciowe, jak i dwuniciowe silniej niż białko w formie naturalnej. Mikroskopia elektronowa potwierdziła, że te zmienione białka tworzyły dłuższe filamenty RecA na krótkich fragmentach DNA niż pełnej długości białko. W bezpośrednich eksperymentach wymiany nici, które naśladują sedno rekombinacji homologicznej, RecA bez ogonka lub z mutacjami w ogonku przeprowadzały wymianę DNA wydajniej. Razem te wyniki pokazują, że ogonek działa normalnie jako element auto‑inhibitory: utrudnia RecA wiązanie DNA, wydłużanie filamentu i przeprowadzanie wymiany nici genetycznych, pomagając zapobiegać gwałtownej rekombinacji w nieuszkodzonych chromosomach.
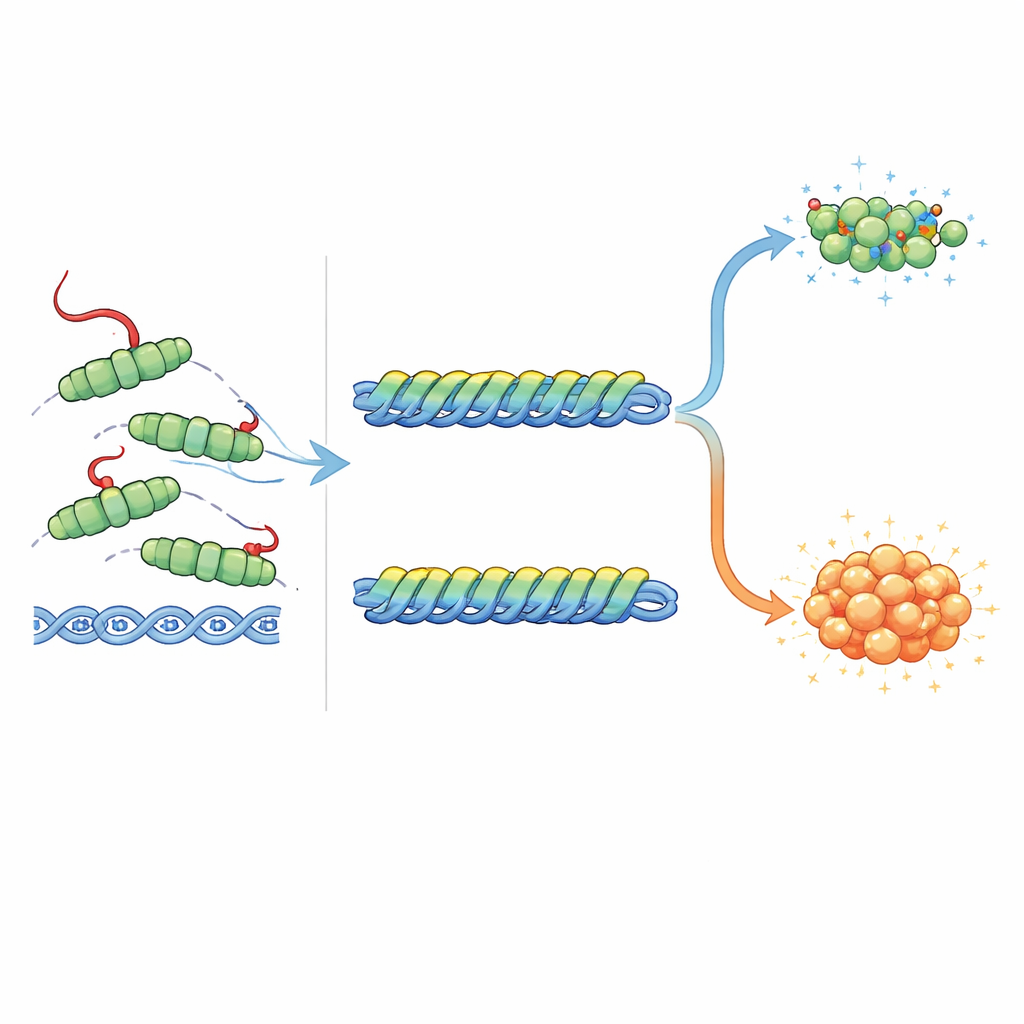
Dostrajanie alarmu SOS w bakteriach
Rola RecA nie ogranicza się do naprawy DNA — pomaga on także wyzwolić odpowiedź SOS, ułatwiając samocięcie dwóch innych białek, LexA i UmuD. LexA normalnie utrzymuje geny SOS w stanie nieaktywnym; po przecięciu te geny się włączają. Cięcie UmuD tworzy partnera dla specjalnej, błędoprzepuszczalnej polimerazy DNA, która potrafi przepisać uszkodzenia, ale także wprowadza mutacje. Autorzy wykazali, że ogonek RecA ma przeciwstawne efekty na te dwa autocięcia. RecA w pełnej długości, z nienaruszonym ogonkiem, najlepiej promował cięcie LexA, podczas gdy formy bez ogonka lub silnie zmienione były w tym gorsze. W przeciwieństwie do tego, te same formy bez ogonka i mutanty lepiej stymulowały cięcie UmuD niż białko normalne. Porównania strukturalne sugerują dlaczego: ogonek może siedzieć komfortowo blisko związanego LexA i nawet tworzyć korzystne interakcje ładunkowe, lecz fizycznie i elektrostatycznie kolidowałby z związanym UmuD′. Innymi słowy, ogonek pomaga włączyć alarm SOS, jednocześnie powstrzymując najbardziej mutagenną odnogę tej odpowiedzi.
Wpływ na reakcję na antybiotyki w żywych komórkach
Aby sprawdzić, jak to działa w komórkach, badacze skonstruowali szczepy Escherichia coli, w których fluorescencyjny reporter świeci, gdy aktywowany jest wczesny gen SOS o nazwie recN. Następnie traktowali te szczepy dwoma czynnikami uszkadzającymi DNA: mitomycyną C i powszechnie stosowanym antybiotykiem ciprofloksacyną. Komórki noszące normalny RecA wykazywały silną aktywację SOS. Komórki pozbawione ogonka jednak wytwarzały znacznie słabsze sygnały fluorescencyjne, co odpowiada zmniejszonemu cięciu LexA i stłumionej odpowiedzi SOS. Mutanty ogonka, które wzmacniały wiązanie DNA i tworzenie filamentów, przeciwnie, często wywoływały jeszcze silniejszą odpowiedź SOS. Wyniki z komórek zgodne są z danymi biochemicznymi i podkreślają rolę ogonka w równoważeniu naprawy, przeżycia i mutacji pod stresem antybiotykowym.
Dlaczego ten mały ogonek ma znaczenie
Praca ta ujawnia ogonek C‑końcowy RecA jako subtelny, lecz potężny regulator utrzymania genomu bakteryjnego. Poprzez kontakt z rdzeniem białka i przesuwanie DNA oraz białek‑partnerów bliżej lub dalej, ogonek spowalnia wzrost filamentu i wymianę nici DNA, pomaga zapewnić właściwe wyzwalanie odpowiedzi SOS przez LexA i tłumi nadmierną, mutagenną naprawę przez UmuD. Dla szerokiej publiczności ma to znaczenie, ponieważ RecA i system SOS wpływają na tempo, w jakim bakterie nabywają oporność na antybiotyki. Zrozumienie strukturalnych i funkcjonalnych sztuczek tego maleńkiego ogonka mogłoby w przyszłości poprowadzić projekt leków, które przesuną równowagę w stronę naprawy bez niekontrolowanych mutacji, przedłużając skuteczność istniejących antybiotyków.
Cytowanie: Su, L., Li, X., Wang, F. et al. Mechanistic insights into the structure and function of the RecA C-terminal tail. Commun Biol 9, 526 (2026). https://doi.org/10.1038/s42003-026-09788-4
Słowa kluczowe: białko RecA, odpowiedź SOS, naprawa DNA, oporność na antybiotyki, stabilność genomu bakteryjnego