Clear Sky Science · fr
Perspicacités mécanistiques sur la structure et la fonction de la queue C-terminale de RecA
Comment les bactéries gèrent le stress de l'ADN
Les bactéries sont constamment exposées à des agents qui endommagent leur ADN, des antibiotiques aux radiations. Pourtant, elles survivent souvent et deviennent parfois plus difficiles à éliminer. Cette étude examine de près une protéine bactérienne clé, RecA, qui aide à réparer l'ADN cassé et à déclencher un programme d'urgence connu sous le nom de réponse SOS. Les auteurs se concentrent sur une petite queue flexible à une extrémité de RecA, longtemps inaccessible aux études structurales, et montrent comment ce fragment agit comme un frein et un commutateur intégrés pour la réparation de l'ADN et la survie face aux antibiotiques.
Un premier regard moléculaire sur une queue cachée
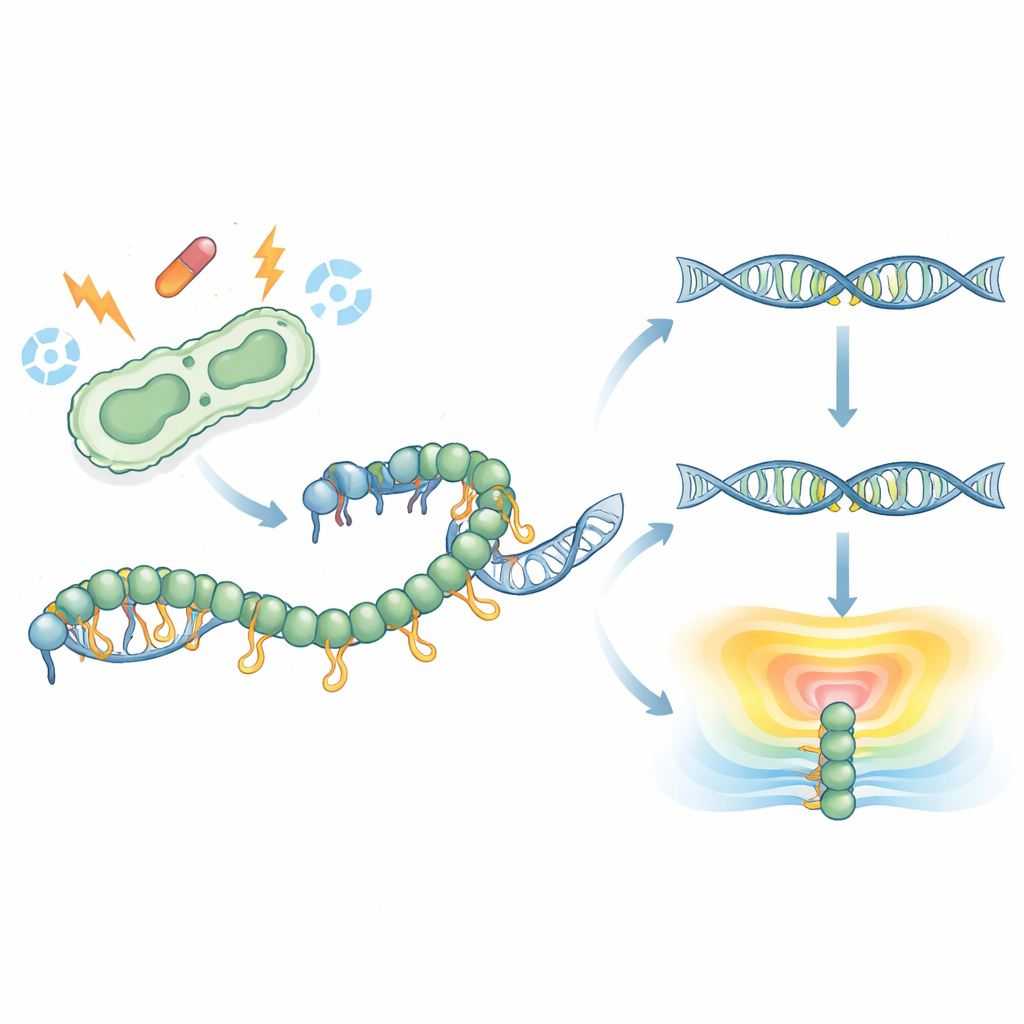
RecA s'enroule autour de brins simples d'ADN pour former un filament qui pilote la réparation de l'ADN et active la réponse SOS. Les structures antérieures n'avaient jamais capturé la queue C-terminale souple de RecA, laissant son rôle mystérieux. Ici, les chercheurs ont résolu une structure cristalline haute résolution de RecA en pleine longueur provenant du pathogène Klebsiella pneumoniae liée à une molécule analogue de l'ATP. À leur surprise, une partie de la queue s'est repliée en une courte bande ordonnée et est venue contacter la région motrice centrale d'une molécule de RecA dans un filament voisin. Cette interaction réunit des charges négatives de la queue avec des charges positives du noyau, révélant une manière jusque-là non vue par laquelle les molécules de RecA peuvent se toucher et s'assembler en structures d'ordre supérieur.
Un frein intégré sur la liaison à l'ADN et la réparation
Parce que la queue se situe près des régions de liaison à l'ADN de RecA, l'équipe a testé son influence sur le contact avec l'ADN. À l'aide d'essais de migration sur gel, ils ont montré que des versions de RecA dépourvues de la queue, ou portant des modifications changeant la charge de la queue, se liaient plus fermement aux ADN simple brin et double brin que la protéine normale. La microscopie électronique a confirmé que ces protéines altérées formaient des filaments RecA plus longs sur de courts fragments d'ADN que la protéine en pleine longueur. Dans des expériences d'échange de brins directes, qui reproduisent le cœur de la recombinaison homologue, RecA sans queue ou muté effectuait l'échange d'ADN plus efficacement. Ensemble, ces résultats montrent que la queue agit normalement comme un élément d'auto-inhibition : elle rend plus difficile pour RecA de se lier à l'ADN, de s'y étendre et d'exécuter l'échange de brins génétiques, aidant à prévenir une recombinaison incontrôlée sur des chromosomes intacts.
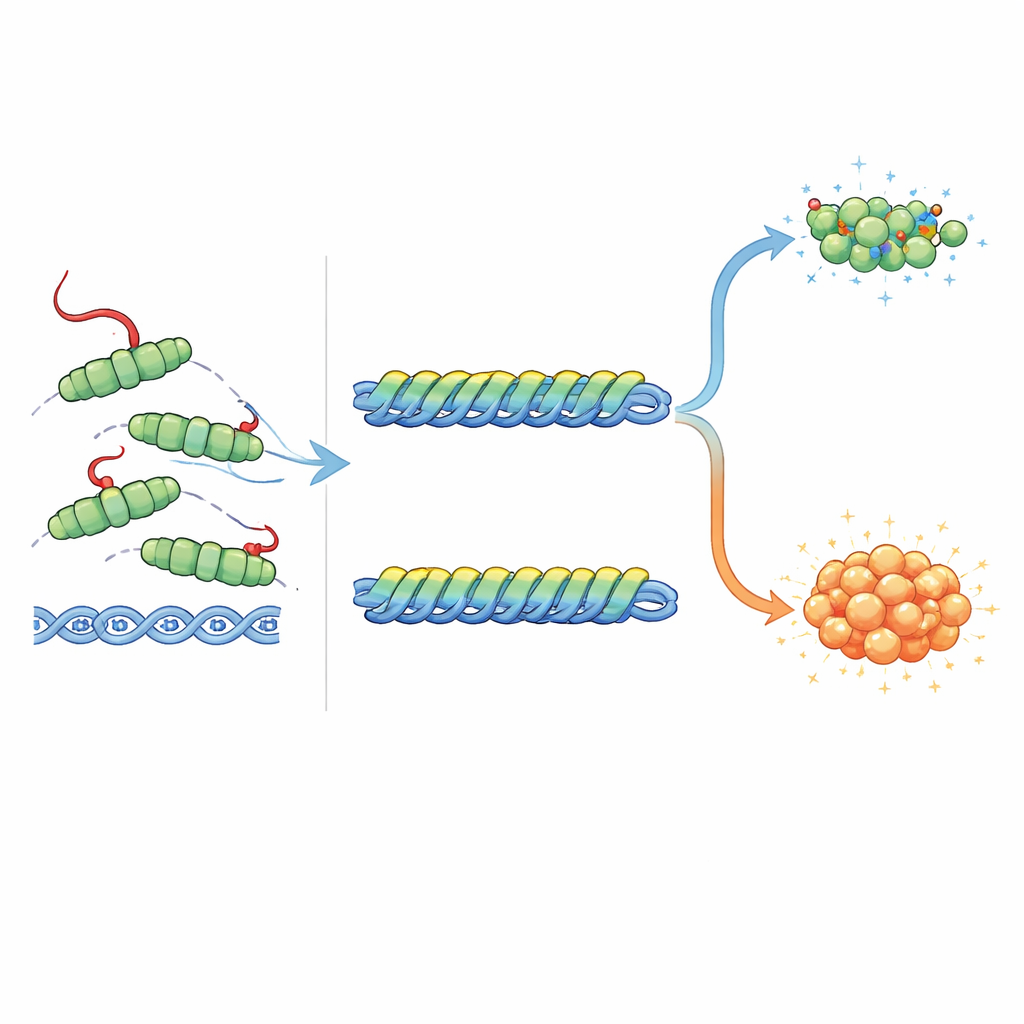
Ajuster finement l'alerte SOS bactérienne
Le rôle de RecA n'est pas seulement de réparer l'ADN mais aussi de déclencher la réponse SOS en aidant deux autres protéines, LexA et UmuD, à se cliver elles-mêmes. LexA maintient normalement les gènes SOS silencieux ; lorsqu'il est clivé, ces gènes s'activent. La clivage d'UmuD produit un partenaire pour une ADN polymérase spéciale, sujette aux erreurs, capable de franchir les dommages mais introduisant aussi des mutations. Les auteurs ont constaté que la queue de RecA a des effets opposés sur ces deux auto-clivages. RecA en pleine longueur, avec sa queue intacte, favorisait le mieux le clivage de LexA, tandis que les versions sans queue ou fortement altérées l'étaient moins. En revanche, les formes sans queue et mutantes stimulaient mieux le clivage d'UmuD que la protéine normale. Les comparaisons structurelles suggèrent pourquoi : la queue peut se loger confortablement près de LexA lié et même former des interactions de charge favorables, mais elle entrerait en conflit physiquement et électrostatiquement avec UmuD' lié. En d'autres termes, la queue aide à déclencher l'alarme SOS tout en restreignant le bras de la réponse le plus susceptible d'entraîner des mutations.
Impact sur la réponse aux antibiotiques dans des cellules vivantes
Pour tester comment cela se traduit à l'intérieur des bactéries, les chercheurs ont conçu des souches d'Escherichia coli dans lesquelles un rapporteur fluorescent s'allume lorsque le gène SOS précoce recN est activé. Ils ont ensuite traité ces souches avec deux agents endommageant l'ADN : la mitomycine C et l'antibiotique largement utilisé ciprofloxacine. Les cellules portant RecA normal montraient une forte activation SOS. Les cellules dépourvues de la queue, en revanche, produisaient des signaux fluorescents beaucoup plus faibles, cohérents avec une réduction du clivage de LexA et une réponse SOS atténuée. Les queues mutantes qui renforçaient la liaison à l'ADN et la formation de filament entraînaient, au contraire, souvent une réponse SOS encore plus forte. Ces résultats in vivo correspondent aux observations biochimiques et soulignent le rôle de la queue dans l'équilibre entre réparation, survie et mutation sous stress antibiotique.
Pourquoi cette petite queue compte
Ce travail révèle la queue C-terminale de RecA comme un régulateur subtil mais puissant de la maintenance du génome bactérien. En contactant le noyau de la protéine et en rapprochant ou en éloignant l'ADN et les protéines partenaires, la queue ralentit la croissance des filaments et l'échange de brins d'ADN, contribue à déclencher correctement la réponse SOS via LexA et atténue la réparation mutagène excessive via UmuD. Pour le grand public, cela importe parce que RecA et le système SOS influencent la rapidité avec laquelle les bactéries développent une résistance aux antibiotiques. Comprendre les astuces structurelles et fonctionnelles de cette petite queue pourrait, à l'avenir, guider la conception de médicaments qui favorisent la réparation sans mutation incontrôlée, rendant les antibiotiques existants plus efficaces plus longtemps.
Citation: Su, L., Li, X., Wang, F. et al. Mechanistic insights into the structure and function of the RecA C-terminal tail. Commun Biol 9, 526 (2026). https://doi.org/10.1038/s42003-026-09788-4
Mots-clés: Protéine RecA, Réponse SOS, Réparation de l'ADN, Résistance aux antibiotiques, Stabilité du génome bactérien