Clear Sky Science · nl
Mechanistische inzichten in de structuur en functie van de C‑terminale staart van RecA
Hoe bacteriën omgaan met DNA‑stress
Bacteriën worden continu blootgesteld aan factoren die hun DNA beschadigen, van antibiotica tot straling. Toch overleven ze vaak en worden ze soms zelfs moeilijker te doden. Deze studie bekijkt nauwkeurig een sleuteleiwit in bacteriën genaamd RecA, dat helpt gebroken DNA te herstellen en een noodprogramma op gang brengt dat bekendstaat als de SOS‑reactie. De auteurs richten zich op een kleine, flexibele staart aan één uiteinde van RecA die lange tijd ontsnapte aan structurele studies, en tonen aan hoe dit kleine stukje fungeert als een ingebouwde rem en schakelaar voor DNA‑herstel en overleving bij aanwezigheid van antibiotica.
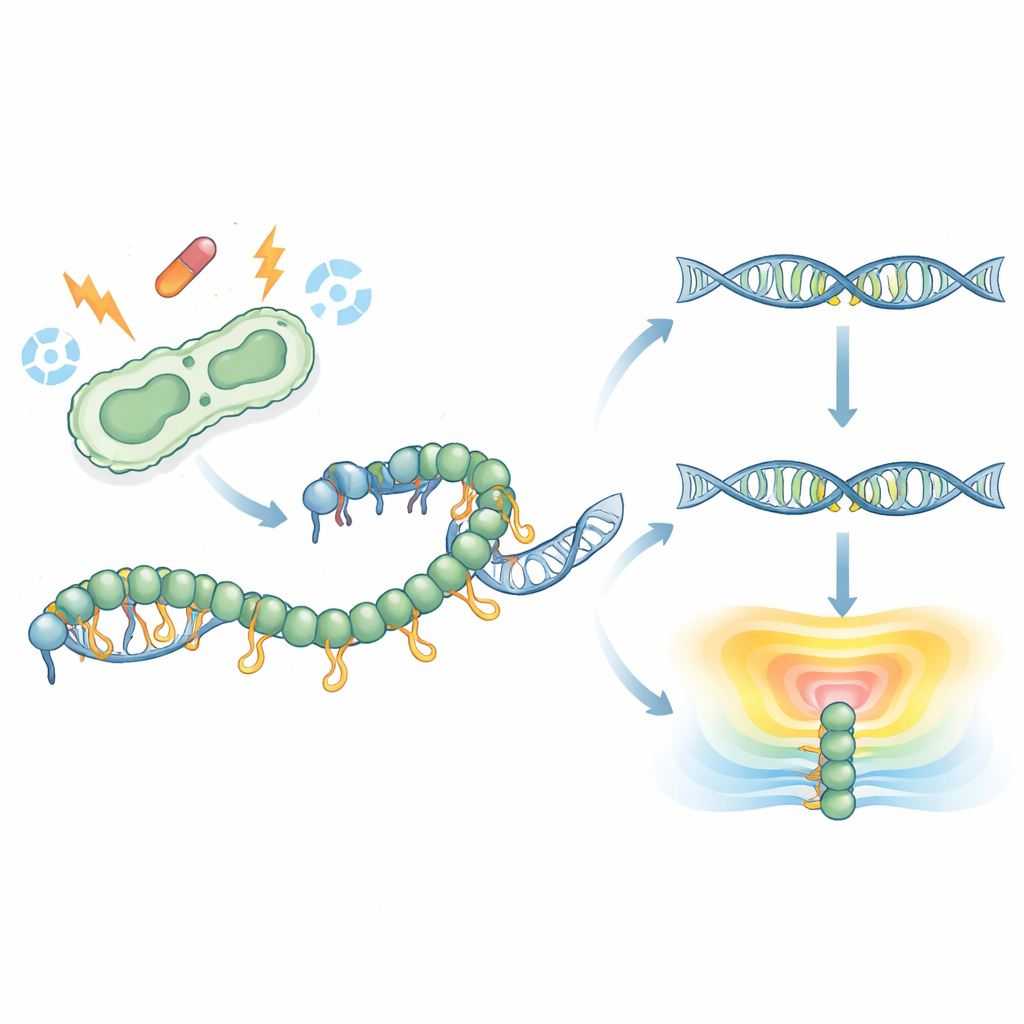
Een moleculaire eerste blik op een verborgen staart
RecA wikkelt zich rond enkelstrengs DNA om een filament te vormen dat DNA‑herstel aandrijft en de SOS‑reactie activeert. Eerdere structuren hadden nooit de slappe C‑terminale staart van RecA vastgelegd, waardoor de rol ervan onduidelijk bleef. Hier losten de onderzoekers een hoge‑resolutie kristalstructuur op van het volledige RecA uit de ziekteverwekker Klebsiella pneumoniae, gebonden aan een ATP‑achtig molecuul. Tot hun verrassing vouwde een deel van de staart zich tot een korte, geordende streng en reikte over om contact te maken met het centrale motorische gebied van een RecA‑molecuul in een aangrenzend filament. Deze interactie verbindt negatieve ladingen op de staart met positieve ladingen op de kern, en onthult een eerder ongeziene manier waarop RecA‑moleculen elkaar kunnen aanraken en in hogere‑orde structuren kunnen assembleren.
Een ingebouwde rem op DNA‑binding en herstel
Omdat de staart dicht bij de DNA‑bindende gebieden van RecA zit, onderzocht het team hoe deze het contact met DNA beïnvloedt. Met behulp van gel‑shift‑assays toonden ze aan dat RecA‑varianten zonder staart, of met ladingsveranderende mutaties in de staart, zowel enkelstrengs als dubbelstrengs DNA strakker vasthielden dan het normale eiwit. Elektronenmicroscopie bevestigde dat deze gewijzigde eiwitten langere RecA‑filamenten op korte DNA‑stukjes vormden dan het volledige eiwit. In directe strenguitwisselingsexperimenten, die het hart van homologe recombinatie nabootsen, voerden RecA zonder staart of met staartmutaties de DNA‑uitwisseling efficiënter uit. Samen laten deze resultaten zien dat de staart normaal fungeert als een autoinhibitorisch element: hij bemoeilijkt de binding van RecA aan DNA, het uitrekken langs DNA en het uitvoeren van genetische strenguitwisseling, en helpt zo ongecontroleerde recombinatie op intacte chromosomen te voorkomen.
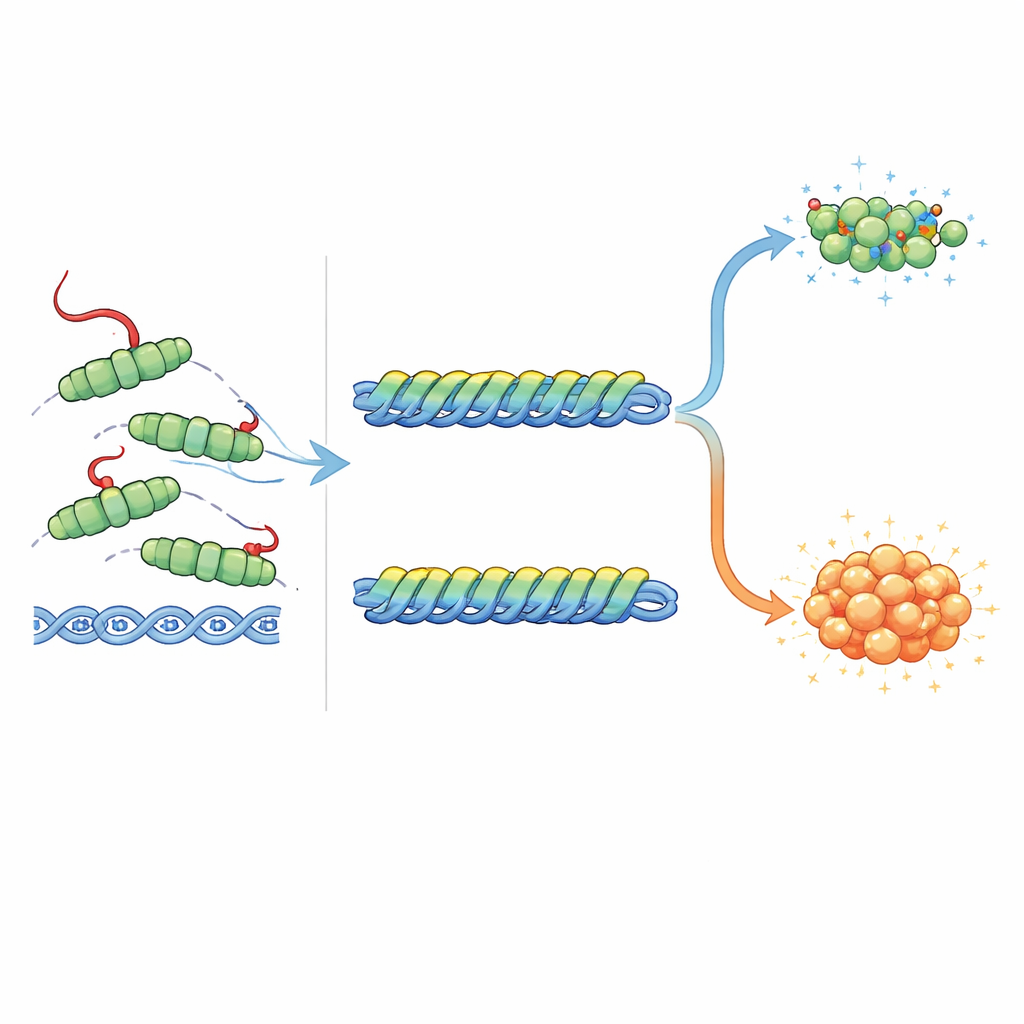
Het fijn afstellen van het bacteriële SOS‑alarm
De taak van RecA is niet alleen DNA repareren, maar ook de SOS‑reactie in gang zetten door twee andere eiwitten, LexA en UmuD, te helpen bij zelfknip. LexA houdt normaal gesproken SOS‑genen stil; wanneer het geknipt wordt, worden die genen geactiveerd. Knippen van UmuD levert een partner op voor een speciale foutgevoelige DNA‑polymerase die beschadigingen kan voorbijgaan maar ook mutaties introduceert. De auteurs ontdekten dat de RecA‑staart tegengestelde effecten heeft op deze twee zelfknipreacties. Volledig RecA, met een intacte staart, was het beste in het bevorderen van LexA‑knip, terwijl staartloze of sterk veranderde versies minder effectief waren. Daarentegen stimuleerden dezelfde staartloze en gemuteerde vormen de UmuD‑knip beter dan het normale eiwit. Structurele vergelijkingen suggereren waarom: de staart kan comfortabel liggen nabij gebonden LexA en zelfs gunstige ladingsinteracties vormen, maar zou fysiek en elektrostatistisch in conflict komen met gebonden UmuD′. Met andere woorden: de staart helpt het SOS‑alarm aan te zetten terwijl hij de meest mutagene tak van de reactie beperkt.
Effect op antibiotica‑respons in levende cellen
Om te testen hoe dit zich binnen bacteriën uitwerkt, construeerden de onderzoekers Escherichia coli‑stammen waarin een fluorescerende reporter oplicht wanneer een vroeg SOS‑gen genaamd recN wordt geactiveerd. Ze behandelden deze stammen vervolgens met twee DNA‑schadende middelen: mitomycine C en het veelgebruikte antibioticum ciprofloxacine. Cellen met normaal RecA toonden sterke SOS‑activatie. Cellen zonder staart produceerden daarentegen veel zwakkere fluorescentiesignalen, wat consistent is met verminderde LexA‑knip en een afgezwakte SOS‑reactie. Mutante staarten die DNA‑binding en filamentvorming versterkten, veroorzaakten daarentegen vaak een nog sterkere SOS‑reactie. Deze in‑cellen resultaten komen overeen met de biochemische bevindingen en benadrukken de rol van de staart in het balanceren van herstel, overleving en mutatie onder antibioticadruk.
Waarom deze kleine staart ertoe doet
Dit werk onthult de C‑terminale staart van RecA als een subtiele maar krachtige regulator van bacterieel genoomonderhoud. Door contact te maken met de kern van het eiwit en DNA en partner‑eiwitten dichterbij of verder weg te duwen, vertraagt de staart filamentgroei en DNA‑strenguitwisseling, helpt hij ervoor te zorgen dat de SOS‑reactie op passende wijze via LexA wordt geactiveerd, en dempt hij excessief mutageen herstel via UmuD. Voor het bredere publiek is dit relevant omdat RecA en het SOS‑systeem beïnvloeden hoe snel bacteriën resistentie tegen antibiotica ontwikkelen. Inzicht in de structurele en functionele trucs van deze kleine staart kan in de toekomst helpen bij het ontwerpen van geneesmiddelen die het evenwicht verschuiven richting herstel zonder ongecontroleerde mutatie, waardoor bestaande antibiotica langer effectief blijven.
Bronvermelding: Su, L., Li, X., Wang, F. et al. Mechanistic insights into the structure and function of the RecA C-terminal tail. Commun Biol 9, 526 (2026). https://doi.org/10.1038/s42003-026-09788-4
Trefwoorden: RecA‑eiwit, SOS‑reactie, DNA‑herstel, antibioticaresistentie, stabiliteit van het bacteriële genoom