Clear Sky Science · pt
Percepções mecanicistas sobre a estrutura e função da cauda C-terminal do RecA
Como as bactérias lidam com o estresse do DNA
As bactérias estão constantemente expostas a agentes que danificam seu DNA, desde antibióticos até radiação. Ainda assim, muitas vezes sobrevivem e até se tornam mais difíceis de eliminar. Este estudo examina de perto uma proteína bacteriana-chave chamada RecA, que ajuda a reparar quebras no DNA e a ativar um programa de emergência conhecido como resposta SOS. Os autores focam numa pequena e flexível cauda na extremidade do RecA que durante muito tempo escapou aos estudos estruturais, e mostram como essa pequena parte atua como um freio e um interruptor integrado para o reparo do DNA e a sobrevivência a antibióticos.
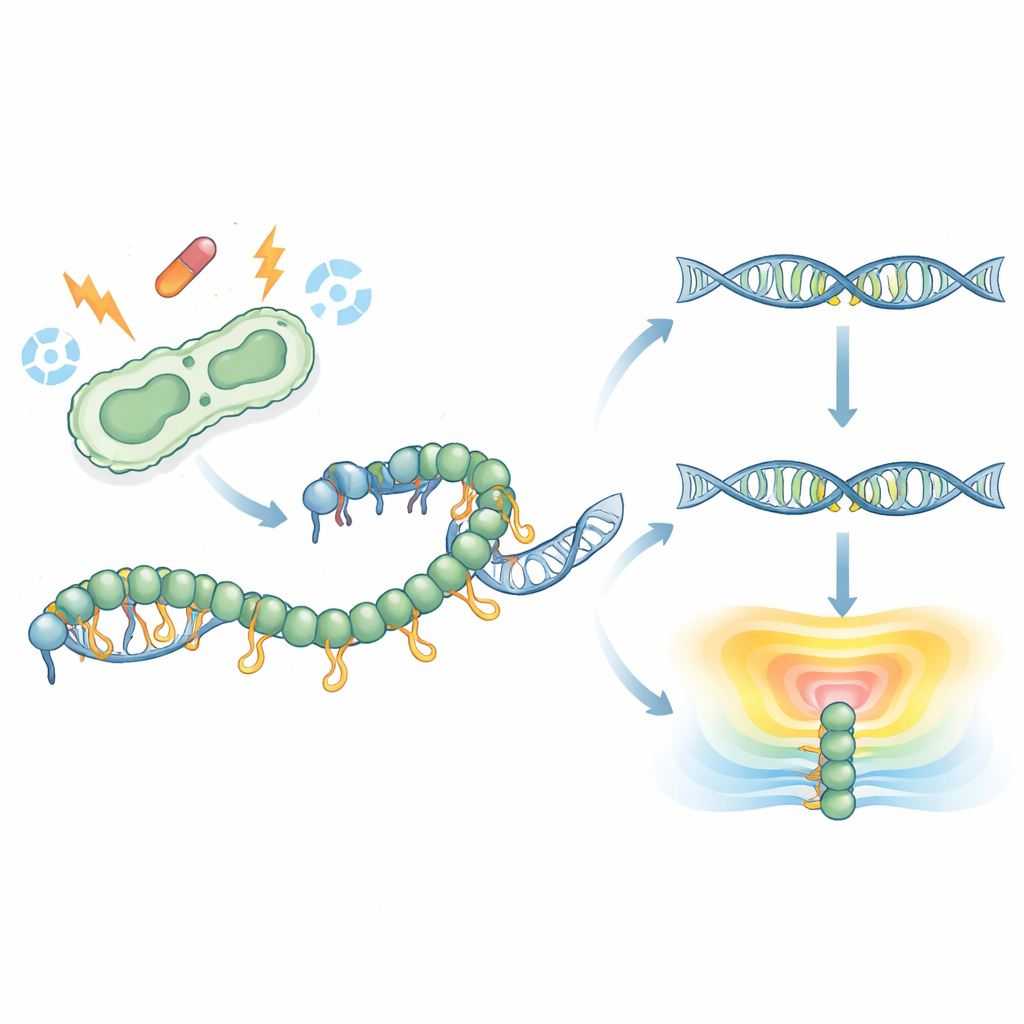
Um primeiro olhar molecular a uma cauda oculta
O RecA envolve-se em torno de fitas simples de DNA para formar um filamento que impulsiona o reparo do DNA e ativa a resposta SOS. Estruturas anteriores nunca haviam capturado a cauda C-terminal flexível do RecA, deixando seu papel misterioso. Aqui, os pesquisadores resolveram a estrutura cristalina de alta resolução do RecA de comprimento total do patógeno Klebsiella pneumoniae ligado a uma molécula semelhante ao ATP. Para surpresa deles, parte da cauda se dobrou em uma faixa curta e ordenada e alcançou para contatar a região motora central de uma molécula de RecA em um filamento vizinho. Essa interação une cargas negativas da cauda a cargas positivas no núcleo, revelando uma forma até então não vista de como moléculas de RecA podem se tocar e se montar em estruturas de ordem superior.
Um freio embutido na ligação e no reparo do DNA
Como a cauda fica próxima às regiões de ligação ao DNA do RecA, a equipe testou como ela afeta o contato com o DNA. Usando ensaios de mudança de mobilidade em gel, mostraram que versões do RecA sem a cauda, ou com alterações que mudam cargas na cauda, capturaram tanto DNA de fita simples quanto de fita dupla com mais afinidade do que a proteína normal. Microscopia eletrônica confirmou que essas proteínas alteradas formaram filamentos RecA mais longos em pedaços curtos de DNA do que a proteína de comprimento total. Em experimentos diretos de troca de fitas, que imitam o cerne da recombinação homóloga, o RecA sem cauda ou com mutações na cauda realizou a troca de DNA de forma mais eficiente. Em conjunto, esses resultados mostram que a cauda atua normalmente como um elemento autoinibitório: ela torna mais difícil para o RecA ligar-se ao DNA, estender-se ao longo dele e efetuar a troca de fitas genéticas, ajudando a prevenir recombinação descontrolada em cromossomos intactos.
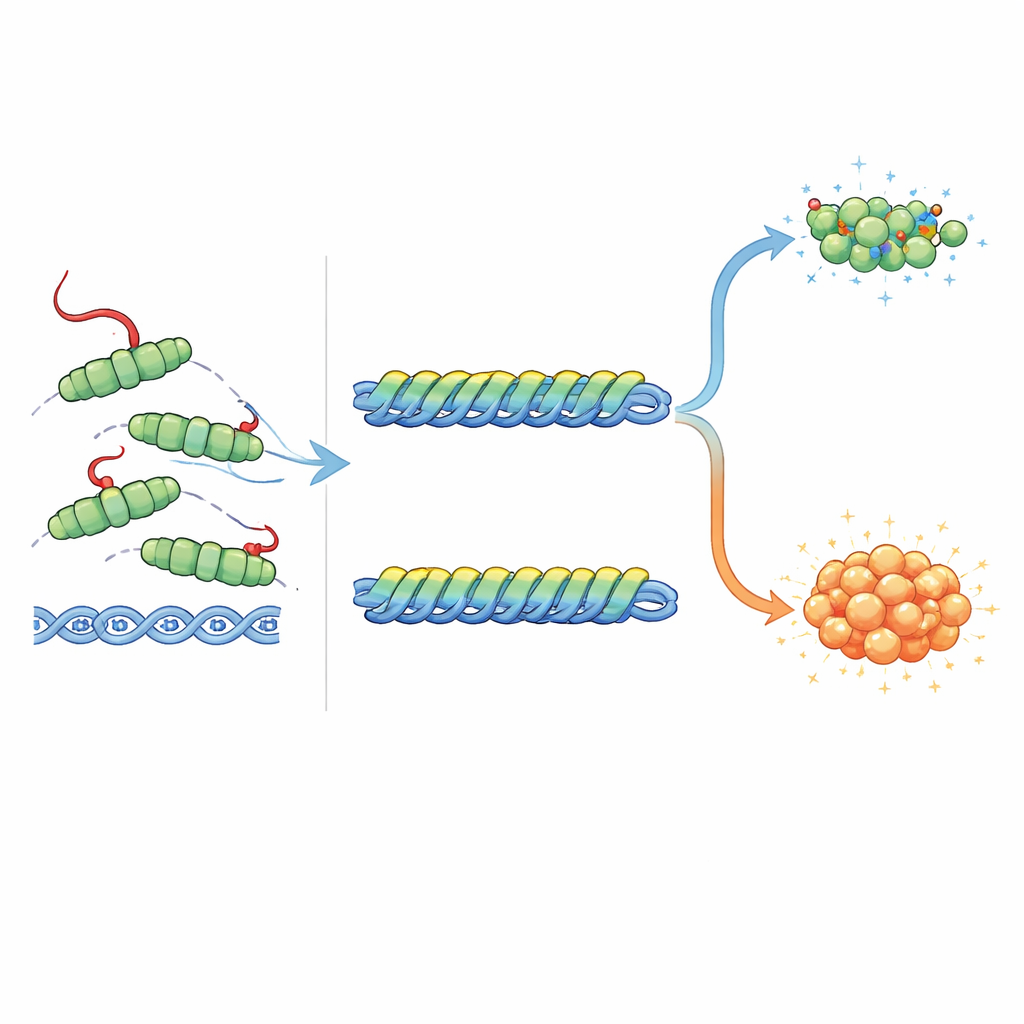
Fine‑tuning do alarme SOS bacteriano
O trabalho do RecA não é apenas reparar o DNA, mas também desencadear a resposta SOS ao ajudar duas outras proteínas, LexA e UmuD, a se autocortarem. A LexA normalmente mantém os genes SOS silenciados; quando é clivada, esses genes são ativados. A clivagem de UmuD gera um parceiro para uma DNA polimerase especial, propensa a erros, que pode copiar além dos danos, mas também introduz mutações. Os autores descobriram que a cauda do RecA tem efeitos opostos nessas duas autoclivagens. O RecA de comprimento total, com sua cauda intacta, foi o melhor em promover a clivagem da LexA, enquanto as versões sem cauda ou fortemente alteradas foram piores. Em contraste, as mesmas formas sem cauda e mutantes foram melhores em estimular a clivagem de UmuD do que a proteína normal. Comparações estruturais sugerem o motivo: a cauda pode acomodar‑se confortavelmente perto da LexA ligada e até formar interações de carga favoráveis, mas colidiria física e eletrostaticamente com a UmuD′ ligada. Em outras palavras, a cauda ajuda a acionar o alarme SOS ao mesmo tempo em que contém o braço mais propenso a causar mutações da resposta.
Impacto na resposta a antibióticos em células vivas
Para testar como isso se manifesta dentro das bactérias, os pesquisadores criaram linhagens de Escherichia coli nas quais um repórter fluorescente brilha quando um gene SOS inicial chamado recN é ativado. Em seguida, trataram essas linhagens com dois agentes que danificam o DNA: mitomicina C e o antibiótico amplamente usado ciprofloxacino. Células com RecA normal mostraram forte ativação da SOS. Células sem a cauda, porém, produziram sinais fluorescentes muito mais fracos, consistente com redução da clivagem da LexA e uma resposta SOS atenuada. Caudas mutantes que fortaleceram a ligação ao DNA e a formação de filamentos, por outro lado, frequentemente impulsionaram uma resposta SOS ainda mais forte. Esses resultados em células correspondem às descobertas bioquímicas e destacam o papel da cauda em equilibrar reparo, sobrevivência e mutação sob estresse por antibióticos.
Por que essa pequena cauda importa
Este trabalho revela a cauda C-terminal do RecA como um regulador sutil, porém potente, da manutenção do genoma bacteriano. Ao contatar o núcleo da proteína e empurrar o DNA e as proteínas parceiras para mais perto ou mais longe, a cauda desacelera o crescimento do filamento e a troca de fitas de DNA, ajuda a garantir que a resposta SOS seja acionada de forma apropriada via LexA e modera reparos mutagênicos excessivos via UmuD. Para o público em geral, isso importa porque o RecA e o sistema SOS influenciam a rapidez com que as bactérias evoluem resistência a antibióticos. Entender as artimanhas estruturais e funcionais dessa pequena cauda pode, no futuro, orientar o desenho de fármacos que inclinem o equilíbrio em favor do reparo sem mutação descontrolada, tornando os antibióticos existentes mais eficazes por mais tempo.
Citação: Su, L., Li, X., Wang, F. et al. Mechanistic insights into the structure and function of the RecA C-terminal tail. Commun Biol 9, 526 (2026). https://doi.org/10.1038/s42003-026-09788-4
Palavras-chave: proteína RecA, resposta SOS, reparo de DNA, resistência a antibióticos, estabilidade do genoma bacteriano